
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчет изменения энтропии для различных процессов
|
|
|
|
Обратимый цикл Карно
Из п. 5.2 мы знаем, что в тепловой машине, работающей по принципу Карно, имеются три тела: холодильник, нагреватель, рабочее тело (газ).
Изменение энтропии газа в тепловой машине 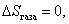 так как газ возвращается в исходное состояние.
так как газ возвращается в исходное состояние.
Изменение энтропии нагревателя:
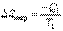 . .
| (6.4.1) |
Для холодильника:
 . .
| (6.4.2) |
 . .
|
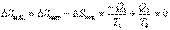 . .
|
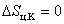 или или
| 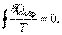
| (6.4.3) |
т.е. S – константа. Таким образом, мы пришли к выражению, полученному в п. 6.1, называемому равенство Клаузиуса.
Термодинамические расчеты изменения энтропии основаны на определении (6) и на свойствах частных производных энтропии по термодинамическим параметрам:
(8)
Последние два тождества представляют собой соотношения Максвелла.
1) Нагревание или охлаждение при постоянном давлении.
Количество теплоты, необходимое для изменения температуры системы, выражают с помощью теплоемкости: Qобр = Cp dT.
(9)
Если теплоемкость не зависит от температуры в интервале от T1 до T2, то уравнение (4.8) можно проинтегрировать:
(10)
Если изменение температуры происходит при постоянном объеме, то в формулах (9) и (10) Cp надо заменить на CV.
2) Изотермическое расширение или сжатие.
Для расчета энтропии в этом случае надо знать уравнение состояния системы. Расчет основан на использовании соотношения Максвелла:
(11)
В частности, для изотермического расширения идеального газа (p = nRT / V)
(12)
Этот же результат можно получить, если использовать выражение для теплоты изотермического обратимого расширения идеального газа: Qобр = nRT ln(V2/V1).
3) Фазовые переходы.
При обратимом фазовом переходе температура остается постоянной, а теплота фазового перехода при постоянном давлении равна Hфп, поэтому изменение энтропии равно:
|
|
|
(13)
При плавлении и кипении теплота поглощается, поэтому энтропия в этих процессах возрастает: Sтв < Sж < Sг. При этом энтропия окружающей среды уменьшается на величину Sф.п., поэтому изменение энтропии Вселенной равно 0, как и полагается для обратимого процесса в изолированной системе.
4) Смешение идеальных газов при постоянных температуре и давлении.
Если n1 молей одного газа, занимающего объем V1, смешиваются с n2 молями другого газа, занимающего объем V2, то общий объем будет равен V1 + V2, причем газы расширяются независимо друг от друга и общее изменение энтропии равно сумме изменений энтропии каждого газа:
, (14)
где xi - мольная доля i-го газа в полученной газовой смеси. Изменение энтропии (14) всегда положительно, т.к. все ln xi < 0, поэтому идеальные газы всегда смешиваются необратимо.
Если при тех же условиях смешиваются две порции одного и того же газа, то уравнение (14) уже неприменимо. Никаких изменений в системе при смешивании не происходит, и S = 0. Тем не менее, формула (14) не содержит никаких индивидуальных параметров газов, поэтому, казалось бы, должна быть применима и к смешению одинаковых газов. Это противоречие называют парадоксом Гиббса.
Впорос 17
Цикл Отто — термодинамический цикл, описывающий рабочий процесс двигателя внутреннего сгорания с воспламенением сжатой смеси от постороннего источника энергии, цикл бензинового двигателя. Назван в честь немецкого инженера Николауса Отто.
Идеальный цикл Отто состоит из четырёх процессов:


p-V диаграмма цикла Отто
· 1—2 адиабатное сжатие рабочего тела;
· 2—3 изохорный подвод теплоты к рабочему телу;
· 3—4 адиабатное расширение рабочего тела;
· 4—1 изохорное охлаждение рабочего тела.
КПД цикла Отто 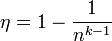 ,
,
где  — степень сжатия,
— степень сжатия,
 — показатель адиабаты.
— показатель адиабаты.
Идеальный цикл лишь приблизительно описывает процессы, происходящие в реальном двигателе, но для технических расчётов в большинстве случаев точность такого приближения удовлетворительна.
|
|
|
Цикл Дизеля — термодинамический цикл, описывающий рабочий процесс двигателя внутреннего сгорания с воспламенением впрыскиваемого топлива от разогретого рабочего тела, цикл дизельного двигателя.
Идеальный цикл Дизеля состоит из четырёх процессов:


p-V диаграмма цикла Дизеля
· 1—2 адиабатное сжатие рабочего тела;
· 2—3 изобарный подвод теплоты к рабочему телу;
· 3—4 адиабатное расширение рабочего тела;
· 4—1 изохорное охлаждение рабочего тела.
КПД цикла Дизеля  ,
,
где  — степень сжатия,
— степень сжатия,
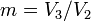 — коэффициент предварительного расширения,
— коэффициент предварительного расширения,
 — показатель адиабаты.
— показатель адиабаты.
Идеальный цикл лишь приблизительно описывает процессы, происходящие в реальном двигателе, но для технических расчётов в большинстве случаев точность такого приближения удовлетворительна.
Цикл д. в. с. с подводом тепла при постоянном объёме (цикл Отто)
Является прототипом рабочего процесса в двигателях с принудительным зажиганием. Отличительной особенностью таких двигателей является сжатие горючей смеси (смеси паров бензина с воздухом). Этот цикл состоит из двух адиабат и двух изохор (рис. 7.2). Адиабата 1—2 отвечает сжатию горючей смеси, изохора 2—3 — сгоранию смеси (подвод теплоты q1), вследствие чего давление повышается до р3. После этого продукты сгорания адиабатно расширяются (процесс 3—4). В изохорном процессе 4—1 от газа отводится теплота q2.

|
| Рис. 7.2. Цикл д. в. с. с изохорным подводом теплоты |
Это цикл двухтактного д. в. с. Между точками 4-1 практически при постоянном объёме осуществляется сначала выпуск отработавших газов а затем и продувка цилиндра смесью топлива с воздухом (карбюраторные д. в. с.) или воздухом (дизельные д. в. с.).
Характеристиками этого цикла являются:
степень сжатия 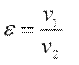 и
и
степень повышения давления  . Здесь v1, v2, p2, p3 – объёмы и давления рабочего тела в соответствующих точках цикла д. в. с.
. Здесь v1, v2, p2, p3 – объёмы и давления рабочего тела в соответствующих точках цикла д. в. с.
Расчёт цикла сводится к определению параметров p, v и T в характерных точках и определению количеств подведенного и отведенного тепла, полезной работы и термического к. п. д. цикла.
Можно показать, что термический к. п. д. цикла
|
|
|
 , ,
| (7.1) |
где k – показатель адиабаты рабочего тела. То есть ηt растёт с увеличением степени сжатия. Однако повышение степени сжатия не должно вызывать детонацию и самовоспламенение горючей смеси в процессе сжатия. В зависимости от вида топлива ε =6÷10.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 992; Нарушение авторских прав?; Мы поможем в написании вашей работы!