
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тема 10. Окислительно-восстановительные реакции
|
|
|
|
ТЕМА 9. ГЕТЕРОГЕННЫЕ РАВНОВЕСИЯ. ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ
171. Растворимость ВаСО3 равна 8,9·10–5 моль/л. Вычислить произведение растворимости карбоната бария.
172. Произведение растворимости МgF2 равно 7,0·10–9. Вычислите растворимость этой соли в молях на литр и в граммах на литр.
173. Вычислите произведение растворимости карбоната стронция, если в 5 л насыщенного раствора содержится 0,05 г этой соли.
174. Сколько воды потребуется для растворения 1 г ВаСО3, произведение растворимости которого равно 1,9·10–9?
175. Произведение растворимости РbI2 равно 8,7·10–6. Вы числить концентрацию ионов Рb2+ и ионов I– в насыщенном растворе иодида свинца.
176. Растворимость АgI равна 1,2·10–8 моль/л. Вычислите произведение растворимости АgI.
177. Растворимость Fе(ОН)3 равна 1,9·10–10 моль/л. Вычислить произведение растворимости Fе(ОН)3.
178. В 2 л воды при температуре 25°С растворяется 2,2·10–4 г бромида серебра. Вычислите произведение растворимости АgВr.
179. Растворимость сульфата бария в воде равна 2,45·10–3 г/л. Вычислите произведение растворимости ВаSО4.
180. Произведение растворимости РbSО4 равно 2,3·10–8. Сколько литров воды потребуется для растворения 1г РbSО4?
181. Произведение растворимости СаSO4 равно 6,0·10–5. Вы падает ли осадок СаSО4, если смешать равные объемы 0,2 М растворов СаС12 и Н2SО4.
182. Произведение растворимости СаСО3 равно 4,8·10–9. Вы падает ли осадок, если смешать равные объемы 0,001М растворов СаС12 и Na2СО3?
183. Произведение растворимости АgС1 равно 1,8·10–10. Вы падает ли осадок, если смешать 20 мл 0,01 M раствора КС1 с 6 мл 0,01 M раствора АgNO3.
184. Растворимость СаСО3 при 18°С равна 6,9·10–5 моль/л. Вычислите произведение растворимости СаСО3.
185. Растворимость РbВr2 при 18°С равна 2,7·10–2 моль/л. Вы числите произведение растворимости РbВr2.
|
|
|
186. Растворимость ВаСО3 равна 8,9·10–4 моль/л. Вычисли те концентрации ионов [Ва2+] и [СО32–] (моль/л), а также про изведение растворимости ВаСО3.
187. Произведение растворимости Аg2Сr2О7 равно 2,0·10–7. Выпадет ли осадок при смешении равных объемов 0,01 н. растворов АgNО3 и К2Сr2О7.
188. В 6 литрах насыщенного раствора РbSO4 содержится 0,186 г иона свинца(II). Вычислить произведение растворимости.
189. Произведение растворимости сульфата цинка ПP = 2,3·10–8. Образуется ли осадок, если к 0,1 М раствору Na2SО4 прибавить равный объем 0,1 М. раствора ацетата свинца Рb(СН3СОО)2?
190. Растворимость AgCl в воде при 25°С равна 1,3·10–5 моль/л. Вычислите произведение растворимости хлорида серебра при этой температуре и его растворимость в граммах на литр.
191. Дайте определение понятию окислительно-восстановительные реакции. Какие из приведенных ниже реакций являются окислительно-восстановительными:
а) 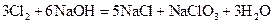 .
.
б) 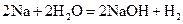 ;
;
в) 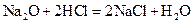 ;
;
192. Какие частицы называют восстановителями. Руководствуясь строением атомов, решите, могут ли фигурировать в качестве восстановителей следующие ионы: Sn2+, Cl–, Zn2+.
193. Дайте определение понятию степень окисления. Определите степень окисления центрального атома в следующих ионах: SO42–, SO32–, S2O32–.
194. Какие частицы называют окислителями. Укажите, какие из перечисленных ионов могут быть окислителями: Fe3+, Br–, Cr3+
195. Какие из перечисленных частиц обладают двойственной окислительно-восстановительной природой, почему?
а) N–3, N20, N+3;
б) H–1, H20, H+1;
в) Fe2+, Fe3+, Fe+6;
г) C+2, Cu+1, F–1.
196. Укажите, какие из перечисленных частиц являются только окислителями:
а) Cl+7, O20, F20;
б) N+5, S+6, Cl+3;
в) H+, Br+7, C+4;
г) Cr+6, Mn+7, Mn+4.
197. Укажите, какие из перечисленных частиц являются только восстановителями:
а) Ca0, N–3, O–1;
б) H–, I–, Na+;
в) O–2, Cu+1, C+4.
198. Окислительно-восстановительные реакции выражаются приведенными схемами:
а) P + HIO3 + H2O® H3PO4 + HI;
|
|
|
б) 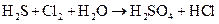 ;
;
в) KMnO4 + N2H4 + H2SO4 ® N2 + MnSO4 + K2SO4 + H2O;
г) HgS + HCl + HNO3 ® S + HgCl2 + NO + H2O;
д) FeSO4 + HNO3 ® Fe(NO3)3 + NO + H2SO4 + H2O;
е) Mg + HNO3 ® NH4NO3 + Mg(NO3)2 + H2O;
ж) 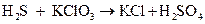 ;
;
з) 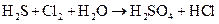 ;
;
и)  ;
;
к) 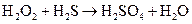 ;
;
л) 
м)  ;
;
н)  ;
;
о)  ;
;
п) 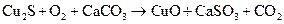 ;
;
Подберите коэффициенты в предложенных реакциях методом электронного баланса. Укажите, какое вещество в каждом взаимодействии является окислителем, какое – восстановителем.
199. Окислительно-восстановительные реакции выражаются ионными уравнениями:
а)  ;
;
б) 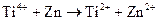 ;
;
в) 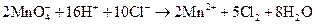 ;
;
г) 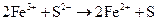 ;
;
д) 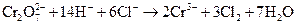 ;
;
е) 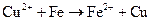
Составьте электронные и молекулярные уравнения. Для каждой реакции укажите, какой ион является восстановителем, какой – окислителем.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 622; Нарушение авторских прав?; Мы поможем в написании вашей работы!