
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Індивідуальні завдання для самостійного приготування розчинів
|
|
|
|
Методика приготування 100 мл розчину купрум(ІІ) сульфату з молярною концентрацією безводної солі 0,1 моль/л.
Приготування розчину за наважкою кристалогідрату
Дослід ІІІ
а) Зважити на технічних терезах наважку кристалогідрату пентааква купрум(ІІ) сульфату. Для цього потрібно провести розрахунки. Масу кристалогідрату визначають за рівняннями
C x = m (CuSO4) / M (CuSO4). V (p)
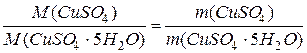
б) Кількісно перенести наважку солі у мірну колбу на 100 мл.
в) Невеликими порціями доливати у колбу воду до повного розчинення солі. Для розрахунку необхідної маси води використовуємо формулу
mр-ну = m (CuSO4 . 5 H2O) + m (H2O).
г) Після повного розчинення солі довести рівень води в колбі до мітки так, щоб нижній меніск опинився на рівні мітки.
д) Закривши колбу пробкою перемішати отриманий розчин.
е) Визначити похибку експерименту.
1. Приготувати 100 мл розчину натрій сульфату з масовою часткою 15 %.
2. Приготувати 100 мл розчину калій карбонату с молярною концентрацією еквівалента 0,5 моль/л.
3. Приготувати 100 мл розчину калій хлориду з молярною концентрацією 0,5 моль/л.
4. Приготувати 100 мл розчину купрум сульфату з масосою часткою 5 %.
5. Приготувати 100 мл розчину амоній сульфату з молярною концентрацією 0,25 моль/л.
6. Приготувати 100 мл розчину амоніаку з масовою часткою 10 %.
7. Приготувати 100 мл розчину ацетатної кислоти з молярною концентрацією 2 моль/л.
8. Приготувати 100 мл розчину амоніаку з молярною концентрацією еквівалента 0,1 моль/л.
9. Приготувати 100 мл розчину ацетатної кислоти з масовою часткою 20 %.
10. Приготувати 100 мл розчину нітратної кислоти з масовою часткою 20 %.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 361; Нарушение авторских прав?; Мы поможем в написании вашей работы!