
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Введение. Способы выражения состава растворов
|
|
|
|
РАСТВОРЫ
Растворами называются такие системы, в которых одно вещество равномерно распределено в среде другого или других веществ. В общем случае этот термин может относиться к любому агрегатному состоянию системы. Сюда входят и смеси газов, и жидкие растворы, и твердые растворы или смешанные кристаллы.
Процесс растворения в общем случае отнюдь не представляет собой простого распределения молекул или ионов одного вещества среди молекул или ионов другого, но большей частью связан с различными взаимодействиями химического и физического характера между ними.
Когда речь идет о жидких растворах, то нередко пользуются понятиями растворителя и растворенного вещества. В случае растворов газов или твердых веществ в жидкостях растворителем считается обычно жидкость, а растворенным веществом— растворенный газ или твердое вещество, независимо от их относительного количественного содержания. В случае же растворов, жидкостей в жидкостях применение этих понятий не всегда целесообразно.
Когда компоненты обладают ограниченной смешиваемостью, то растворителем является тот из них, прибавление которого к раствору возможно в неограниченном количестве без нарушения гомогенности. Растворенным же веществом считается тот компонент, растворимость которого в данном растворе ограничена.
Если компоненты обладают неограниченной взаимной растворимостью, то можно выделить два случая. При значительном различии содержания компонентов в растворе растворителем называется обычно тот из них, который присутствует в относительно большем количестве, а остальные компоненты называются растворенными веществами. Так, при растворении небольшого количества спирта в большом количестве воды можно считать этот раствор раствором спирта в воде и называть воду растворителем, а спирт растворенным веществом. В обратном же случае, т. е. при растворении небольшого количества воды в большом количестве спирта, можно считать растворителем спирт, а воду растворенным веществом. В области промежуточных составов, когда различие в. относительном содержании компонентов невелико, применение этих понятий становится нецелесообразным и может привести к недоразумениям. Количественный состав растворов выражают различными способами. Широко распространено выражение его в массовых % или массовых долях. В физической химии чаще характеризуют его в мольных % или мольных долях, так как зависимость свойств растворов от состава обычно проще при выражении его соотношением мольных количеств компонентов.
|
|
|
Мольная доля Ni компонента iравна отношению числа молей ni этого компонента к сумме чисел молей (ni + n2 + nз+ … + nk)всех K компонентов раствора и определяется по формуле:
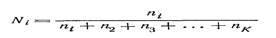
Мольную долю называют также молярной или молекулярной долей или дробью. Мольный процент равен 100 Ni.
Когда компонентами жидкого раствора являются жидкости или когда речь идет о газовых смесях, в некоторых случаях сопоставляют не весовые или мольные, а объемные количества компонентов; при этом выражают состав или в объемных долях, или в объемных процентах, или в объемных отношениях. Например, градусы крепости водно-спиртовых смесей выражают объемный процент спирта в растворе.
Объемная доля φi компонента i определяется по формуле:
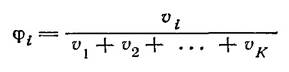

Когда концентрация выражается числом молей растворенного вещества в 1 л раствора, она называется молярностью. В некоторых случаях содержание растворенного вещества относят не к количеству раствора в целом, а к тому или иному количеству растворителя. Так, концентрация, выраженная числом молей растворенного вещества на 1000 г растворителя, называется моляльностью.
|
|
|
|
|
Дата добавления: 2015-06-25; Просмотров: 454; Нарушение авторских прав?; Мы поможем в написании вашей работы!