
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теоретические основы метода. по дисциплине «Аналитическая химия»
|
|
|
|
Лабораторная работа № 1
ОПТИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Лабораторные работы
по дисциплине «Аналитическая химия»
по теме:
Специальность 1 - 49 01 02«Технология хранения и переработки животного сырья»
Специализация: 1 - 49 01 02 01 Технология мяса и мясопродуктов
Проверил Выполнили
Автушенко В.В. студенты группы ТЖМП – 111
___________________________ _______________________________
«_____» ______________ 2012 г. _______________________________
_______________________________
«_____» ____________________ 2012 г.
Могилев 2012
Фотоэлектроколориметрическое определение ионов Cu2+ в виде аммиачного комплекса методом добавок
Фотоэлектроколориметрия основана на поглощении света определяемым веществом в видимой части спектра (400–760 нм). Интенсивность светового потока при его прохождении через исследуемую среду уменьшается вследствие превращения энергии излучения в различные формы внутренней энергии вещества и (или) в энергию вторичного излучения. Поглощательная способность вещества зависит от электронного строения атомов и молекул, а также от длины волны и поляризации падающего света, толщины слоя, концентрации вещества, температуры. Для измерения поглощательной способности в данном методе используют фотоэлектроколориметры – оптические приборы, состоящие из источника света, камеры для образцов, монохроматора (призма или дифракционная решетка) и детектора.
Применение фотоэлектроколориметрии основано на основном законе светопоглощения, или законе Бугера-Ламберта-Бера, который связывает уменьшение интенсивности света с концентрацией раствора и толщиной слоя. Согласно закону Бугера-Ламберта-Бера, растворы одного и того же окрашенного вещества при одинаковой концентрации этого вещества и одинаковой толщине слоя раствора поглощают равное количество световой энергии, т.е. светопоглощение таких растворов одинаково.
|
|
|
Этот закон выражается уравнением:
 1
1
где I – интенсивность света прошедшего через раствор; I 0 – интенсивность падающего на раствор света; ε – молярный коэффициент поглощения; С – молярная концентрация окрашенного вещества в растворе, моль/л; l – толщина слоя светопоглощающего раствора, см.
После логарифмирования и смены знаков на обратные, уравнение (1) принимает следующий вид:
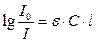 2
2
Величина lg I 0/ I является важной характеристикой окрашенного раствора; ее называют оптической плотностью и обозначают буквой D или А, тогда:
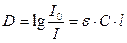 3
3
Из этого уравнения следует, что оптическая плотность раствора прямо пропорциональна концентрации окрашенного вещества и толщине слоя раствора.
Для определения концентрации анализируемого иона обычно используют следующие методы: метод добавок и метод калибровочного графика.
Метод добавок основан на сравнении оптической плотности исследуемого раствора и того же раствора с добавкой известного количества стандартного раствора определяемого вещества. Для определения неизвестной концентрации используют два способа.
1. Расчет по уравнению:
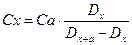 4
4
где С а – концентрация добавки в фотометрируемом растворе; D х – оптическая плотность исследуемого раствора без добавки стандартного раствора; D х+а – оптическая плотность исследуемого раствора с добавкой стандартного раствора.
2. Графический способ
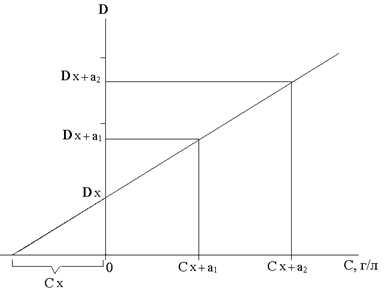
При определении неизвестной концентрации графическим способом на оси ординат откладывают значения оптической плотности исследуемого раствора D х (без добавки) и оптические плотности исследуемого раствора с двумя добавками D х+а1 и D х+а2, а на оси абсцисс – концентрации добавленного вещества С а1 и С а2 в анализируемом растворе.
Через полученные точки проводят прямую (рисунок 1) до пересечения с осью абсцисс в точке С х. Абсолютное значение отрезка 0Сх выражает неизвестную концентрацию исследуемого раствора.
|
|
|
|
| Рисунок 1 – Графическое определение концентрации анализируемого иона методом добавок |
Метод добавок применяют для определения малых количеств различных элементов в присутствии больших количеств посторонних.
Метод калибровочного графика. При использовании метода калибровочного графика готовят серию стандартных растворов с различной концентрацией определяемого иона и измеряют их оптическую плотность. Согласно основному закону светопоглощения между концентрацией C и оптической плотностью D существует прямолинейная зависимость, причем, если С = 0, то и D = 0 (рисунок 2):

|
| Рисунок 2 – Калибровочный график для определения концентрации анализируемого иона методом фотоэлектроколориметрии |
Измерив оптическую плотность исследуемого раствора D х, находят ее значение на оси ординат, а затем на оси абсцисс соответствующее значение С х.
Метод калибровочного графика применяют при выполнении серийных анализов. Этот метод позволяет определить концентрацию растворов даже в том случае, когда основной закон светопоглощения не соблюдается.
1.2 Цель работы: освоить навыки работы на фотоэлектроколориметре, определить содержание Cu2+ в водном растворе методом добавок.
1.3 Приборы и реактивы:
Фотоэлектроколориметр ФЭК–56 (КФК–3) с набором кювет; стандартный раствор сульфата меди с концентрацией 1 г/л; 10% раствор аммиака (NH4OH); мерные колбы объемом 100 мл; градуированная пипетка объемом 10 мл; мерный цилиндр.
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 396; Нарушение авторских прав?; Мы поможем в написании вашей работы!