
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Порядок работы на установке для кулонометрического титрования в амперостатическом режиме
|
|
|
|
1. Испытуемый раствор переносят в мерную колбу объемом 100 см3 и доводят объем до метки дистиллированной водой.
В катодное пространство ячейки помещают 30 см3 раствора фонового электролита и доводят объем раствора до 150 см3 дистиллированной водой.
Заполняют анодную камеру раствором фонового электролита.
Опускают генераторный и индикаторные электроды в катодное пространство, а вспомогательный – в анодное простраство титрационной ячейки и закрепляют таким образом, чтобы все электроды были погружены в раствор на 1 см.
Заполняют соединительный мостик раствором хлорида калия и помещают один его конец в анодную камеру, а другой - в катодное пространство.
Для работы источника постоянного тока в режиме стабилизации тока устанавливают кодовый переключатель выходного тока в положение, соответствующее 2-50 мА, а переключатель напряжения в положение 299В.
На индикаторные электроды подают постоянное напряжение (порядка 0,01В). Фиксируют силу тока в индикаторной цепи.
5.2.3.2. Контрольная задача Определение содержания ионов 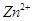 .
.
1. Аликвотную часть испытуемого раствора (например, 10 см3) из бюретки переносят в катодное пространство ячейки и включают мешалку. Записывают значение силы тока в индикаторной цепи в таблицу 13.4.
Данные для определения точки эквивалентности.
Таблица 13.4.
| № точки | Время, сек | Ток в индикаторной цепи, mA |
Одновременно включают секундомер и тумблер ВКЛ источника постоянного тока. Фиксируют с помощью миллиамперметра точное значение тока генерации.
Во время электролиза записывают значения силы тока в индикаторной цепи через каждые 10 секунд.
Строят кривые титрования в координатах 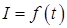 силы тока в индикаторной цепи от времени. Определяют время электролиза до точки эквивалентности.
силы тока в индикаторной цепи от времени. Определяют время электролиза до точки эквивалентности.
|
|
|
Проводят многократное (3-5 раз) титрование различных по объему (от 2 до 5 см3) порций испытуемого раствора. Результаты заносят в таблицу 13.4.
Данные кулонометрического титрования.
Таблица 13.4.
| Объем раствора, см3 | Генерационный ток, мА | Время электролиза, сек | Найдено ионов 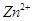 , мг , мг
|
Находят конечную точку титрования и рассчитывают содержание иона цинка в мг в каждой аликвоте по формуле:
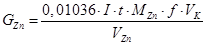
где 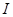 - генерационный ток, А;
- генерационный ток, А;
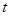 – время генерации, сек;
– время генерации, сек;
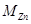 – атомная масса
– атомная масса 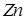 , г/моль;
, г/моль;
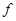 – фактор эквивалентности;
– фактор эквивалентности;
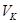 – объем мерной колбы, см 3;
– объем мерной колбы, см 3;
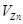 - объем аликвоты испытуемого раствора, см3.
- объем аликвоты испытуемого раствора, см3.
Находят концентрацию иона цинка для каждого опыта и среднее значение концентрации иона цинка в анализируемом растворе.
5.2.4. Определение ионов 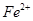 .
.
Потенциометрическое определение ионов 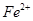 основано на электроокислении в кислых растворах до
основано на электроокислении в кислых растворах до 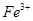 при контролируемом потенциале платинового рабочего электрода (+0,95 В относительно хлорсеребряного электрода сравнения):
при контролируемом потенциале платинового рабочего электрода (+0,95 В относительно хлорсеребряного электрода сравнения):
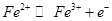 на аноде.
на аноде.
Для определения рабочего потенциала предварительно снимают поляризационные кривые (зависимость ток-потенциал) в растворе фона в отсутствие и в присутствии анализируемого вещества. По поляризационной кривой находят область потенциалов, в которой достигается предельный ток определяемого вещества. Потенциал рабочего электрода выбирают в этой области (в середине площадки предельного тока).
Приборы и реактивы
1. Установка для кулонометрии в потенциостатическом режиме.
Генераторный электрод – пластина из платины размером 1х1 см.
Генераторный электрод – платиновая сетка.
Вспомогательный электрод – стальной стержень.
Хлорсеребряный электрод сравнения.
Магнитная мешалка.
Мерная колба вместимостью 100 см3.
Мерный цилиндр вместимостью 50 см3.
Пипетка вместимостью 2 см3.
|
|
|
Раствор серной кислоты, 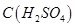 = 1моль/дм3.
= 1моль/дм3.
Cульфат железа (II),  моль/дм3.
моль/дм3.
Ход работы
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 451; Нарушение авторских прав?; Мы поможем в написании вашей работы!