
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Систематические ошибки
|
|
|
|
Проверка показаний лица,признавшегося в совершении насильственного преступления.
[1]См.: Корчагин А.Ю. Организационно‑тактические и методические основы криминалистического обеспечения судебного разбирательства уголовных дел: Автореф. дисс… докт. юрид. наук. – Краснодар, 2008. – С. 20.
Систематические ошибки возникают при пользовании неточными измерительными приборами (неправильно калиброванной измерительной посудой, некалиброванным разновесом, вращающейся измерительной шкалой, имеющей люфт (мертвый ход), эксцентричное положение стрелки прибора, загрязнение реактивов, введение в растворы веществ, выщелачиваемых из стенок посуды: стекла, фарфора и др.).
К систематическим ошибкам относятся субъективные ошибки, вызванные личными особенностями работающего (слабостью зрения, дальтонизмом — отсутствием способности различать цвета) и т. д.
Систематические ошибки не дают больших отклонений в параллельных определениях. Близкое сходство параллельных определений часто рассматривают как показатель высокой точности и правильности анализа. Для выявления систематической ошибки проводят анализ совершенно иным методом, используя другие приборы, другие реактивы, и лучше в другой лаборатории другими аналитиками.
Случайные ошибки
Связаны с различными факторами, не поддающимися учету и устранению. В каждом отдельном случае эти ошибки приводят к различным результатам. Могут иметь разное численное значение и разные знаки.
К случайным ошибкам относятся также грубые ошибки — промахи в цифрах, и отсчетах по шкале прибора, ошибки в вычислениях, при переписывании цифр, перепутывание колб с пробами во время титрования и т. д. Грубые ошибки легко выявляются при повторных анализах по резким отклонениям или сумме анализа, которая будет сильно отличаться от 100%.
|
|
|
Повторяющиеся при параллельных определениях ошибки. Величина их одинакова при всех определениях, проводящихся одним и тем же методом.
2 раздел 1. Титриметрический анализ (титриметрия). Основные понятия (аликвота, титрант, титрование, точка эквивалентности, конечная точка титрования, индикатор, кривая титрования, степень оттитрованноcти, уровень титрования).
Титриметрический (объёмный) анализ является одним из важнейших видов количественного анализа. Его основными достоинствами являются точность, быстрота исполнения и возможность применения для определения самых разнообразных веществ. Определение содержания вещества в титриметрическом анализе осуществляется в результате проведения реакции точно известного количества одного вещества с неизвестным количеством другого, с последующим расчётом количества определяемого вещества по уравнению реакции. Реакция, которая при этом протекает должна быть стехиометрической, т.е. вещества должны реагировать строго количественно, согласно коэффициентам в уравнении. Только при соблюдении этого условия реакция может быть использована для количественного анализа.
Основной операцией титриметрического анализа является титрование – постепенное смешивание веществ до полного окончания реакции. Обычно в титриметрическом анализе используются растворы веществ. В ходе титрования раствор одного вещества постепенно приливается к раствору другого вещества до тех пор, пока вещества полностью не прореагируют. Раствор, который приливают, называется титрантом, раствор, к которому приливается титрант, называется титруемым раствором. Объём титруемого раствора, который подвергается титрованию, называется аликвотной частью или аликвотным объёмом.
|
|
|
Точкой эквивалентности называется момент, наступающий в ходе титрования, когда реагирующие вещества полностью прореагировали. В этот момент они находятся в эквивалентных количествах, т.е. достаточных для полного, без остатка, протекания реакции.
Для титрования применяются растворы с точно известной концентрацией, которые называются стандартными или титрованными.
3 раздел 1. Ацидиметрия. Титрование сильного основания. Расчет рН в различных точках титрования. Кривая титрования. Индикаторы метода. Примеры. Реакции.
В основе кислотно-основного титрования лежит реакция нейтрализации между кислотой и основанием. В результате реакции нейтрализации образуется соль и вода.
HAn + KtOH ® KtAn + H2O
Реакция нейтрализации протекает при комнатной температуре практически мгновенно. Кислотно-основное титрование применяется для определения кислот, оснований, а также многих солей слабых кислот: карбонатов, боратов, сульфитов, и т. д. При помощи данного метода можно титровать смеси различных кислот или оснований, определяя содержание каждого компонента в отдельности.
При титровании кислоты основанием или наоборот, происходит постепенное изменение кислотности среды, которое выражается водородным показателем рН. Вода представляет собой слабый электролит, который диссоциирует согласно уравнению.
Н2О ® Н+ + ОН-
Произведение концентрации ионов водорода на концентрацию ионов гидроксила есть величина постоянная, и называется ионное произведение воды.

 (1)
(1)
В нейтральной среде концентрации водородных ионов и гидроксид-ионов равны и составляют 10-7м/л. Ионное произведение воды остаётся постоянным при добавлении в воду кислоты или основания. При добавлении кислоты увеличивается концентрация ионов водорода, что приводит к сдвигу равновесия диссоциации воды влево, в результате чего концентрация гидроксид-ионов уменьшается. Например, если [H+] = 10-3м./л., то [OH-] = 10-11м./л. Ионное произведение воды останется постоянным.
10-3 10-11 = 10-14.
Если увеличить концентрацию щёлочи, то концентрация гидроксид-ионов увеличится, а концентрация ионов водорода уменьшится, ионное произведение воды также останется постоянным. Например, [OH-] = 10-2, [H+] = 10-12
10-12 10-2 = 10-14.
|
|
|
Водородным показателем рН называется отрицательный десятичный логарифм концентрации ионов водорода.
рН = - lg [H+]. (2)
Исходя из уравнения (1) можно заключить, что в нейтральной среде рН = 7.
pН = - lg 10-7 = 7.
В кислой среде рН < 7, в щелочной рН > 7. Аналогично выводится формула для рОН из уравнения (1).
pОН = - lg [OH-] = 14 – pH. (3)
В ходе кислотно-основного титрования с каждой порцией приливаемого титранта изменяется рН раствора. В точке эквивалентности рН достигает определённого значения. В этот момент времени титрование необходимо прекратить и измерить объём титранта, пошедший на титрование. Для определения рН в точке эквивалентности строят кривую титрования – график зависимости рН раствора от объёма прибавляемого титранта. Кривую титрования можно построить экспериментально, измеряя рН в различные моменты титрования, или рассчитать теоретически, используя формулы (2) или (3). Для примера рассмотрим титрование сильной кислоты HCl сильным основанием NaOH.
Таблица 1. Титрование 100мл 0,1М раствора HCl 0,1М раствором NaOH.
| VNaOH (мл) | nNaOH (моль) | nHCl (моль) вступившее в реакцию. | nHCl остающееся в растворе (моль) | CHCl | рH |
| 50,0 | 5,00 10-3 | 5,00 10-3 | 0,05 | 0.0500 | 1.3 |
| 90,0 | 9,00 10-3 | 9,00 10-3 | 1 10-2 | 0.0100 | 2.0 |
| 99,0 | 9,90 10-3 | 9,90 10-3 | 1 10-3 | 0.0010 | 3.0 |
| 99,9 | 9,99 10-3 | 9,99 10-3 | 1 10-4 | 0.0001 | 4.0 |
| 100,0 | 1,00 10-2 | 1,00 10-2 | 7.0 | ||
| 101,0 | 1,01 10-2 | 1,01 10-2 | |||
| 1,10 ×10-2 | 1,10 ×10-2 |
По мере прибавления щёлочи к раствору кислоты, происходит уменьшение количества кислоты и рН раствора увеличивается. В точке эквивалентности кислота полностью нейтрализована щёлочью и рН = 7. Реакция раствора нейтральная. При дальнейшем добавлении щёлочи рН раствора определяется избыточным количеством NaOH. При добавлении 101 и 110мл. раствора NaOH избыток щёлочи составляет соответственно 1 и 10 мл. Kоличество NaOH в этих двух точках, исходя из формулы молярной концентрации раствора равно соответственно 0.1 10-3 моль и 1 10-3моль
Исходя из формулы (3) для титруемого раствора с избытком щёлочи 1 и 10 мл. имеем значения рН соответственно 10 и 11. По рассчитанным значениям рН строим кривую титрования.
|
|
|
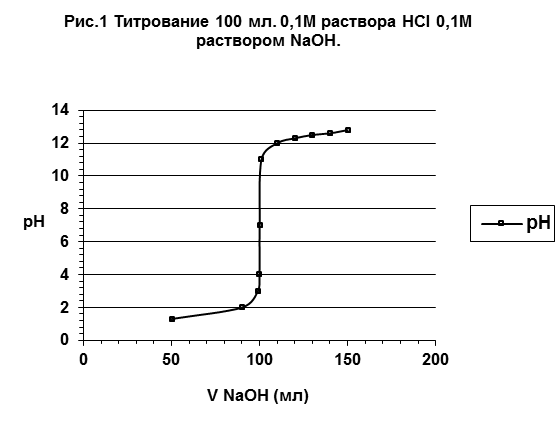
По кривой титрования видно, что в начале титрования рН раствора определяется присутствием в растворе соляной кислоты и слабо изменяется при добавлении раствора щёлочи. Вблизи точки эквивалентности происходит резкий скачок рН при добавлении очень малого количества щёлочи. В точке эквивалентности в растворе присутствует только соль и вода. Соль сильного основания и сильной кислоты гидролизу не подвергается и поэтому реакция раствора нейтральная рН = 7. Дальнейшее прибавление щёлочи приводит к увеличению рН раствора, которое также незначительно изменяется от объёма приливаемого титранта, как и в начале титрования. В случае титрования сильных кислот сильными основаниями и наоборот, точка эквивалентности совпадает с точкой нейтральности раствора.
4 раздел 4. Перманганатометрическое титрование. Сущность метода. Условия проведения титрования. Титрант. Установление конечной точки титрования. Реакции. Расчеты результатов титрования.
В данном методе окислительно-восстановительного титрования окислителем служит перманганат калия KMnO4. Перманганат калия сильный окислитель. Он способен вступать в реакции в кислой, нейтральной и щелочной средах. о различных средах окислительная способность перманганата калия неодинакова. Наиболее сильно она выражена в кислой среде.
MnO4- + 8H+ +5e ® Mn+ + 4H2O
MnO4- + 2H2O + 3e ® MnO2¯ + 4OH-
MnO4- + e ® MnO42-
Перманганатометрическим методом можно определять самые разнообразные вещества: Fe2+, Cr2+, Mn2+, Cl-, Br-, SO32-, S2O32-, NO2,- Fe3+, Ce4+, Cr2O72+, MnO2, NO3-, ClO3-.и т. д. Многие органические вещества: фенолы, аминосахара, альдегиды, щавелевую кислоту и т. д.
Перманганатометрия имеет много достоинств.
1. Перманганат калия является дешёвым и легкодоступным веществом.
2. Растворы перманганата окрашены в малиновый цвет, поэтому точку эквивалентности можно установить без применения индикаторов.
3. Перманганат калия сильный окислитель и поэтому пригоден для определения многих веществ, которые не окисляются другими окислителями.
4. Титрование перманганатом можно проводить при различной реакции среды.
Перманганатометрия имеет и некоторые недостатки.
1. Перманганат калия трудно получить в химически чистом виде. Поэтому приготовить стандартный раствор по точной навеске вещества затруднительно. Для титрования используют вторичные стандарты перманганата, концентрация которых устанавливается по стандартным растворам других веществ: (NH4)2C2O4, K4[Fe(CN)6], H2C2O4 и др. которые называются установочными веществами.
2. Растворы перманганата неустойчивы и при длительном хранении меняют свою концентрацию, которую необходимо периодически проверять по растворам установочных веществ.
3. Окисление перманганатом многих веществ при комнатной температуре протекает медленно и для проведения реакции требуется нагревание раствора.
6 раздел 5. Тиоцианатометрическое титрование. Сущность метода. Титрант метода, его приготовление, стандартизация. Индикатор метода. Расчеты результатов титрования.
Тиоцианометрическое титрование (роданометрическое), титрант –
раствор NН4CNS.
Роданометрическим методом титрования пользуются для определения галогенид-ионов и ионов серебра. Для определения катионов Аg+ в качестве
стандартного раствора используют роданид (тиоцианат) аммония, для определения галогенидов и других анионов – нитрат серебра и роданид аммония.
В качестве индикатора применяют насыщенный раствор железоаммонийных
квасцов.
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 688; Нарушение авторских прав?; Мы поможем в написании вашей работы!