
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение состава получаемого газа
|
|
|
|
Пример технологического расчета процесса газификации кокса
Газификация по методу Winkler проводится под давлением 0,2 МПа, так как повышение давления приводит к увеличению в газе количества метана и диоксида углерода и снижению выхода водорода и оксида углерода. Расчет выполняется исходя из производительности установки, равной 363000 т кокса заданного состава в год. Число дней работы в году – 330.
Для газификации кокса принимаются параметры процесса:
- температура процесса газификации 950°С;
- температура подаваемого кислорода 250°С;
- температура перегретого водяного пара 500°С;
- состав дутья: 98% кислорода и 2% азота;
- соотношение пар: кокс 1,0;
- выход золы 2 % масс от количества кокса;
- содержание метана в получаемом газе 0,2 % об.
Температура в газогенераторе не должна превышать 1000°С, так как при высокой температуре происходит спекание золы.
Исходные данные по составу кокса приведены в таблице 7.1.
Таблица 7.1 – Элементарный состав кокса
| Состав кокса | вес. % | моль/100 кг | м3/363000000 кг |
| С | 90,5 | 7,5417 | |
| Н | 5,3 | 2,6500 | |
| S | 2,8 | 0,0875 | |
| N | 0,5 | 0,0179 | |
| О | 0,9 | 0,0281 | |
| Всего | 100,0 | 10,3251 |
Низшая теплота сгорания кокса определяется по формуле Д. И. Менделеева
Qн = 81 · С + 246 · Н – 26 · (О - S) – 6 · W, (7.1)
где С, Н, О, S, W – содержание в топливе соответствующих элементов и влаги, %.
Qн = 81 ∙ 90,5 + 246 ∙ 5,3 – 26 ∙ (0,9 – 2,8) – 6 · 0 = 8683,7 ккал/кг;
Qн = 8683,7 · 4,187 = 36358,7 кДж/кг.
Для составления системы уравнений принимаются следующие обозначения:
а, b, h - соответственно количество СО2, СО и Н2 в получаемом газе, тыс. м3;
w – количество прореагировавшего водяного пара, тыс. м3;
V – объем получаемого сухого газа, тыс. м3;
x – расход технического кислорода, тыс. м3.
|
|
|
Тогда получаемый сухой газ будет иметь состав, приведенный в таблице 7.2.
Составляется система из шести уравнений, включающая шесть принятых неизвестных: a, b, h, w, V, x.
Таблица 7.2 – Состав получаемого сухого газа
| Компонент газа | Количество, тыс. м3 |
| СО2 | а |
| СО | b |
| Н2 | h |
| СН4 | 0,002V |
| N2 | 0,02x + 1452,0 |
| Н2S | 7114,8·1=7114,8 |
1) Уравнение баланса углерода.
Количество золы, выделяющейся при газификации 363000 т кокса, равно
0,02·363000 = 7260 т;
 тыс. м3.
тыс. м3.
Тогда уравнение баланса углерода будет
613228,0 = a + b + 0,002V + 13552,0; (7.2)
599676,0 = a + b + 0,002V. (7.3)
2) Уравнение баланса водорода.
Расход водяного пара при газификации 363000 т кокса равен
1,0 · 363000 = 363000 т;
w1 = 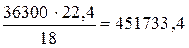 тыс. м3.
тыс. м3.
Получается следующее уравнение баланса водорода:
215476,8 + 451733,4 = h + 2·0,002V + (451733,4– w) +7114,8; (7.4)
208362,0 = h + 0,004V – w. (7.5)
3) Уравнение баланса кислорода:
0,98х + 0,5·451733,4 + 2286,9 = а + 0,5b + 0,5·(451733,4 – w); (7.6)
2286,9 = а + 0,5b – 0,5w – 0,98х. (7.7)
4) Уравнение суммы компонентов сухого газа:
V = a + b + h + 0,002V + 0,02 x + 9545,827. (7.8)
5) Уравнение равновесия реакции водяного газа:
СО + Н2О = СО2 + Н2; (7.9)
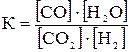 ; (7.10)
; (7.10)
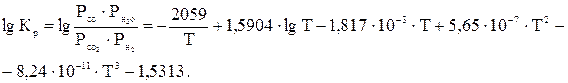 (7.11)
(7.11)
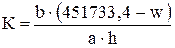 = 1,47. (7.12)
= 1,47. (7.12)
|
|
|
|
|
Дата добавления: 2015-06-27; Просмотров: 814; Нарушение авторских прав?; Мы поможем в написании вашей работы!