
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Формула М.Г. Курлова
Классификация О.А. Алекина
Химическая классификация природных вод
Содержание растворенных газов, температура, дебит
Минерализация воды
Определение состава природных вод
2.2.1 Жёсткость воды
Жёсткость воды определяется содержанием растворённых солей, кальция и магния. Различают общую, устранимую и постоянную жёсткости воды. Общая жёсткость обусловлена суммарным содержанием ионов Ca2+ и Mg2+, устранимая представляет собой ту часть жёсткости, которая вызывается бикарбонатами Ca2+ и Mg2+ и устраняется кипячением воды, постоянная равно общей жёсткости минус устранимая. Общая жёсткость принято выражать в миллиграмм – моль (эквивалент) на дм3 (ммоль/дм3) и в немецких градусах (оН). Миллиграмм – моль жёсткости соответствует раздельному содержанию в дм3 воды эквивалентных количеств Ca2+, Mg2+ и CaО, а именно 20,04 мг Ca2+ , 12,16 мг Mg2+ или 28 мг CaО. Немецкий градус жесткости эквиваленте содержанию 10 мг CaО в литре воды. Сопоставляя названные показатели жесткости по величине CaО устанавливаем, что один ммоль жесткости равен 2,8 немецких градусов.
Значение общей жесткости воды в ммоль/дм3 находится суммированием содержания иона Ca2+ и Mg2+ в молярной форме. Умножая полученную величину на 2,8 находим общую жесткость в немецких градусах.
Минерализация воды определяется содержанием растворенных минеральных веществ и рассчитывается как арифметическая сумма весовых количеств всех ионов в дм3 воды. При подсчете минерализации суммарное содержание ионов, выраженное в миллиграммах на дм3 переводится в граммы, с округлением до первого знака после запятой.
Пример: сумма ионов составляет 14176 миллиграмм, минерализация воды 14,2 г/ дм3.
Полный химический анализ воды предусматривает определение растворенных газов (СО2, Н2S и др.) содержание которых выражается миллиграммами на дм3 (мг/ дм3). При полевых исследованиях устанавливается температура природных вод (Т) и определяется дебит источников или скважин путем замера вытекающей или откачиваемой из них воды.
Дебит (Д) выражается литрами в секунду (л/с) или кубометрами в сутки (м3/сутки).
Классификация О.А. Алекина (рисунок 8) сочетает принцип деления подземных вод по преобладающим ионам и по соотношению между ними. По преобладающему аниону О.А. Алекиным /4/ выделяются три класса вод: гидрокарбонатная, сульфатная и хлоридная. По ведущему катиону различают группы кальциевых, магниевых и натриевых вод. Соотношение ионов позволяет установить различные типы вод. При выделении которых содержание ионов выражается в молярной форме (r)
1тип r 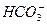 > r Ca2+ + r Mg2+ (гидрокарбонатный натриевый),
> r Ca2+ + r Mg2+ (гидрокарбонатный натриевый),
2тип r 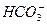 < r Ca2+ + r Mg2+ (сульфатный натриевый),
< r Ca2+ + r Mg2+ (сульфатный натриевый),
3тип r 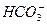 +
+ 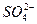 < r Ca2+ + r Mg2+ или r Сl- >r Na+
< r Ca2+ + r Mg2+ или r Сl- >r Na+
4тип r 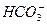 +
+ 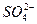 =0
=0
3 тип подразделяется: 3а rCl- < r Na++ r Mg2+ (хлормагниевый),
3б rCl- < r Na++ r Mg2+(хлоркальциевый).
|

|

|
|


 |  |  |  |  |  |  |  |  | |||||||||
|
|
|
|
|
|
|
|
|
Типы гидрокарбонатных: Ca - I,II,III; Mg – I,II,III; Na – I,II,III
Типы сульфатных: Ca - IV,II,III; Mg – IV,II,III; Na – I,II,III
Типы хлоридных: Ca - IV,II,III; Mg – IV,II,III; Na – I,II,III
Рисунок 8 Классификация природных вод по О.А. Алекину
Эти гидрохимические оценки можно записать и в более сжатой форме. Если классы вод обозначить условными индексами (С-гидрокарбонатные воды, S-сульфатные, Cl-хлоридные), а типы римскими выделить символами ведущих катионов (Ca,Mg, Na), а типы римскими цифрами (I-IV), то химическая характеристика вод указанного состава запишется так: 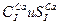 .
.
Эту краткую форму записи следует использовать, указывая класс воды по Алекину в таблице результатов химических анализов природных вод (таблица 5).
При массовых определениях химического состава природных вод возникает необходимость обобщения, полученных результатов и изображения анализов воды в виде кратких формул, допускающих обзор и интерпретацию аналитического материала. Формула Курлова представляет собой псевдо-дробь, в числителе которой в порядке убывающего содержания записываются анионы, а в знаменателе катионы, выраженные в процентах (дробные величины процентов округляются до целых чисел). Слева от полученной «простой дроби» указывается содержание растворенных газов в мг/ дм3 и величина минерализации воды в г/ дм3, справа от нее температура воды и дебит скважины в м3 /сутки. Образец записи результатов анализа в виде формулы Курлова приводится ниже:
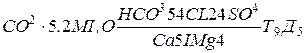 .
.
Наименование водам дается по преобладающим (свыше 20% моль) анионам и катионам в порядке их возрастания (приведенный анализ читается – вода сульфатно-хлоридно-карбонатная, магниево-кальциевая).
2.3.3 Пересчет из ионной формы в солевую производится по правилу фрезенуса в соответствии с растворимостью солей. В первую очередь комбинируются малорастворимые, а затем более растворимые. Общая схема связывания следующая. Ионы Ca2+ связываются последовательно с 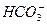 ,
, 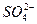 , Cl в зависимости от его содержания в процентах. В такой же последовательности связываются ионы Mg2+ и Na+. Пересчет в солевую форму имеет важное значение при оценке питьевых, лечебных, технических и др. качеств воды, т.к. полезно принять во внимание не только абсолютное содержание ионов но и предполагаемые ассоциации анионов с катионами (соли).
, Cl в зависимости от его содержания в процентах. В такой же последовательности связываются ионы Mg2+ и Na+. Пересчет в солевую форму имеет важное значение при оценке питьевых, лечебных, технических и др. качеств воды, т.к. полезно принять во внимание не только абсолютное содержание ионов но и предполагаемые ассоциации анионов с катионами (соли).
|
|
Дата добавления: 2015-06-27; Просмотров: 6271; Нарушение авторских прав?; Мы поможем в написании вашей работы!