
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пределы обнаружения (ПО) некоторых неметаллов в воде
|
|
|
|
| Элемент (линия, нм) | ПО, (мкг/л) | ПДК в питьевой воде, (мкг/л) |
| Br (163,340) | ||
| Cl (134,724) | 25 000 | |
| I (161,761) | ||
| P (178,290) | 3,9 | |
| S (182,037) | 6,5 | 8 300 |
| S (180,734) | 3,5 | 8 300 |
Принцип масс-спектроскопии заключается в следующем. Тем или иным способом проводится ионизация пробы, после чего в вакууме из образовавшихся ионов формируется направленный пучок, который в магнитном и электрическом полях разделяется по массам (точнее, по отношению массы иона m к его заряду е).
Ионизация вещества проводится тремя основными способами. Наиболее распространено использование электрического искрового разряда. В этом способе из пробы изготавливают электроды, которые устанавливают в камере с зазором 0,05–0,5 мм и подают на них мощный электрический импульс. При этом происходит пробой зазора (образование искры), частично разрушающий, испаряющий и ионизирующий материал электродов, то есть пробу. Этот способ получил название искровой масс-спектрометрии. Пригоден он, в основном, для исследования проводящих материалов.
Ионизация любых светопоглощающих твердых проб, в том числе непроводящих, может осуществляться лазерным пучком. Используется для этого, как правило, импульсный твердотельный лазер. Этот способ называется лазерной масс-спектрометрией.
Еще один вариант – масс-спектрометрия вторичных ионов – используется при изучении свойств поверхности.
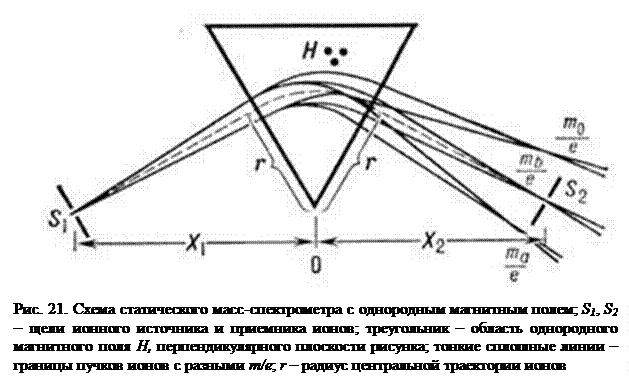
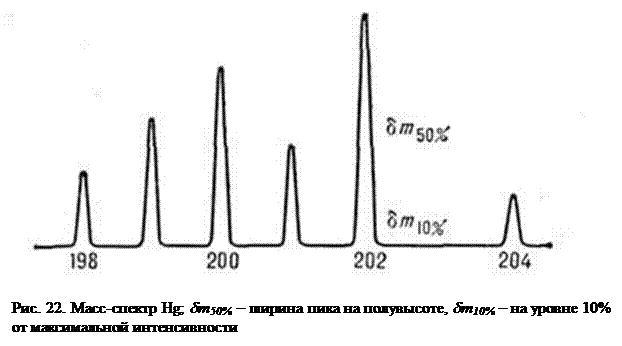
В масс-спектрографах пучки ионов с разными m/e фокусируются в разных местах фотопластинки, расположенной в фокальной плоскости прибора, образуя после проявления следы в виде полосок (выходное отверстие ионного источника обычно имеет форму прямоугольника – щели). В статическом масс-спектрометре (рис. 21) пучок ионов с заданным m/e фокусируется на щель приемника ионов. При плавном изменении магнитного или электрического полей в приемную щель последовательно попадают пучки ионов с разными m/e. При непрерывной записи ионного тока получается график с ионными пиками масс-спектра (рис. 22).
|
|
|
В статическом масс-спектрометре с однородным магнитным полем H ионы, образованные в источнике, выходят из щели шириной S1 в виде расходящегося пучка, который в магнитном поле разделяется на пучки ионов с разными m/e (mа/e, mb/e, m0/e). Пучок ионов с массой mb фокусируется на щель шириной S 2 приемника ионов. Величина mb/e определяется выражением:
mb/e = 4,824´10 –5H2r2/V
где mb – масса иона в а. е. м.; е – его заряд в единицах элементарного электрического заряда; r – радиус центр, траектории в см; V – ускоряющий потенциал в В; H – напряженность магнитного поля в Э. Развертка масс-спектра производится изменением H или V. Первый метод предпочтительнее, так как в этом случае по ходу развертки не изменяются условия «вытягивания» ионов из источника.
Разрешающая способность статического масс-спектрометра определяется из соотношения:
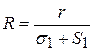
где s 1 – ширина пучка в месте, где он попадает в щель приемника S2.
Если бы фокусировка ионов была идеальной, то в случае X1=X2 (см. рис. 21) s 1 была бы в точности равна S1. В действительности s 1 > S1, что уменьшает разрешающую способность масс-спектрометра. Одна из причин уширения пучка – неизбежный разброс по кинетической энергии у ионов, вылетающих из источника. Другие причины – рассеяние ионов из-за столкновений с молекулами остаточного газа, а также электростатическое «расталкивание» ионов в пучке. Для уменьшения рассеяния ионов стремятся к созданию высокого вакуума (давление p ~10–6 Па»10 –8 мм.рт.ст) на всем пути ионов от источника до коллектора.
Регистрируемый с помощью масс-спектрометра масс-спектр представляет собой зависимость ионного тока от массы т (точнее, от m/e). Например, в масс-спектре Hg каждый из пиков ионного тока соответствует однозарядным ионам изотопов ртути (рис. 22). Высота пика пропорциональна содержанию данного изотопа.
|
|
|
Изотопы – химические элементы, расположенные в одной и той же клетке периодической системы и, следовательно, обладающие одинаковым атомным номером или порядковым числом. При этом изотопы не должны обладать одинаковым атомным весом. Различные изотопы одного элемента обладают одинаковыми электронными оболочками и всеми свойствами, связанными с электронной оболочкой Изотопы различаются только строением ядра, а именно числом входящих в него положительных элементов, протонов, от которых зависит масса атома.
Считается, что масс-спектроскопия с R £102 имеет низкую разрешающую способность, с R ~102–103 – среднюю, с R ~103–104 – высокую, с R ~105 – очень высокую.
Масс-спектральный анализ позволяет наиболее полно решить задачу определения всех возможных примесей в материале. В одном эксперименте можно зарегистрировать все элементы Периодической системы и даже провести изотопный анализ. Таким образом, масс-спектральный метод характеризуется более высокой селективностью, чем другие способы исследования химического состава вещества. На полный масс-спектральный анализ расходуется обычно не более 10 мг вещества. Случайная погрешность анализа варьируется от 1 до 10%.
В основе рентгеноспектроскопии элементного состава материалов лежит изучение рентгеновских характеристических спектров веществ.
Схему процесса можно представить следующим образом. При облучении вещества (например, жестким рентгеновским излучением, электронами, ионами или g-излучением) возможна ионизация атома за счет удаления электрона с ближних к ядру уровней. Через небольшой промежуток времени ионизированный атом релаксирует из возбужденного состояния, а избыточная энергия выделяется в виде рентгеновского кванта. В результате электронных переходов, заполняющих вакансии, образуется рентгеновский спектр. Полученный таким образом спектр называется характеристическим, поскольку каждому переходу соответствует вполне определенная, характерная только для этого элемента энергия.
|
|
|
Если возбуждение характеристического рентгеновского излучения в образце осуществляется первичным рентгеновским излучением, то данный способ называется рентгенофлюоресцентным анализом.
В рентгенорадиометрическом анализе возбуждение осуществляется g-излучением от радиоактивного изотопа.
Возбуждение сфокусированным пучком электронов с энергией в десятки кэВ применяется в электроннозондовом рентгеноспектральном микроанализе.
И, наконец, возбуждение тяжелыми ионами с энергиями до единиц МэВ используется в рентгеноспектральном анализе с ионным возбуждением.
Независимо от способа генерации характеристического рентгеновского излучения, все эти методы идентичны. В то же время наблюдается различие по пределам обнаружения элементов, определяемым соотношением полезного сигнала и фона.
Рентгеноспектроскопия позволяет проводить количественную оценку большого числа элементов. Однако ее применение ограничено при определении элементов с атомными номерами меньше, чем Mg (z = 12). Для определения элементов более легких, чем фтор (z = 9), метод практически не используется из-за низкого уровня возбуждения их характеристического излучения и сильного его поглощения. Анализируемые пробы могут представлять собой пленки, порошки, массивные образцы, жидкости. Какие-либо изменения в пробах в ходе рентгеноспектрального анализа ничтожны, в связи с чем он является методом неразрушающего контроля.
В основе активационного анализа лежит измерение радиоактивного излучения, возбуждаемого в пробах путем бомбардировки их высокоэнергетическими частицами (нейтронами, протонами) или g-квантами.
Можно представить следующую схему процесса. В результате бомбардировки атомов анализируемого вещества нейтронами или протонами происходят различные ядерные реакции. В частности, частицы могут захватываться ядрами атомов, вследствие чего образуются новые, как правило, нестабильные самопроизвольно распадающиеся ядра. Синтезированные радиоактивные изотопы имеют, чаще всего, сильно различающиеся значения периода полураспада. Измерение этой постоянной, а также учет вида распада и энергии излучения дают возможность идентифицировать большинство элементов.
|
|
|
Активационный анализ является одним из наиболее чувствительных методов. Для него характерна экспрессность, универсальность, высокая селективность. С помощью этого метода возможен анализ металлов высокой чистоты, определение содержания в материале редких и рассеянных элементов.
Все физические методы анализа элементного состава, описанные выше, являются экспрессными, что позволяет использовать их для контроля технологических процессов производства и аттестации нанопродукции.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 360; Нарушение авторских прав?; Мы поможем в написании вашей работы!