
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Механизмы ишемии и реперфузионных повреждений
Особенности архитектуры микроциркуляторного русла ворсинок кишечника делают их особенно восприимчивыми к гипоксии [8]. Каждая ворсинка снабжается через одну единственную центральную артерию, которая окружена "плащом" субэпителиальных ве-нул и капилляров, отводящих кровь от вершины ворсинки. Небольшое расстояние между этими сосудами и наличие противотока в них приводит к шунтированию кислорода в микроциркуляторном русле, особенно при снижении скорости кровотока, возникающем при геморрагическом, кардиогенном и септическом шоке [2,8,13,14]. Перфузия в желудочно-кишечном тракте может в последующем снижаться под воздействием ренин-ангиотензиновой системы, вызывающей вазоконстрикцию во внутренних органах [5,15,16].
Метаболические последствия ишемии проявляются прогрессивным сокращением продукции аденозинтрифосфата (АТФ) несмотря на постоянное использование этого энергоемкого фосфата. Для поддержки внутриклеточного уровня АТФ происходит активизация анаэробного гликолиза, что приводит к развитию внутриклеточного ацидоза. Энергоемкие фосфаты деградируют до аденозина, который после быстрой диффузии в интерстициальное пространство метаболизируется до инозина и гипоксантина, где становится главным источником реактивных метаболитов кислорода [11]. В экспериментальной модели на животных с неокклюзионной ишемией кишечника двухчасовой период ишемии снижал концентрацию АТФ на 40% с последующим увеличением концентрации аденозина монофосфата и гипоксантина в ткани кишечника [7].
Реперфузия ишемизированного кишечника приводит к генерированию токсичных свободных радикалов кислорода в результате взаимодействия молекулярного кислорода с гипоксантином и ксантином, возникающими в результате деградации пуринов [11,18]. Эти реактивные метаболиты кислорода вызывают повреждения, известные как реперфу-зионные повреждения [18-20]. Более того, полиморфноклеточные нейтрофилы сами по себе генерируют реактивные кислородные метаболиты и напрямую взаимодействуют с эндотелиальными клетками сосудов, что ведет к микроциркуляторным нарушениям кишечника и затем к утрате барьерной функции по отношению к интралюминальным токсическим бактериальным продуктам [5,19].
В нормальных условиях ксантин-дегидрогеназа (XDH) является ферментом, ответственным за деградацию гипоксантина до мочевой кислоты, т.е. за последний этап метаболизма пуринов. В неишемизированных клетках XDH использует никотинамид-аденин-динуклеотид (NAD+) вместо молекулярного кислорода в качестве акцептора электронов в реакции преобразования NAD+ в NADH. В состоянии ишемии тканей ксантин-дегидрогеназа конвертируется в реактивные метаболиты кислорода с образованием ксантин оксидазы (ХО) [12,21]. Два различных пути корверсии в ксантин оксидазу (обратимая оксидация или необратимый протеолизис) реализуются по-разному в различных тканях, хотя объем конверсии пропорционален продолжительности ишемии [21].
При ишемии наблюдается накопление гипоксантинов, которое происходит в результате деградации пуринов, а также метаболизирования их ксантин-оксидазой. При реперфузии кишечника также включаются другие субстраты ферментов (молекулярный кислород) и ХО деградирует гипоксантин до мочевой кислоты [17]. После восстановления кровотока электроны переносятся не к NAD+, а к молекулярному кислороду. В результате происходит формирование супероксидных радикадов (02-) или перекиси водорода Н2О2- Присутствие этих двух реактивных кислородных метаболитов характерно и для физиологических условий, однако здесь они контролируются внутриклеточными антиоксидантными механизмами, такими как супероксид-дисмутаза и каталаза (Табл. 1).
При ишемии образование большого количества супероксида кислорода и перекиси водорода делает данный защитный механизм неэффективным. Кроме всего прочего эти два радикала являются предшественниками гидроксильных радикалов (НО), которые являются самыми окисляющими агентами и, вероятно, несут основную ответственность за развитие клеточных повреждений при реперфузии [12,18,20]. Образование гидроксильных радикалов посредством реакции Haber-Weiss также встречается в физиологических условиях, но весьма незначительно. При реперфузии данная реакция ускоряется благодаря присутствию ионов переходных металлов железа и меди, которые высвобождаются при ишемии и содержат непарные электроны, действующие в качестве матрицы для формирования гидроксильных радикалов [18,22].
В данной схеме супероксидные радикалы редуцируют перекись водорода до радикалов водорода. Наблюдения, свидетельствующие о том, что сильнодействующий реагент хелатного железа десферроксамин прерывает образование гидроксильных радикалов, наглядно демонстрируют роль железа в возникновении реперфузионных осложнений.
Другим метаболитом кислорода, образующимся в результате реакции окиси азота (NO) и супероксида, является пероксинитрит (ONOO-). Окись азота, извлекаемая из эндотелия сосудов, которая обладает сосудорасширяющим, антиадгезивным и антитром-бообразующим действиями и активизируется супероксидом, в данном случае выступает ' в роли защитника против реперфузионных повреждений [12,23].
Ингибиторы ксантин-оксидазы аллопуринол, оксипуринол и птерина альдегид также, уменьшают степень повреждения в ишемизированном кишечнике [12,24,25].
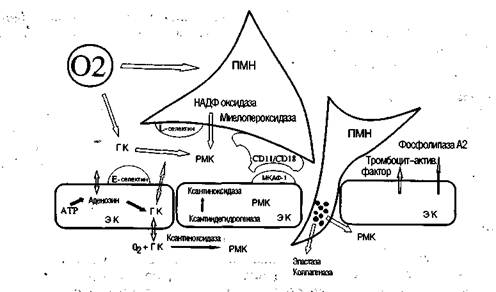
Рис. 1. Реакция между полиморфноклеточными нейтрофилами (ПМН) и эндотелиальными клетками (НЭ) играет существенную роль в ишемическом/ реперфузионном повреждении. РМК-реактивные метаболиты кислорода, МКАФ-1=межклеточные адгезивные молекулы 1, ГК=гипоксантины, CD-11/CD-18-лейкоцитарные адгезивные гликопротеины.
Дата добавления: 2014-01-03; Просмотров: 375; Нарушение авторских прав?; Мы поможем в написании вашей работы!