
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внутренняя энергия реального газа
Тема №6
Свойства реальных газов
Между молекулами реальных газов действуют как силы взаимного притяжения, так и силы отталкивания. При весьма малых расстояниях превалируют силы отталкивания, с увеличением расстояний начинают преобладать силы притяжения. Поэтому молекулы реального газа обладают потенциальной энергией, величина которой закономерно изменяется в зависимости от расстояния между ними.
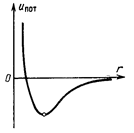 Характер этой закономерности виден из рис. 6.1, на котором показана кривая зависимости потенциальной энергии двух молекул реального газа от расстояния между ними.
Характер этой закономерности виден из рис. 6.1, на котором показана кривая зависимости потенциальной энергии двух молекул реального газа от расстояния между ними.
 Если, преодолевая действие сил отталкивания, сильно сблизить молекулы, то они приобретут потенциальную энергию, весьма существенную по величине, поскольку силы отталкивания очень значительны. При таком положении молекул их энергию можно уподобить потенциальной энергии сжатой пружины. С увеличением расстояния между молекулами сила отталкивания уменьшается, а вместе с ней убывает и их потенциальная энергия, достигая минимального значения в тот момент, когда силы отталкивания и притяжения взаимно компенсируются. После этого потенциальная энергия молекул начинает возрастать, поскольку, пройдя через нулевое значение, результирующая сила взаимодействия меняет направление, превращаясь в силу притяжения. Вместе с тем по абсолютной величине потенциальная энергия уменьшается и уже на расстоянии примерно 10-7 см становится близкой к нулю. Это означает, что минимальное значение потенциальной энергии отрицательно, как и показано на рисунке.
Если, преодолевая действие сил отталкивания, сильно сблизить молекулы, то они приобретут потенциальную энергию, весьма существенную по величине, поскольку силы отталкивания очень значительны. При таком положении молекул их энергию можно уподобить потенциальной энергии сжатой пружины. С увеличением расстояния между молекулами сила отталкивания уменьшается, а вместе с ней убывает и их потенциальная энергия, достигая минимального значения в тот момент, когда силы отталкивания и притяжения взаимно компенсируются. После этого потенциальная энергия молекул начинает возрастать, поскольку, пройдя через нулевое значение, результирующая сила взаимодействия меняет направление, превращаясь в силу притяжения. Вместе с тем по абсолютной величине потенциальная энергия уменьшается и уже на расстоянии примерно 10-7 см становится близкой к нулю. Это означает, что минимальное значение потенциальной энергии отрицательно, как и показано на рисунке.
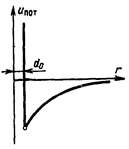
Характер рассмотренной кривой показывает, что без большой погрешности левую ветвь ее, соответствующую области действия силы отталкивания, можно заменить вертикальной прямой, расположенной на расстоянии d0 от оси ординат (рис. 6.2). Это означает, что силу отталкивания можно считать бесконечно большой, а сами молекулы – твердыми упругими шариками с диаметром d0. Иначе это же самое можно представить так, что каждая молекула окружена упругой сферической оболочкой, недоступной для проникновения в нее других молекул (а также и сферических оболочек, окружающих эти молекулы).

Значение потенциальной энергии взаимодействия всех молекул, содержащихся в 1 кг реального газа, можно получить, разбив все молекулы на пары и сложив потенциальные энергии парных взаимодействий всех возможных пар. Очевидно, что это значение зависит от среднего расстояния между молекулами и, следовательно, от удельного объема газа. Таким образом, в противоположность внутренней энергии идеального газа, которая не зависит от объема, у реального газа внутренняя энергия является функцией удельного объема, а, следовательно, и давления.
При не очень малых объемах, или, что тоже, не очень больших давлениях, когда средние расстояния между молекулами сравнительно велики и преобладают силы притяжения, внутренняя потенциальная энергия отрицательна и с увеличением удельного объема возрастает (т.е. по абсолютной величине уменьшается). В первом приближении ее можно выразить формулой
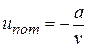 , (6.1)
, (6.1)
где а – некоторая характерная для каждого газа положительная величина, слабо зависящая от Т.
Соответственно этому внутренняя энергия реального газа может быть определена по формуле
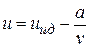 , (6.2)
, (6.2)
где uид – внутренняя энергия соответствующего идеального газа при той же температуре.
|
Дата добавления: 2014-01-03; Просмотров: 385; Нарушение авторских прав?; Мы поможем в написании вашей работы!