
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термические коэффициенты
|
|
|
|
Как и у идеального газа, каждый из основных параметров р,J и Т, являясь функцией состояния реального газа, определяется значениями двух других параметров и может быть найден из уравнения
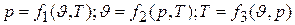 ,
,
которые являются различными формами уравнения состояния.
Таким образом, два любых параметра могут быть приняты за независимые переменные, определяющие значение третьего параметра, а следовательно, и всех других термодинамических величин, являющихся функциями состояния газа.
При этих условиях выше приведенные уравнения состояния в дифференциальной форме будут иметь вид
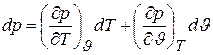 , (6.4)
, (6.4)
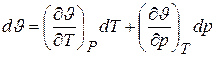 , (6.5)
, (6.5)
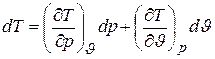 , (6.6)
, (6.6)
где dp,dJ, dT – полные дифференциалы соответствующих параметров.
В указанные уравнения входят шесть частных производных, которые попарно обратны друг другу, например
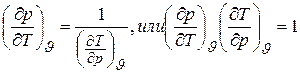 . (6.7)
. (6.7)
Следовательно, самостоятельное значение из шести частных производных имеют только три. В качестве основных применяются частные производные
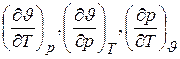 ,
,
которые называются термическими коэффициентами. Каждый из термических коэффициентов имеет определенное физическое содержание.
Так, частная производная 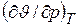 характеризует интенсивность изменения объема при изменении давления в условиях постоянной температуры. Отношение этой величины к начальному объему газа J0, взятое с обратным знаком, называется коэффициентом сжатия
характеризует интенсивность изменения объема при изменении давления в условиях постоянной температуры. Отношение этой величины к начальному объему газа J0, взятое с обратным знаком, называется коэффициентом сжатия
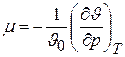 . (6.8)
. (6.8)
Термический коэффициент 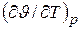 характеризует интенсивность увеличения объема при нагревании при постоянном давлении. Отношение этой величины к начальному объему, т.е.
характеризует интенсивность увеличения объема при нагревании при постоянном давлении. Отношение этой величины к начальному объему, т.е.
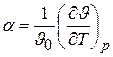 , (6.9)
, (6.9)
называется коэффициентом объемного расширения.
Наконец, термический коэффициент 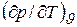 характеризует интенсивность изменения давления при изохорном нагреве тела. Отношение этой величины к начальному давлению р0, т.е.
характеризует интенсивность изменения давления при изохорном нагреве тела. Отношение этой величины к начальному давлению р0, т.е.
|
|
|
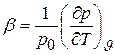 , (6.10)
, (6.10)
называется коэффициентом упругости.
Названные коэффициенты связаны между собой весьма простым соотношением. Найти это соотношение можно следующим образом.
Из математики известно, что если переменные x,y и z связаны между собой уравнением
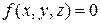
и не зависит от каких – либо других переменных, то их частные производные удовлетворяют тождеству
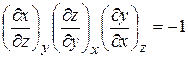 .
.
Применив это положение к уравнению состояния
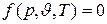 ,
,
получаем
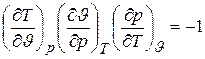
или 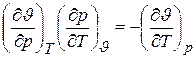 ,
,
т.е уравнение связи между термическими коэффициентами.
Далее, учитывая, что
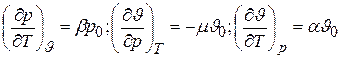 ,
,
находим
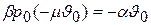 ,
,
или окончательно
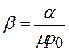 . (6.11)
. (6.11)
Эта формула позволяет теоретически определить коэффициент упругости, нахождение которого опытным путем затруднительно, в то время как коэффициенты a и m легко определяются экспериментально.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 2001; Нарушение авторских прав?; Мы поможем в написании вашей работы!