
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Co(NH3)6]3+ и [CoF6]3-
|
|
|
|
Известно, что первый из них диамагнитен, второй парамагнитен.
Ион-комплексообразователь в этих комплексных ионах имеет электронную конфигурацию 3d6. В соответствии с правилом Хунда эти шесть электронов в d–состоянии располагаются по энергетическим ячейкам следующим образом:
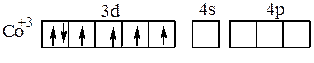
При образовании комплексного иона [Co(NH3)6]3+ четыре d-электрона сначала образуют электронные пары, освобождая две 3d–орбитали:
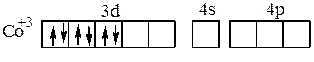
Затем образуется ион [Co(NH3)6]3+, имеющий строение
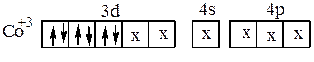
При образовании этого комплекса имеет место d2sp3 -гибридизация, причём она осуществляется при участии внутренних d-орбиталей третьего энергетического уровня иона Co3+. В случае иона [CoF6]3- образования пар d-электронов в ионе Co3+ не происходит. Шесть неподелённых электронных пар ионов F- располагаются в свободных s-,p-, d- орбиталях четвёртого энергетического уровня. Комплексный ион [CoF6]3- имеет строение:
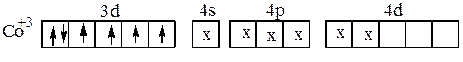
Этот комплексный ион образуется за счёт sp3d2-гибридизации, причём в образовании этого иона участвуют d– орбитали иона Co3+ четвёртого энергетического уровня (внешнего).
Комплексный ион [CoF6]3-, в образовании которого участвуют d-орбитали иона Co3+ четвёртого энергетического уровня, более реакционноспособен, чем ион [Co(NH3)6]3+, так как в [CoF6]3- лиганды слабее связаны с ионом Co3+,чем в [Co(NH3)6]3+, и могут легче отделяться от комплексообразователя.
Рассмотренные примеры показывают, что метод валентных связей успешно объясняет определённые значения координационных чисел и геометрические формы комплексных частиц, различия в магнитных свойствах (диамагнитность или парамагнитность) этих частиц. Однако, некоторые свойства комплексных соединений (например, спектры поглощения) не находят удовлетворительного объяснения с позиций метода валентных связей. Нельзя объяснить с этих позиций также π- дативную связь.
Спаривание же d–электронов Co3+ в [Co(NH3)6]3+ и отсутствие его в [CoF6]3- удовлетворительно объясняется в рамках теории кристаллического поля.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 6575; Нарушение авторских прав?; Мы поможем в написании вашей работы!