
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Устойчивость комплексных соединений
Устойчивость комплексных соединений определяется как внешними условиями (температура, природа растворителя, ионная сила, состав раствора), которые учитываются при расчёте условной константы устойчивости, так и фундаментальными факторами. Такими факторами являются: природа центрального атома и донорных атомов лигандов, структура лигандов и стерические факторы.
Природа центрального атома и лигандов
Согласно теории Льюиса, комплексообразование можно рассматривать как один из видов кислотно-основных равновесий, в котором роль кислоты играет центральный ион (акцептор электронов), а роль основания –лиганды(доноры электронов). В соответствии с теорией Льюиса все кислоты и основания условно делятся на два класса: жёсткие и мягкие кислоты и основания. При оценке жёсткости и мягкости кислот и оснований учитывается их химический состав, электронное строение и сравнительная устойчивость образуемых ими кислотно-основных комплексов. Согласно принципу жёстких и мягких кислот и оснований кислотно-основные взаимодействия протекают таким образом, что жёсткие кислоты предпочтительно связываются с жёсткими основаниями, а мягкие кислоты – с мягкими основаниями. Примеры жёстких и мягких кислот и оснований приведены в табл. 5 и 6:
Таблица 5. Классификация кислот Льюиса
| Жёсткие | Промежу- Точные | Мягкие | |
| Кислоты Льюиса (комплексо- образова- тели) | H+,Li+,Na+, K+,Mg2+,Ca2+, Al3+,Mn2+,Cr3+, Fe3+,Co3+,Zr4+, BF3,AlCl3, HHal,CO2, NC+ | Fe2+,Co2+,Ni2+, Cu2+,Zn2+,Ru2+, Rh3+,Ir3+,SO2, NO+,R3C+,C6H5 | Cu+,Ag+,Au+, Au3+,Hg2+, Pb2+,Bi3+,Cd2+, Pt2+,Pt4+,Cr, Fe,I2,I+,Br+, Br2, RO+, CH3Hg, R+, алкены, хиноны |
Таблица 6. Классификация оснований Льюиса
| Жёсткие | Промежу-точные | Мягкие | |
| Основания Льюиса (донорные атомы лигандов) | F-,OH-,O2-H2O,CO32-, PO43-,SO42-, NO3-,NH3, N2H4,RNH2, CH3COO- ROH,RO-, R2O | C5H5N | R2S,R3P, R3As,CO, RNC |
Применительно к комплексообразованию мягкость кислоты или основания Льюиса означает его склонность к образованию связей преимущественно ковалентного, а жёсткость – преимущественно ионного характера. Типичные жёсткие кислоты (катионы – комплесообразователи) имеют малый атомный или ионный радиус, высокую электроотрицательность, с трудом поляризуются (Н+,Mn2+,Cr3+,Fe3+,Co3+) и трудно восстанавливаются.
Наиболее жёсткие катионы имеют электронную структуру инертного газа и не имеют вакантных энергетически низко расположенных d-орбиталей. Катионы с частично заполненными
d-орбиталями занимают промежуточное положение. При прочих равных условиях жёсткость катиона возрастает с увеличением его заряда. Так, Fe3+ является более жёсткой кислотой Льюиса, чем Fe2+.
Лиганды с высокоотрицательными донорными атомами являются жёсткими основаниями (H2O,OH-,NH3,Cl-), тогда как поляризуемые лиганды – мягкие основания (SCN-, CN-, RS-,RSH).
Мягкие кислоты имеют большие размеры и легко поляризуются (Ag+,Pd2+,Pt2+,Pt4+,Cd2+).Мягкие кислоты Льюиса имеют электроны на d-орбиталях, способные к образованию p-связей в результате перекрывания с вакантными d-орбиталями мягких лигандов. Наиболее устойчивые комплексы образуются между жёсткой кислотой и жёстким основанием или мягкой кислотой и мягким основанием.
Поскольку реакции комплексообразования подразумевают взаимодействие кислот и оснований Льюиса, с увеличением основных свойств лигандов устойчивость комплексов повышается.
Например, среди однотипных соединений: [Ag(NH3)2]+ (β2=1,5×107) и [Ag(CN)2]- (β2=1×1021) более стойким является второе.
Хелатный эффект
Комплексы хелатообразующих реагентов по сравнению с комплексами их монодентатных аналогов обладают повышенной устойчивостью (так называемый хелатный эффект). Например, комплексы этилендиамина устойчивее, чем аммиака, причём устойчивость хелатного цикла зависит от числа атомов в нём; наиболее устойчивы пяти – и шестичленные циклы. Так, для [Cd(NH3)4]2+ константа устойчивости β4=3,63×106,а этилендиаминового комплекса кадмия почти в 106 раз больше- β4=1,91×1012. Объясняется это тем, что при координации этилендиамина
NН2-CH2-CH2-NH2 во внутренней сфере образуется пятичленный цикл. Мерой хелатного эффекта обычно служит разность общих констант устойчивости хелатного комплекса и его нециклического аналога Δlgβ. При этом монодентатный и полидентатный лиганды должны иметь одинаковые донорные атомы и по возможности близкую структуру, а комплексы – иметь одинаковое число донорных атомов и геометрию внутренней координационной сферы. Величины хелатного эффекта для некоторых комплексов приведены в табл.7.
Таблица 7. Хелатный эффект для комплексов некоторых
полиаминов Δlgβ (N – дентатность лигандов)
| Ион | en N = 2 | den N = 3 | trien N = 4 | tren N = 4 | Penten N = 6 |
| Δlgβ | Δlgβ | Δlgβ | Δlgβ | Δlgβ | |
| Co(II) | 2,4 | 3,7 | 5,7 | 7,5 | 10,5 |
| Ni(II) | 2,9 | 4,3 | 6,2 | 7,0 | 10,8 |
| Cu(II) | 3,4 | 6,0 | 7,8 | 6,2 | - |
| Zn(II) | 1,8 | 2,2 | 3,0 | 5,5 | - |
| Cd(II) | 1,2 | 2,7 | 3,8 | 5,4 | 11,9 |
В табл.7 указаны следующие полиамины:en- H2N-CH2-CH2-NH2,
den - H2N-CH2-CH2-NH-CH2-CH2-NH2, tren - N(CH2-CH2-NH2)3,
trien - H2N-CH2-CH2-NH-CH2-CH2-NH-CH2-CH2-NH2,
penten - [CH2-N(CH2-CH2-NH2)2]2.
Величина Δlgβ положительна, если стандартная свободная энергия комплексообразования ΔGо < 0. На практике хелатный эффект имеет как энтальпийную, так и энтропийную составляющие. В самом первом приближении изменение энтропии при химической реакции определяется изменением числа частиц. При этом увеличение числа частиц означает увеличение энтропии. Для монодентатного лиганда изменение суммарного числа частиц в растворе в результате комплексообразования не происходит: [Zn(Н2O)4]2+ + 4NH3 D [Zn(NH3)4]2+ + 4H2O.
Поэтому можно считать, что приблизительно ΔSр-ции = 0.
Если лиганд полидентатный, то суммарное число частиц в ходе реакции увеличивается, и в этом случае ΔSр-ции > 0:
[Zn(OH2)4]2+ + 2NH2(CH2)2NH2 D [Zn(NH2(CH2)2NH2)2]2+ + 4H2O.
Но эти рассуждения можно считать достаточно приблизительными, так как не учитываются: сольватация комплекса, размер цикла и что образующаяся при комплексообразовании вода не остаётся в свободном виде и включается в общую, достаточно упорядоченную структуру воды. Однако увеличение энтропии комплексообразования при переходе от монодентатных к аналогично построенным полидентатным лигандам наблюдается почти всегда (табл.8):
Таблица 8. Константы устойчивости и термодинамические параметры комплексов кадмия(II) с аминами при 25оС
| Комплекс | lgβn | ΔHo кДж/моль | ΔSo Дж/моль·К | ΔGo кДж/моль |
| [Cd(NH3)2]2+ | 4,95 | -29,79 | -5,19 | -28,24 |
| [Cd(NH2CH3)2]2+ | 4,81 | -29,37 | -6,46 | -27,45 |
| [Cd(N2H4C2H4)]2+ | 5,84 | -29,41 | 13,05 | -33,30 |
| [Cd(NH3)4]2+ | 7,44 | -53,14 | -35,50 | -42,51 |
| [Cd(NH2CH3)4]2+ | 6,55 | -57,32 | -66,94 | -37,41 |
| Cd(N2H4C2H4)2]2+ | 10,62 | -56,48 | 13,75 | -60,67 |
В соотвествии с правилом Чугаева наиболее устойчивыми являются пяти- и шестичленные хелатные циклы, и наибольший выигрыш энтропии наблюдается именно у них. Особенно значителен энтропийный эффект, если при образовании комплекса замыкается несколько циклов. Так, комплексы металлов с ЭДТА содержат пять хелатных циклов и поэтому исключительно устойчивы.
Изменение стандартной энтальпии системы в результате комплексообразования: ΔНо = ΔНо1 + ΔНо2.
ΔНо1 характеризует энергию образования координационных связей центрального атома с донорными атомами лиганда. ΔНо2 характеризует изменение энергии лигандов в результате комплексообразования. ΔНо1 < 0, поскольку образование связей металл – лиганд энергетически выгодно.
ΔНо2 > 0, так как ориентация лигандов вокруг центрального атома и связанное с ней их взаимное отталкивание, деформация лигандов и пр. требуют затраты энергии. Если монодентатный и полидентатный лиганды достаточно близки по своей природе, то в первом приближении можно считать, что энергия образования связей для нециклического и хелатного комплексов равны ΔНо1 нецикл = ΔНо1 цикл. Но соответствующие стерические составляющие ΔНо2 нецикл и ΔНо2 цикл могут различаться. Одной из причин этого различия является то обстоятельство, что для ориентации монодентатных лигандов вокруг центрального атома надо затратить больше энергии, чем для ориентации полидентатных лигандов, поскольку в полидентатном лиганде его функциональные группы уже ориентированы друг относительно друга. Таким образом ΔНо2 нецикл > ΔНо2 цикл, и,
следовательно, в итоге ΔНоцикл - ΔНонецикл < 0.
Стерические факторы
Чем меньше радиус иона-комплексообразователя, и чем выше его заряд, тем более прочные комплексы он образует. Так, для [Co(NH3)6]2+ lgβ6 =4,39, а для [Co(NH3)6]3+ lgβ6=35,21.
Комплексный ион [Co(NH3)6]2+ обратимо распадается в воде:
[Co(NH3)6]2+ + 6H2O D [Co(H2O)6]2+ + 6NH3.В то же время комплексный ион [Co(NH3)6]3+ практически не разрушается водой.
Устойчивость комплексных соединений также зависит от пространственного окружения донорных атомов. Введение заместителей в положения, близкие к донорным атомам, может затруднить образование комплекса. Особенно сильно проявляются стерические затруднения в комплексах с хелатообразующими лигандами. Например, такой эффект наблюдается при использовании 2-алкилпроизводных 8-оксихинолина(HL):

Он может образовывать с двухзарядными ионами внутрикомплексные соединения тетраэдрической конфигурации состава МL2,а с трёхзарядными - октаэдрические комплексы МL3. Однако для ионов малого радиуса, в частности Al3+, образование комплексов ML3 невозможно ввиду стерических затруднений, создаваемых группой в положении 2. В этом случае образуются лишь заряженные, растворимые комплексы ML2+и ML2+. На этом основано применение в аналитической химии 2-замещённых
8-оксихинолинов для осаждения ионов Cr3+,Fe3+,Zn2+ в присутствии Al3+.
Пространственные затруднения возникают и при образовании комплексов с вынужденной конфигурацией. Так, линейный триэтилентетрамин образует с ионами Cu2+ более устойчивый хелат, чем разветвлённый:
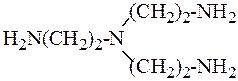
В первом случае возможна более благоприятная для Cu2+ плоская квадратная конфигурация, во втором требуется не характерная для Cu2+ тетраэдричекая структура. Для Zn2+, наоборот, предпочтительнее тетраэдрическая конфигурация, поэтому с разветвлённым амином комплекс Zn2+ более устойчив.
|
Дата добавления: 2014-01-03; Просмотров: 6768; Нарушение авторских прав?; Мы поможем в написании вашей работы!