
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Влияние температуры наскорость реакции
|
|
|
|
Правило Вант-Гоффа
С повышением температуры скорость реакции увеличивается. Зависимость скорости реакции от температуры приближенно описывается эмпирическим правилом Вант-Гоффа: при повышении температуры на каждые 10° скорость реакции увеличивается в 2-4 раза.
Математическое выражение правила Вант-Гоффа:
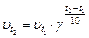 (16),
(16),
а при условии, что концентрации всех реагирующих веществ равны 1 моль/л:
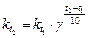 (17),
(17),
где 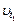 ,
, 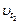 и
и 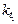 ,
, 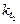 - соответственно скорости и константы скоростей реакции при температурах
- соответственно скорости и константы скоростей реакции при температурах 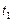 и
и 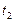 .
.
Температура может быть выражена как в °С, так и в К, так как изменение температуры не зависит от единиц измерения (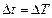 ).
).
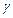 - температурный коэффициент скорости реакции, который показывает, во сколько раз возрастает скорость реакции при повышении температуры на 10 градусов:
- температурный коэффициент скорости реакции, который показывает, во сколько раз возрастает скорость реакции при повышении температуры на 10 градусов:
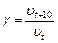 (18)
(18)
Поскольку при концентрациях реагирующих веществ 1 моль/л скорость химической реакции численно равна константе скорости 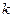 , то
, то
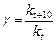 (19)
(19)
Учитывая тот факт, что скорость реакции обратно пропорциональна времени ее протекания из уравнения (18), при 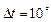 получаем
получаем
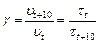 (20)
(20)
Используя уравнения (16 – 20), можно рассчитать:
- константу скорости (или скорость) реакции при заданной температуре, если известны значения этих величин при двух других температурах;
- на сколько градусов надо повысить (или понизить) температуру реакции, чтобы скорость ее увеличилась (или уменьшилась) в N раз;
- при какой температуре следует проводить реакцию, чтобы она закончилась за определенное время, если известны температурный коэффициент реакции и скорость ее при любой температуре;
- температурный коэффициент реакции и т. д.
Задача 1. Как изменится скорость реакции при повышении температуры от 0 до 100 оС, если g=2?
|
|
|
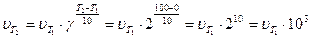 или
или 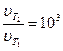
Ответ: скорость реакции увеличилась в 103 раз.
Задача 2. Во сколько раз изменится скорость реакции при понижении температуры от60 до 30 оС, если g = 3?
Воспользуемся правилом Вант-Гоффа. Обратите внимание на то, что температура понижается, следовательно
Т1 = 60 оС,
Т2 = 30 оС
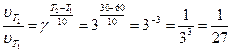
Ответ: скорость реакции уменьшилась в 27 раз.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 641; Нарушение авторских прав?; Мы поможем в написании вашей работы!