
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электролиз расплавов
|
|
|
|
Электролиз расплавов электролитов обычно ведут с использованием инертных (неактивных, не расходуемых) электродов, то есть электродов, выполненных из материалов, которые в процессе электролиза химически не изменяются, а служат лишь для передачи электронов. Инертные электроды обычно изготовляются из графита, угля, платины. Кроме инертных анодов различают также растворимые (активные, расходуемые) аноды. Это аноды, выполненные из активных материалов (меди, цинка, никеля, железа и др. металлов). У таких анодов в процессе электролиза окисляется в первую очередь сам материал анода.
Рассмотрим процессы, протекающие при электролизе расплава хлорида магния. При плавлении MgCl2 (как и любого другого ионного соединения) происходит его термическая диссоциация по уравнению
MgCl2 ® Mg2+ + 2Cl–.
Если в такой расплав погрузить инертные электроды и пропускать электрический ток, то в электролите начнется направленное движение ионов: положительно заряженные ионы (катионы) будут двигаться к отрицательному электроду (катоду), а отрицательно заряженные ионы (анионы) направятся к аноду. Схематично эти процессы на примере MgCl2 можно представить так
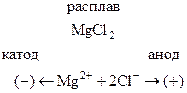
На электродах будут протекать следующие процессы:
1) восстановление катионов на катоде
Mg2+ + 2 ē ® Mg
2) окисление анионов на аноде
2Cl– – 2 ē ® Cl2
Суммарная реакция электролиза расплава хлорида магния
MgCl2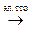 Mg + Cl2
Mg + Cl2
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 471; Нарушение авторских прав?; Мы поможем в написании вашей работы!