
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Характерная окраска и области перехода ряда индикаторов
|
|
|
|
| Индикатор | Область перехода рН | Окраска | |
| в кислом растворе | в щелочном растворе | ||
| Пикриновая кислота | 0,0-2,0 | Бесцветная | Желтая |
| Метиловый оранжевый | 3,1-4,4 | Розовая | Оранжево-желтая |
| Метиловый красный | 4,2-6,3 | Красная | Оранжево-желтая |
| Лакмус | 6,0-8,0 | Красная | Синяя |
| Феноловый красный | 6,8-8,4 | Желтая | Красная |
| Фенолфталеин | 8,0-10,0 | Бесцветная | Малиновая |
| Ализариновый желтый | 10,1-12,1 | Желтая | Оранжевая |
Индикаторы чаще всего представляют собой слабые органические кислоты или основания, имеющие различную окраску молекулярной и ионной форм. Диссоциация этих веществ в растворе протекает по следующему механизму:
Ind OH <–> ОН– + Ind+
H Ind<–> H+ + 1пd–
Так как процесс диссоциации слабых электролитов обратим, положение равновесия будет определяться кислотностью исследуемого раствора. Предположим, что молекулярная форма индикатора лакмуса — органической кислоты Hind– — имеет красную окраску, а ионная (1пd–) — синюю. В кислых растворах, в соответствии с принципом Ле-Шателье, подобный индикатор преимущественно находится в виде молекул, и окраска раствора красная. При смещении рН раствора в сторону больших значений (щелочная среда) равновесие сместится вправо и раствор приобретет синюю окраску. Индикаторы, имеющие две окрашенные формы, называются двухцветными. К таким индикаторам относятся, кроме лакмуса, метиловый оранжевый, метиловый красный и т. д. Индикаторы, имеющие только одну окрашенную форму, называются одноцветными (фенолфталеин).
Изменение окраски индикатора связано с таутомерией органических молекул, содержащих хромофорные группы (так называемые «носители цвета»), содержащие л-электроны. Наиболее известными хромофорными группами являются карбонильные группы — СОН, расположенные в определенной последовательности, азогруппа — N = N—, нитрогруппа -О—N = О, —N= N— и т. д. Молекулы индикатора также содержат ауксохромные и антиауксохромные группы, которые в присутствии хромофоров усиливают окраску за счет влияния на распределение электронной плотности в молекуле. К первым относятся галогенид-ионы —F, —Сl, —Вr; гидроксильная группа —ОН; аминогруппа — МН2; ко вторым относятся — NH3+; —SО2NН2; —СN; —СООСН3. Согласно хромофорной теории окраски присоединение или отщепление протона вызывает перестройку молекулы индикатора, в результате которой появляются новые или исчезают существовавшие ранее хромофорные группы, что, в свою очередь, приводит к изменению окраски. В качестве примера рассмотрим индикатор фенолфталеин, который является слабой органической кислотой. Молекулярная форма H Ind бесцветна, так как не имеет хромофорной группировки, а ионная форма 1пd– имеет красно-малиновую окраску. В состав молекулы фенолфталеина входят три бензольных ядра, одно из которых может переходить в хиноидную группу, которая является хромофором. В растворах данного индикатора устанавливается равновесие между бензольной и хиноидной структурами:
|
|
|
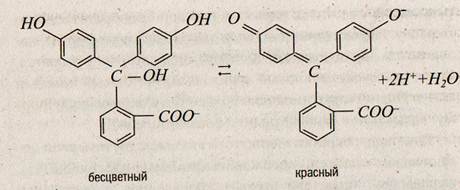
Структурные изменения в растворах метилового оранжевого при изменении рН можно представить схемой:
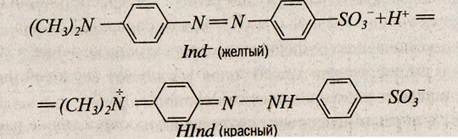
В качестве индикаторов также используются другие группы органических соединений: сульфофталеины (тимоловый синий, бромкрезоловый зеленый, феноловый красный), три-фенилметановые красители (метиловый фиолетовый, кристаллический фиолетовый, метиловый фиолетовый) и др. При смешении нескольких индикаторов можно получить универсальный индикатор, имеющий соответствующую окраску при любом значении рН.
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 934; Нарушение авторских прав?; Мы поможем в написании вашей работы!