
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термодинамические свойства простых веществ и соединений
|
|
|
|
Средняя изобарная теплоемкость простых веществ и соединений
СПРАВОЧНЫЕ ТАБЛИЦЫ
Таблица 7.1.
Средние изобарные теплоемкости СP, 298-Т (в Дж/(моль·К)) приведены для температурного интервала от 298 К до указанной в таблице температуры. Для некоторых веществ Сp, 298-Т приведены с учетом превращения α-модификации в β- и γ- или плавления вещества.
| Вещество | Температура, К | ||||||
| Простые вещества | |||||||
| Ag (кр.) Аl (кр.) С (графит) Сu (кр.) Fе-α Н2 (г.) Ni (-α,- β) О2 (г.) Zn (кр.) | 25,90 25,75 13,03 25,15 27,12 28,92 28,74 (α) 30,28 26,38 | 26,20 26,01 14,22 25,46 28,36 29,02 30,21 (α) 30,87 26,89 | 26,48 26,27 15,15 25,77 29,60 29,15 31,55 (β) 31,34 27,39 (690 К) | 26,76 26,53 15,90 26,09 30,74 29,28 31,39 31,74 – | 27,03 26,79 16,54 26,40 32,31 29,42 31,41 32,09 – | 27,31 27,05 17,09 26,72 34,70 29,57 31,56 32,39 – | |
| Продолжение табл. 7.1 | |||||||
| Вещество | Температура, К | ||||||
| Неорганические соединения | |||||||
| СО (г.) СО2 (г.) СаС2- α СаСО3 (кальцит) СаО (кр.) Са(ОН)2 (кр.) FеО (кр.) Fe3O4(кр.) Н2О (г.) МgСО3(кр.) МgО (кр.) ZnS (кр.) ZnSO4(кр.) | 29,74 42,02 67,55 95,86 46,76 97,23 52,01 169,63 34,49 89,26 42,56 48,10 106,74 | 29,99 43,43 69,12 99,86 47,76 99,39 52,82 180,08 34,99 94,10 43,99 48,91 110,55 | 30,24 44,56 70,40 103,03 48,55 – 53,51 190,52 35,50 98,38 45,06 49,55 114,36 | 30,47 45,52 – 105,69 49,19 – 54,14 200,97 36,02 – 45,90 50,11 118,17 | 30,69 46,37 – 107,97 49,74 – 54,72 – 36,54 – 46,59 50,60 121,97 | 30,92 47,15 – 110,06 50,23 – 55,28 – 37,06 – 47,18 51,04 125,78 | |
| Окончание табл. 7.1 | |||||||
| Вещество | Температура, К | ||||||
| Органические соединения | |||||||
| СH4 (г.) C2H2 (г.) С2H4 (г.) С2H6 (г.) C6H6 (г.) CH2O (г.) CH2O2 (г.) СH4O (г.) метанол С2H6O (г.) этанол С3H6O (г.) ацетон СCl4 (г.) CHCl3 (г.) CH2Cl2 (г.) | 41,16 48,72 53,84 66,21 110,94 39,57 56,66 52,20 80,57 92,64 90,00 74,16 58,96 | 44,06 50,83 58,17 72,27 123,02 41,77 60,12 56,03 87,39 99,81 92,54 77,38 62,36 | 46,85 52,75 62,25 77,94 133,98 43,86 63,24 59,64 93,69 106,53 94,75 80,00 65,46 | 49,52 54,49 66,08 83,24 143,81 45,84 66,03 63,04 99,48 112,81 96,63 82,00 68,25 | 52,08 56,06 69,66 88,14 152,50 47,72 68,49 66,22 104,74 118,65 98,18 83,41 70,72 | 54,52 57,46 72,98 92,66 160,06 49,50 70,66 69,21 109,55 124,10 99,40 84,21 72,89 | |
Таблица 7.2
|
|
|
ΔНof,298 и ΔGof,298 – изменения стандартных энтальпии (теплоты образования) и энергии Гиббса при образовании (индекс f- formation) данного вещества из простых веществ, термодинамически устойчивых при 101,325 кПа (1 атм) и при выбранной температуре 298 К. So298 и coP,298 – стандартные значения энтропии и изобарной теплоемкости вещества при 298 К. Теплоемкость в 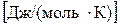 при температуре Т в указанном в таблице интервале температур выражается уравнениями:
при температуре Т в указанном в таблице интервале температур выражается уравнениями:
coP = а + bT + с/ / Т2 (простые и неорганические вещества) или co P = а + bT + сТ2 (органические вещества).
| Вещество | ΔНof,298, кДж/моль | So298, Дж/(моль∙ּК) | ΔGof,298, кДж/моль | coP, Дж/(моль∙ּК) | Коэффициенты уравнения coP = f(Т) | Температурный интервал, К | ||
| а | b ∙ 103 | c' ∙ּ 10-5 | ||||||
| Простые вещества | ||||||||
| Ag (кр.) Al (кр.) Au (кр.) Bi (кр.) Br2 (г.) С (графит) | 30,91 | 42,55 28,33 47,40 56,90 245,37 5,74 | 3,14 | 25,44 24,35 25,36 26,02 36,07 8,54 | 23,97 20,67 23,68 18,79 37,32 16,86 | 5,27 12,38 5,19 22,59 0,50 4,77 | – 0,25 – – – –1,26 –8,54 | 273–1234 273–932 298–1336 298–544,5 298–1600 298–2500 |
| Продолжение табл. 7.2 | ||||||||
| Вещество | ΔНof,298, кДж/моль | So298, Дж/(моль∙ּК) | ΔGof,298, кДж/моль | coP, Дж/(моль∙ּК) | Коэффициенты уравнения coP = f(Т) | Температурный интервал, К | ||
| а | b ∙ּ 103 | c' ∙ 10-5 | ||||||
| Cl2 (г.) Cr (кр.) Cu (кр.) F2 (г.) Fe-α Gе (кр.) Н2 (г.) I2 (г.) Мg (кр.) N2 (г.) Ni-α О2 (г.) Рb (кр.) S (монокл.) S (ромб.) S (г.) S2 (г.) | 62,43 0,38 278,81 128,37 | 222,98 23,64 33,14 202,67 27,15 31,09 130,52 260,60 32,68 191,50 29,87 205,04 64,81 32,55 31,92 167,75 228,03 | 19,39 0,19 0 238,31 79,42 | 33,93 23,35 24,43 31,30 24,98 23,35 28,83 36,90 24,89 29,12 26,07 29,37 26,82 23,64 22,68 23,67 32,51 | 37,03 24,43 22,64 34,56 17,24 25,02 27,28 37,40 22,30 27,88 16,99 31,46 24,23 23,64 22,68 – 36,11 | 0,67 9,87 6,28 2,51 24,77 3,43 3,26 0,59 10,63 4,27 29,46 3,39 8,71 – – – 1,09 | –2,85 –3,68 – –3,51 – –2,34 0,50 –0,71 –0,42 – – –3,77 – – – – –3,51 | 298–3000 298–2000 298–1357 298–2000 298–700 298–1210 298–3000 298–3000 298–920 298–2500 298–633 298–3000 298–601 368–392 273–368 – 298–2000 |
|
|
|
| Продолжение табл. 7.2 | ||||||||
| Вещество | ΔНof,298, кДж/моль | So298, Дж/(моль∙ּК) | ΔGof,298, кДж/моль | coP, Дж/(моль∙ּК) | Коэффициенты уравнения coP = f(Т) | Температурный интервал, К | ||
| а | b ∙ 103 | c' ∙ 10-5 | ||||||
| Si (кр.) Sn (бел.) Тi -α Tl -α W (кр.) Zn (кр.) | 18,83 51,55 30,63 64,18 32,64 41,63 | 19,99 26,99 25,02 26,32 24,27 25,44 | 22,82 21,59 21,10 22,01 22,91 22,38 | 3,86 18,10 10,54 14,48 4,69 10,04 | –3,54 – – – – – | 298–1685 298–505 298–1155 273–500 298–2500 273–690 | ||
| Неорганические соединения | ||||||||
| Al2О3 (корунд) Al2(SO4)3 (кр.) СО (г.) СО2 (г.) СОСl2 (г.) СS2 (г.) CaC2-α СаСО3 (кальцит) СаО (кр.) Са(ОН)2 (кр.) FeO (кр.) | –1675,69 –3441,80 –110,53 –393,51 –219,50 116,70 –59,83 –1206,83 –635,09 –985,12 –264,85 | 50,92 239,20 197,55 213,66 283,64 237,77 69,96 91,71 38,07 83,39 60,75 | –1582,27 –3100,87 –137,15 –394,37 –205,31 66,55 –64,85 –1128,35 –603,46 –897,52 –244,30 | 79,04 259,41 29,14 37,11 57,76 45,48 62,72 83,47 42,05 87,49 49,92 | 114,55 366,31 28,41 44,14 67,15 52,09 68,62 104,52 49,62 105,19 50,80 | 12,89 62,59 4,10 9,04 12,03 6,69 11,88 21,92 4,52 12,01 8,61 | –34,31 –112,47 –0,46 –8,54 –9,04 –7,53 –8,66 –25,94 –6,95 –19,00 –3,31 | 298–1800 298–1100 298–2500 298–2500 298–1000 298–1800 298–720 298–1200 298–1800 298–600 298–1650 |
| Продолжение табл. 7.2 | ||||||||
| Вещество | ΔНof,298, кДж/моль | So298, Дж/(моль∙ּК) | ΔGof,298, кДж/моль | coP, Дж/(мольּ∙К) | Коэффициенты уравнения coP = f(Т) | Температурный интервал, К | ||
| а | b ∙ 103 | c' ∙ 10-5 | ||||||
| НВr (г.) НСl (г.) НF (г.) НI (г.) Н2О (ж.) Н2О (г.) Н2S (г.) MgCO3 (кр.) МgО (кр.) Мg(ОН)2 (кр.) NH3 (г.) NH4Cl-β NО (г.) NO2 (г.) РСl3 (г.) РСl5 (г.) SO2 (г.) | –36,38 –92,31 –273,30 26,36 –285,83 –241,81 –20,60 –1095,85 –601,49 –924,66 –45,94 –314,22 91,26 34,19 –287,02 –374,89 –296,90 | 198,58 186,79 173,67 206,48 69,95 188,72 205,70 65,10 27,07 63,18 192,66 95,81 210,64 240,06 311,71 364,47 248,07 | –53,43 –95,30 –275,41 1,58 –237,23 –228,61 –33,50 –1012,15 –569,27 –833,75 –16,48 –203,22 87,58 52,29 –267,98 –305,10 –300,21 | 29,14 29,14 29,14 29,16 75,30 33,61 33,44 76,11 37,20 76,99 35,16 84,10 29,86 36,66 71,84 112,97 39,87 | 26,15 26,53 26,90 26,32 39,02 30,00 29,37 77,91 48,98 46,99 29,80 – 29,58 41,16 80,11 129,49 46,19 | 5,86 4,60 3,43 5,94 76,64 10,71 15,40 57,74 3,14 102,85 25,48 – 3,85 11,33 3,10 2,93 7,87 | 1,09 1,09 1,09 0,92 11,96 0,33 – –17,41 –11,44 – –1,67 – –0,59 –7,02 7,99 –16,40 –7,70 | 298–1600 298–2000 298–2500 298–2000 273–380 298–2500 298–1800 298–750 298–3000 298–541 298–1800 – 298–2500 298–1500 298–1000 298–1500 298–2000 |
| Продолжение табл. 7.2 | ||||||||
| Вещество | ΔНof,298, кДж/моль | So298, Дж/(моль∙ּК) | ΔGof,298, кДж/моль | coP, Дж/(мольּ∙К) | Коэффициенты уравнения coP = f(Т) | Температурный интервал, К | ||
| а | b ∙ 103 | c' ∙ 10-5 | ||||||
| SO 2Cl2 (г.) SO3 (г.) SiO2 (кварц-α) SnO2 (кр.) ТiО2 (рутил) ТiО2(анатаз) | –363,17 –395,85 –910,94 –580,74 –944,75 –933,03 | 311,29 256,69 41,84 52,30 50,33 49,92 | –318,85 –371,17 –856,67 –519,83 –889,49 –877,65 | 77,40 50,09 44,43 52,59 55,04 55,21 | 87,91 64,98 46,99 73,85 62,86 75,04 | 16,15 11,75 34,31 10,04 11,36 | –14,23 –16,37 –11,30 –21,59 –9,96 –17,63 | 298–1000 298–1300 298–846 298–1500 298–2140 298–2000 |
| Органические соединения | ||||||||
| Коэффициенты уравнения coP = f(Т) | ||||||||
| а | b ∙ 103 | c ∙ 106 | ||||||
| Углеводороды | ||||||||
| СН4 (г.) метан С2Н2 (г.) ацетилен С2Н4 (г.) этилен С2Н6 (г.) этан С3Н6 (г.) пропен С3Н8(г.) пропан C4H6 (г.) 1,2-бутадиен | –74,85 226,75 52,30 –84,67 20,41 –103,85 162,21 | 186,27 200,82 219,45 229,49 266,94 269,91 293,01 | –50,85 209,21 68,14 –32,93 62,70 –23,53 198,44 | 35,71 43,93 43,56 52,64 63,89 73,51 80,12 | 14,32 26,44 11,32 5,75 12,44 1,72 17,74 | 74,66 66,65 122,01 175,11 188,38 270,75 234,43 | –17,43 –26,48 –37,90 –57,85 –47,60 –94,48 –84,73 | 298–1500 298–1000 298–1500 298–1500 298–1000 298–1500 298–1000 |
| Продолжение табл. 7.2 | ||||||||
| Вещество | ΔНof,298, кДж/моль | So298, Дж/(моль∙ּК) | ΔGof,298, кДж/моль | coP, Дж/(моль∙ּК) | Коэффициенты уравнения coP = f(Т) | Температурный интервал, К | ||
| а | b ∙ 103 | c ∙ 106 | ||||||
| С4Н8 (г.) 1-бутен С4Н10 (г.) бутан С6Н6 (г.) бензол С6Н12 (ж.) циклогексан С6Н12(г.) циклогексан | –0,13 –126,15 82,93 –156,23 –123,14 | 305,60 310,12 269,20 204,35 298,24 | 71,26 –17,19 129,68 26,60 31,70 | 85,65 97,45 81,67 156,48 106,27 | 21,47 18,23 –21,09 – –51,71 | 258,40 303,56 400,12 – 598,77 | –80,84 –92,65 –169,87 – –230,00 | 298–1500 298–1500 298–1000 – 298–1000 |
| Кислородсодержащие соединения | ||||||||
| СН2О (г.) формальдегид СН2О2 (г.) муравьиная кислота СН4О (г.) метанол С2Н4О2 (г.) уксусная кислота С2Н4О (г.) ацетальдегид С2Н6О (г.) этанол С3Н6О (г.) ацетон | –115,90 –378,80 –201,00 –434,84 –166,0 –234,80 –217,57 | 218,78 248,77 239,76 282,50 264,2 281,38 294,93 | –109,94 –351,51 –162,3 –376,68 –132,95 –167,96 –153,05 | 35,39 45,80 44,13 66,50 54,64 65,75 74,90 | 18,82 19,40 15,28 14,82 13,00 10,99 22,47 | 58,38 112,80 105,20 196,70 153,50 204,70 201,80 | –15,61 –47,50 –31,04 –77,70 –53,70 –74,20 –63,50 | 298–1500 298–1000 298–1000 298–1000 298–1000 298–1000 298–1500 |
| Продолжение табл. 7.2 | ||||||||
| Вещество | ΔНof,298, кДж/моль | So298, Дж/(моль∙ּК) | ΔGof,298, кДж/моль | coP, Дж/(мольּ∙К) | Коэффициенты уравнения coP = f(Т) | Температурный интервал, К | ||
| а | b ∙ 103 | c ∙ 106 | ||||||
| С3H8O (г.) 1- пропанол C4H10O (г.) бутанол C4H10O (г.) диэтиловый эфир | –257,53 –274,43 –252,21 | 324,80 363,17 342,67 | –163,01 –150,73 –122,39 | 87,11 110,00 112,51 | 13,10 14,68 21,09 | 277,50 358,10 341,70 | –98,44 –129,00 –117,90 | 298–1000 298–1000 298–1000 |
| Галогенсодержащие соединения | ||||||||
| ССl4 (г.) тетрахлорметан СНСl3 (г.) трихлорметан СН3Сl (г.) хлорметан C2H5Cl (г.) хлорэтан C6H5Cl (г.) хлорбензол | –100,42 –101,25 –86,31 –111,72 51,84 | 310,12 295,64 234,47 275,85 313,46 | –58,23 –68,52 –62,90 –60,04 99,15 | 83,76 65,73 40,75 62,72 98,03 | 59,36 29,50 15,57 11,63 –3,09 | 97,00 148,90 92,74 193,00 388,92 | –49,57 –90,70 –28,31 –72,92 –166,25 | 298–1000 298–773 298–1500 298–1000 298–1000 |
|
|
|
|
|
|
Таблица 7.3
|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 1575; Нарушение авторских прав?; Мы поможем в написании вашей работы!