
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Экспериментальная часть
|
|
|
|
Аминофенолы
Аминоспирты
Аминоспирты – это органические вещества, содержащие в молекуле OH- и NH2-группы. Наиболее важными являются 1,2-аминоспирты. Аминогруппа может быть первичной, вторичной, третичной. Могут существовать и четвертичные аммониевые основания. В промышленности 1,2 – аминоспирты получают действием большого количества аммиака или аминов на 1,2 – эпоксиды.

этиленоксид 2 – аминоэтанол (коламин)
Побочно образуются 16 % диэтаноламин (НОСН2СН2)2NH, 4 % триэтаноламина (HOCH2CH2)3N.
Аминоспирты проявляют химические свойства и спиртов и аминов. Однако взаимное влияние функциональных групп приводит к ряду особенностей. Из-за электроноакцепторного влияния ОН-группы основность аминоспиртов и нуклеофильность их атома азота ниже, чем у алифатических аминов, т.е. они образуют соли только с сильными минеральными и органическими кислотами, а нуклеофильные реакции протекают для них труднее. Нуклеофильность атома кислорода ОН-группы также понижена благодаря – I – эффекту аминогруппы, в результате чего аминоспирты этерифицируются труднее, чем алифатические спирты.
Этаноламины применяются как органические основания для связывания кислых газов, входят в состав моющих средств. Из триэтаноламина получается N(CH2CH2Cl)3 – "азотистый спирт", боевое отравляющее стойкое вещество.
Аминоспирты имеют большое биологическое значение, т. к. входят в состав тканей органов животных и человека. Так, коламин – структурный компонент сложных липидов.
Холин – гидроокись β-оксиэтилтриметиламмония

этиленоксид холин
Холин содержится в тканях организма, особенно высоко его содержание в нервных тканях, в частности в мозге, а также в печени, почках, мышцах сердца. Играет большую роль в обмене веществ, в построении клеточных мембран, входит в состав лицитинов и сфингомиэлинов.
Ацетилхолин – сложный эфир холина –
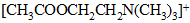
важнейший нейромедиатор – химический передатчик нервного импульса. Его действие прекращается под влиянием фермента ацетилхолестеразы, которая вызывает его гидролиз на холин и уксусную кислоту. При ингибировании ацетилхолин-эстеразы ацетилхолин накапливается в организме, что приводит к непрерывной передаче нервных импульсов и соответственно к непрерывному сокращению мускульной ткани. На этом основано действие инсектицидов и нервнопаралитических ядов.
К аминофенолам относят соединения, в которых NH2- и OH- группы присоединены к бензольному кольцу. Известны о-, м- и n-аминофенолы

Наибольший интерес представляет n-изомер; его производные находят применение в медицине как обезболивающие и жаропонижающие средства

парацетомол фенацетин
(4΄-гидроксиацетанилид) (4΄-этоксиацетанилид)
Биологическое значение имеют производные фенолов, содержащие аминогруппу в боковой цепи. Соединения такого типа, в которых фенольный фрагмент представлен пирокатехином, называют катехоламинами. Важнейшими из них являются адреналин и норадреналин – гормоны мозгового слоя надпочечников человека и животных. Относятся к нейромедиаторам, участвуют в регуляции сердечной деятельности и обмена углеводов и жиров

адреналин норадреналин
Опыт № 1. Амфотерные свойства аминокислот.
а) в пробирку поместите 5 капель 1 % раствора α-аланина или другой аминокислоты и добавьте по каплям 9,1 % хлороводородной кислоты, подкрашенной индикатором конго в синий цвет до появления розово-красной окраски. Напишите уравнение реакции и объясните изменение окраски.
б) В пробирку поместите 5 капель 1 % раствора аминокислоты и по каплям добавьте 0,1 % раствора гидроксида натрия, подкрашенного фенолфталеином, до исчезновения окраски. Объясните происходящее явление и напишите уравнение реакции.
Опыт № 2. Реакция глицина с азотистой кислотой.
В пробирку поместите 5 капель 1 %-го раствора глицина и равный объем 5 %-го раствора нитрита натрия. Добавьте 2 капли конц. уксусной кислоты и осторожно взболтайте смесь. Наблюдается выделение газа; реакция используется для качественного определения аминогрупп в аминокислотах. Напишите схему взаимодействия глицина с азотистой кислотой.
Опыт № 3. Нингидриновая реакция на аминогруппу в α-положении.
Растворы α-аминокислот при нагревании с нингидрином дают синее окрашивание. В этой реакции α-аминокислоты окисляются нингидрином, подвергаясь при этом окислительному дезаминированию и декарбоксилированию.
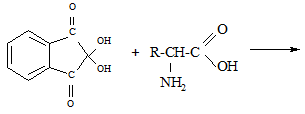
нингидрин α-аминокислота

альдегид нингидрин (восст.)
Восстановленный нингидрин конденсируется с другой молекулой нингидрина в окисленной форме, образуя окрашенный продукт конденсации:

В пробирку поместите 4 капли 1 %-ного раствора глицина и 0,1 %-ного раствора нингидрина. Содержимое пробирки осторожно нагреть до появления сине-красного цвета.
Опыт № 4. Биуретовая реакция на пептидные связи.
В щелочной среде при добавлении к раствору белка гидрата окиси меди образуется комплексное (хелатное) соединение розово-фиолетового цвета. Такую реакцию дают белки, некоторые аминокислоты, пептиды, биурет, средние пептиды.
Впервые данный комплекс получен Биуретом (NH2CONHCONH2). Отсюда и название – биуретовая реакция. Схематично реакцию Cu(ОН)2 с пептидами можно представить так:


В пробирку поместите 5–6 капель белка, добавьте равный объем 30 %-го раствора NaOH и по стенке добавьте 1–2 капли раствора сульфата меди. Наблюдается появление красно-фиолетового окрашивания.
Опыт № 5. Ксантопротеиновая реакция на ароматические аминокислоты – реакция нитрования бензольного ядра циклических аминокислот концентрированной азотной кислотой.
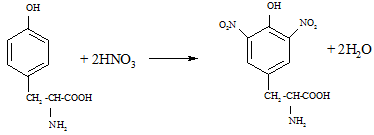
тирозин динитротирозин
В результате образуются нитропроизводные аминокислот, имеющие желтую окраску. В щелочной среде нитропроизводные образуют соли хиноидной структуры, окрашенные в оранжевый цвет (ксантиновый).
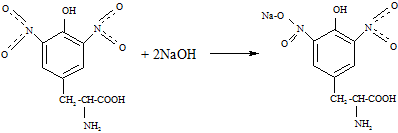
В белке содержится достаточное количество ароматических аминокислот, поэтому ксантопротеиновая реакция применяется и для определения белков.
В пробирку поместите 10 капель раствора тирозина (раствор белка) и 2 капли конц. азотной кислоты.
Содержимое пробирки осторожно нагрейте до растворения осадка. Образуется раствор лимонно-желтого цвета. Охладив пробирку, осторожно добавьте 1–3 капли 10 %-го раствора гидроксида натрия до появления ярко-желтого цвета. Написать уравнение реакции.
|
|
|
|
|
Дата добавления: 2017-02-01; Просмотров: 209; Нарушение авторских прав?; Мы поможем в написании вашей работы!