
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Висота адсорбера 1 страница
|
|
|
|
Вступ
Дифузія
Знак (-) показує, що енерґія переноситься у
Теплопровідність
Якщо в одній області газу середня кінетична енерґія молекул більша ніж віншій, то з часом, внаслідок постійних зіткнень відбудеться вирівнювання середніх значень кінетичної енерґії молекул, тобто вирівнювання температури.
Перенесення енерґіїв формі теплоти описується законом Фур’є:
 , (6.12)
, (6.12)
де JE - густина теплового потоку, яка визначається
енерґією, що переноситься у формі теплоти
за одиницю часу через поверхню одиничної
площі, перпендикулярну до осі ОZ;
 - теплопровідність, яка чисельно дорівнює
- теплопровідність, яка чисельно дорівнює
густині теплового потоку при одиничному
ґрадієнті температури;
 - ґрадієнт температури в напрямі осі ОZ.
- ґрадієнт температури в напрямі осі ОZ.
напрямі зменшення температури.
Явище самовільного взаємопроникнення і перемішування частинок двох газів, рідин чи навіть твердих тіл, які дотикаються називають дифузією. Дифузія призводить до обміну частинками маси тіл, які дотикаються і виникає та продовжується, поки існує ґрадієнт густини. Явище дифузії описується законом Фіка:
 , (6.13)
, (6.13)
де Jm – густина потоку маси, яка визначається масою
речовини, що дифундує за одиницю часу
через поверхню одиничної площі перпенди-
кулярно до осі ОZ;
D – коефіцієнт дифузії, який чисельно дорівнює
густині потоку маси при одиничному
ґрадієнті густини;
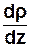 – ґрадієнт густини в напрямі осі ОZ. Знак (-)
– ґрадієнт густини в напрямі осі ОZ. Знак (-)
показує, що перенесення маси відбувається у
напрямку зменшення густини.
Між коефіцієнтами явищ перенесення існують такі залежності:
 ;
;
(6.14)
 .
.
де сv – питома теплоємність речовини при постійному об’ємі.
Адсорбція - процес вибіркового поглинання одного або декількох компонентів з газової суміші або розчину твердим поглиначем.
|
|
|
Речовина, яка міститься в газовій (або рідкій) фазі та при адсорбції не переходить в тверду фазу, називається газом-носієм (рідиною-носієм).
Тверда речовина, яка поглинає речовини, що адсорбуються називається адсорбентом.
Речовина, яка міститься в газовій (або рідкій) фазі та при адсорбції переходить в тверду, тобто поглинається, називається адсорбтивом.
Речовина, яка поглинулась твердою фазою називається адсорбатом.
Процеси адсорбції є вибірковими і зазвичай зворотними. Завдяки їх зворотності можна виділяти поглинуті речовини з адсорбенту. Цей процес називається десорбцією.
Процес адсорбції застосовується переважно тоді, коли речовина, яка поглинається, перебуває у початковій суміші в малих кількостях і необхідно досягнути повного вилучення адсорбтиву з суміші.
У промисловості адсорбція застосовується для очищення розчинів, очищення та висушування газів, розділення сумішей газів або пари, зокрема для виділення летких розчинників з їх суміші з повітрям або з іншими газами (рекуперація летких розчинників) тощо. Наприклад, адсорбція застосовується для очищення мономерів у виробництві синтетичного каучуку, пластичних мас і смол, виділення ароматичних вуглеводнів з коксового газу. Переважно після адсорбції поглинуті речовини виділяють з поглинача.
Адсорбція є фізичною і хімічною. Фізична адсорбція зумовлена взаємним притяганням під дією сил Ван-дер-Ваальса молекул адсорбенту і адсорбату, і не супроводжується хімічною взаємодією останніх. За хімічної адсорбції (хемосорбції) в результаті хімічної реакції між молекулами поглинутої речовини і поверхневими молекулами поглинача виникає хімічний зв’язок.
Адсорбенти, їх характеристика. Адсорбентами є тверді речовини з великою питомою поверхнею відносно одиниці маси речовини. Вони відрізняються за діаметром капілярних каналів - пор, які умовно можуть поділятися на макропори (понад 2·10-4 мм), перехідні пори (6·10-6-2·10-4 мм) та мікропори (2·10-6-6·10-6 мм). Інтенсивність процесу адсорбції визначається розміром, кількістю та конфігурацією пор.
|
|
|
Розміри мікропор наближаються до розмірів адсорбованих молекул, і тому, внаслідок адсорбції в мікропорах, відбувається заповнення їх об’єму.
Адсорбенти характеризуються своєю поглинальною (адсорбційною) здатністю, яка визначається кількістю адсорбату в одиниці маси або об’єму адсорбенту. Адсорбційну здатність також називають активністю адсорбенту.
Поглинальна здатність адсорбенту щодо певної речовини залежить від температури і тиску, за яких відбувається адсорбція, і від концентрації речовини, яка поглинається. Максимально можливу за певних умов поглинальну здатність адсорбенту називають його рівноважною (статичною) активністю.
У промисловості як адсорбенти використовують переважно активоване вугілля, також мінеральні адсорбенти (силікагель, цеоліти тощо) або синтетичні іонообмінні смоли (іоніти).
Активоване вугілля. Високопористе активоване вугілля одержують під час сухої перегонки різних речовин, що містять вуглець (деревини, деревної тирси, костей та ін.) з подальшим активуванням одержаного вугілля для збільшення його пористості. Активування здійснюють прожарюванням вугілля за температури до 900 оС або видаленням з його пор смол та інших продуктів сухої перегонки їх екстрагуванням органічними розчинниками чи окисленням киснем повітря тощо. Для підвищення активності вугілля до нього перед обвуглюванням можна додавати активуючі речовини (розчини ZnCl2, лугів, кислот та ін.).
Застосування того чи іншого типу вугілля залежить від задачі, яка ставиться (поглинання газів, рекуперація летких розчинників та ін.). Переважно воно використовується для рекуперації летких розчинників. Активоване вугілля краще поглинає пару органічних речовин ніж води, однак із збільшенням їх вологості здатність поглинати пару органічних речовин знижується. До недоліків активованого вугілля належать його здатність до горіння та низька механічна міцність.
Силікагель.Силікагель одержують в результаті обробки рідкого скла (розчин силікату натрію) мінеральними кислотами або кислими розчинами їх солей і є продуктом зневоднення гелю кремнієвої кислоти. Питома поверхня силікагелю коливається в межах 440-770 м2/г, насипна густина може становити 100-800 кг/м3, розмір гранул - 0,2-7 мм.
|
|
|
Силікагель використовують переважно для висушування повітря та інших газів. Поглинаюча здатність силікагелю відносно парів органічних речовин за присутності вологи суттєво знижується. Порівняно з активованим вугіллям силікагелю властиві більша механічна міцність і повна негорючість.
Процеси адсорбції є періодичними та неперервними.
Періодичні процеси адсорбції відбуваються в адсорберах з нерухомим шаром адсорбенту. Такі адсорбери бувають трьох типів: вертикальні, горизонтальні та кільцеві.
Неперервні процеси адсорбції - в апаратах з рухомим шаром адсорбенту. Такі апарати поділяється на адсорбери, в яких адсорбент рухається самопливом зверху вниз, або транспортується спеціальними транспортними засобами (шнеками, елеваторами тощо) та адсорбери, в яких адсорбент знаходиться в псевдозрідженому (киплячому) стані.
У даному розділі будуть розглянуті принципи розрахунку адсорберів періодичної дії з нерухомим шаром адсорбенту та адсорберів неперервної дії з псевдозрідженим шаром адсорбенту.
6.1. Адсорбери періодичної дії з нерухомим шаром адсорбенту
Виходячи з вихідних даних (зазвичай задані витрата і склад вихідної суміші; умови, за яких відбувається адсорбція; гранично допустима концентрація адсорбтиву на виході з апарату), вибирають тип адсорберу та вид адсорбенту.
Складають принципову схему адсорбційної установки періодичної дії з нерухомим шаром адсорбенту [1,3,4,5].
Метою розрахунку адсорберів є визначення геометричних розмірів (діаметра та висоти) апарата, тривалості процесу, гідравлічного опору шару адсорбенту.
Розрахунок вертикальних та горизонтальних адсорберів
Розрахунок відбувається в наступній послідовності:
6.1.1.Швидкість газу і діаметр адсорбера
Діаметр адсорбера визначають за рівнянням витрати:
|
|
|
 (6.1)
(6.1)
де Vг – об’ємна витрата газоповітряної суміші, м3/с;
wг - фіктивна швидкість парогазової суміші, м/с
Для адсорберів з нерухомим шаром адсорбенту, згідно рекомендацій [1,4,5] вибирають фіктивну швидкість газу  .
.
Також фіктивна швидкість може бути розрахована за рівнянням [1]:
 (6.2.)
(6.2.)
де dч – середній діаметр зерна (частинки) адсорбенту, м;
 - насипна густина адсорбенту, кг/м3;
- насипна густина адсорбенту, кг/м3;
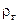 - густина газоповітряної суміші, кг/м3;
- густина газоповітряної суміші, кг/м3;
Середній діаметр частинок адсорбенту розраховують згідно залежності:
 (6.3)
(6.3)
де di – розмір і-ої фракції, м; сі – вміст і-ої фракції в частках одиниці (таблиця 6.4а, додаток 6)
6.1.2. Висота та об’єм шару адсорбенту
Висоту шару адсорбенту визначають за рівнянням:
 (6.4)
(6.4)
де Нш – висота шару адсорбенту, м;
hу - висота одиниці перенесення, м;
nу - число одиниць перенесення, м.
а) Визначення числа одиниць перенесення.
Число одиниць перенесення визначають за рівнянням

Для визначення  необхідно побудувати ізотерму адсорбції та робочу лінію процесу адсорбції (рис.6.1.).
необхідно побудувати ізотерму адсорбції та робочу лінію процесу адсорбції (рис.6.1.).
Позначення на рис.6.1.:
 та
та  – початкова та кінцева концентрація адсорбтиву в газовій суміші, кг/м3;
– початкова та кінцева концентрація адсорбтиву в газовій суміші, кг/м3;
 та
та  – початкова та кінцева концентрація адсорбату в твердій фазі, кг/м3.
– початкова та кінцева концентрація адсорбату в твердій фазі, кг/м3.
 та
та  – біжуча (робоча) концентрація відповідно адсорбату в твердій та адсорбтиву у газовій фазі, кг/м3;
– біжуча (робоча) концентрація відповідно адсорбату в твердій та адсорбтиву у газовій фазі, кг/м3;
 та
та  – рівноважна концентрація відповідно адсорбату в твердій та адсорбтиву у газовій фазі. За заданих
– рівноважна концентрація відповідно адсорбату в твердій та адсорбтиву у газовій фазі. За заданих  та
та 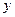 знаходяться відповідно до їх значень
знаходяться відповідно до їх значень  та
та  за рівноважною кривою), кг/м3.
за рівноважною кривою), кг/м3.
Ізотерму адсорбції будують згідно експериментальних або довідникових даних [1,4,5].
Існує декілька теорій побудови ізотерми адсорбції, зокрема це теорії об’ємного заповнення мікропор та потенціальна теорія Ейкена і Поляні – теорія, яка передбачає використання ізотерми адсорбції стандартної величини [1,4,5].
В даному посібнику використовується теорія Ейкена і Поляні, а саме, якщо ізотерма адсорбції невідома, її можна побудувати за ізотермою адсорбції стандартної речовини. За стандартну речовину зазвичай беруть бензол (таблиця 6.1, додаток 6)
Знаючи рівноважні концентрації бензолу (таблиця 6.1.додаток 6), знаходять рівноважні концентрації досліджуваної речовини (рівноважна концентрація відповідно адсорбату в твердій та адсорбтиву у газовій фазі) за наступними рівняннями:

Рис.6.1. Графічне зображення ізотерми адсорбції (1) та робочої лінії (2).
 (6.5)
(6.5)
де  - абсциса ізотерми стандартної речовини (зазвичай бензолу), кг/м3;
- абсциса ізотерми стандартної речовини (зазвичай бензолу), кг/м3;  - абсциса визначуваної ізотерми, кг/м3;
- абсциса визначуваної ізотерми, кг/м3;  і
і  - мольні об‘єми стандартної і досліджуваної речовин (в рідкому стані), м3/кмоль; β – коефіцієнт афінності, що дорівнює відношенню мольних об‘ємів
- мольні об‘єми стандартної і досліджуваної речовин (в рідкому стані), м3/кмоль; β – коефіцієнт афінності, що дорівнює відношенню мольних об‘ємів
 . (6.6)
. (6.6)
В таблиці. 6.3, додатку 6 наведено коефіцієнти афінності  для багатьох речовин.
для багатьох речовин.
Мольні об‘єми визначають за формулою:
 (6.7)
(6.7)
де Мi – мольна маса, кг/кмоль;  - густина рідини, кг/м3.
- густина рідини, кг/м3.
Рівновагу в газовій фазі розраховують за допомогою рівняння, яке зв’язує концентрації адсорбтиву в парогазовій суміші досліджуваної ( ) та стандартної (
) та стандартної ( ) речовини.
) речовини.
Для визначення величини 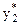 (необхідної для побудови ізотерми адсорбції досліджуваної речовини) застосовують рівняння:
(необхідної для побудови ізотерми адсорбції досліджуваної речовини) застосовують рівняння:
 (6.8)
(6.8)
Значення ун1 ун2 визначають з рівняння
 та
та  (6.9)
(6.9)
де Рs,1 – тиск насиченої пари стандартної речовини за температури Т1 (вираженої в К), мм рт. ст. або Па;
Рs,2 – тиск насиченої пари досліджуваної речовини за температури Т2 (вираженої в К), мм рт. ст. або Па. (тобто величини тисків повинні бути записані в однакових одиницях);
Т2 – температура, при якій відбувається адсорбція, К;
Т1 – температура, при якій відбувається адсорбція стандартної речовини (бензолу), К. Т1 = 20 0С (таблиця 6.1, додаток 6);
ун1 - концентрація парів бензолу в насиченій парі при температурі адсорбції, кг/м3;
ун2 - концентрація компонента (адсорбтиву) в парогазовій суміші в стані насичення, кг/м3;
М1 – мольна маса бензолу, кг/кмоль;
М2 – мольна маса досліджуваної речовини, кг/кмоль;
R – універсальна газова стала 8310 Дж/(кмоль·К).
Зауваження: в рівняннях (6.9) значення Рs,1 та Рs,2 вимірюються в Па. Тиск насиченої пари речовин визначають з таблиці 6.2 додатку 6.
Для побудови робочої лінії (лінія АВ, рис. 6.1.) визначають координати точок: точка А (хп, у к), точка В (хк, у п).
Значення хк визначають з рівняння матеріального балансу процесу:
Gадсорбату = V г · (у п - у к) = V ад · (хк – хп) (6.10)
де Vад – об’єм адсорбенту, що насичується адсорбатом в одиницю часу, м3/с;
Gадсорбату – кількість адсорбату, що поглинається адсорбентом в одиницю часу, кг/с.
Тобто рівняння матеріального балансу (6.10) використовується для визначення кількості речовин за одиницю часу.
Для визначення Vад використовують наступну залежність
 (6.11)
(6.11)
де k – коефіцієнт надлишку адсорбенту. Приймається в межах  [1,3,4,5].
[1,3,4,5].
В рівнянні (6.11)  визначають за ізотермою адсорбції (рис. 6.1.).
визначають за ізотермою адсорбції (рис. 6.1.).
Тоді  , що випливає з рівняння (6.10).
, що випливає з рівняння (6.10).
Точки А та В будують на графіку (рис. 6.1) та проводять пряму АВ – робочу лінію процесу.
Число одиниць перенесення визначають методом графічного інтегрування. Задаючись рядом значень 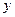 в інтервалі від
в інтервалі від  до
до  будують криву залежності
будують криву залежності  від
від  (рис. 6.2). Вимірюють площу, обмежену даною кривою і крайніми абсцисами, що відповідають
(рис. 6.2). Вимірюють площу, обмежену даною кривою і крайніми абсцисами, що відповідають  та
та  .
.
 |
Рис.6.2.Залежність

Після цього знаходять величину інтеграла з врахуванням масштабів М1 і М2, які виражають число одиниць в 1 мм на осі ординат і на осі абсцис графіка:
 . (6.12)
. (6.12)
Величину масштабів можна визначити з рівнянь:
 та
та 
де l1 – значення ординати  на графіку, кг/м3; h1 – значення цієї ординати в мм; l2 - значення абсциси у на графіку, кг/м3; h2 - значення цієї абсциси в мм.
на графіку, кг/м3; h1 – значення цієї ординати в мм; l2 - значення абсциси у на графіку, кг/м3; h2 - значення цієї абсциси в мм.
б) Визначення висоти одиниці перенесення.
Висоту одиниці перенесення h визначають з рівняння
 (6.13)
(6.13)
де Gг – масова витрата парогазової суміші, кг/с; Sш - площа перерізу шару, м2;  - об’ємний коефіцієнт масовіддачі в газовій суміші, 1/с;
- об’ємний коефіцієнт масовіддачі в газовій суміші, 1/с; 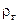 - густина парогазової суміші, кг/м3.
- густина парогазової суміші, кг/м3.
Об’ємний коефіцієнт масовіддачі визначають з дифузійного критерію Нуссельта (Nu/ )
 (6.14)
(6.14)
де dч – середній діаметр зерна адсорбенту, м; Dy - коефіцієнт молекулярної дифузії речовини в газовій фазі, м2/с (таблиця 6.5, додаток 6)
Критерій Нуссельта визначають в залежності від числового значення модифікованого критерію Рейнольдса
 (6.15)
(6.15)
 - динамічна в’язкість газу, Па·с;
- динамічна в’язкість газу, Па·с;  - пористість нерухомого шару адсорбенту, м3/м3
- пористість нерухомого шару адсорбенту, м3/м3
Зауваження: пористість нерухомого шару адсорбенту,  , м3/м3 знаходять за рівнянням
, м3/м3 знаходять за рівнянням  ; насипну та уявну густини вибирають з таблиці 6.4а додатку 6.
; насипну та уявну густини вибирають з таблиці 6.4а додатку 6.
За певних значень критерію Рейнольдса, критерій Нуссельта розраховують наступним чином:
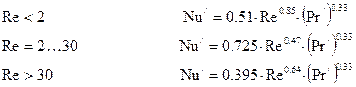 (6.16)
(6.16)
де Pr/ – дифузійний критерій Прандтля, який визначають за рівнянням
 (6.17)
(6.17)
в) Визначають об’єм шару адсорбенту, м3:
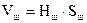 (6.18)
(6.18)
6.1.3. Тривалість адсорбції
Розраховують час поглинання адсорбтиву до проскоку  . Тобто тривалість процесу адсорбції.
. Тобто тривалість процесу адсорбції.
Тривалість адсорбції визначається за допомогою рівнянь, вигляд яких залежить від типу ізотерми адсорбції і діапазону зміни концентрацій адсорбтиву у газовій фазі в процесі адсорбції, тобто заданих початкової і кінцевої концентрації. Припустимо, що ізотерма адсорбції має вигляд, показаний на рис. 6.3.

Рис. 6.3. Графічне зображення ізотерми адсорбції.
Умовно її можна поділити на три ділянки: 1- залежність зміни концентрації адсорбтиву в газовій фазі від зміни його концентрації в твердій фазі прямолінійна (ізотерма адсорбції приблизно відповідає закону Генрі); 2 - криволінійна; 3 – автомодельна область, в межах якої кількість речовини, що поглинається адсорбентом досягає певної границі та залишається величиною сталою.
Тривалість адсорбції під час періодичного процесу визначається розв‘язком системи рівнянь, що містить рівняння балансу поглинутої речовини, рівняння кінетики адсорбції і рівняння ізотерми адсорбції.
Розв’язок системи таких рівнянь дає можливість отримати розрахункові залежності для визначення тривалості адсорбції. Таким чином, для розрахунку тривалості адсорбції потрібно побудувати ізотерму; визначити, в межах якої ділянки знаходяться задані початкова та кінцева концентрації адсорбтиву у газовій фазі, і вибрати відповідне рівняння.
а) для першої ділянки, де ізотерма адсорбції вважається прямолінійною і наближено відповідає закону Генрі, використовують рівняння:
 (6.19)
(6.19)
де  - тривалість адсорбції, с; wг – фіктивна швидкість парогазового потоку, м/с; Нш – висота шару активованого вугілля, м;
- тривалість адсорбції, с; wг – фіктивна швидкість парогазового потоку, м/с; Нш – висота шару активованого вугілля, м;  - початкова концентрація адсорбованої речовини (адсорбтиву) в парогазовому потоці, кг/м3;
- початкова концентрація адсорбованої речовини (адсорбтиву) в парогазовому потоці, кг/м3;  - кількість адсорбованої речовини (адсорбату) в твердій фазі, рівноважної з концентрацією потоку
- кількість адсорбованої речовини (адсорбату) в твердій фазі, рівноважної з концентрацією потоку  , кг/м3;
, кг/м3;  - об’ємний коефіцієнт масовіддачі, с-1.
- об’ємний коефіцієнт масовіддачі, с-1.
Значення коефіцієнта b приймають відповідно до значень  з табл. 6.1.
з табл. 6.1.
Таблиця 6.1.

| b | 
| b | 
| b |
| 0,005 | 1,84 | 0,01 | 1,67 | 0,03 | 1,35 |
| 0,05 | 1,19 | 0,1 | 0,94 | 0,2 | 0,63 |
| 0,3 | 0,42 | 0,4 | 0,23 | 0,5 | 0,09 |
| 0,6 | -0,10 | 0,7 | -0,27 | 0,8 | -0,46 |
| 0,9 | -0,68 |
б) Для другої ділянки ізотерми адсорбції використовують рівняння:
 , (6.20)
, (6.20)
де  ;
;  - вміст речовини в газовому потоці, що є рівноважним з половиною кількості від максимально адсорбованого заданим адсорбентом, тобто рівноважне з
- вміст речовини в газовому потоці, що є рівноважним з половиною кількості від максимально адсорбованого заданим адсорбентом, тобто рівноважне з  , кг/м3.
, кг/м3.
в) Для третьої ділянки ізотерми адсорбції, де кількість речовини, що поглинається адсорбентом, досягає границі та є величиною сталою:
 (6.21)
(6.21)
6.1.4. Матеріальний баланс по речовині, яка поглинається адсорбентом за час роботи адсорбера
Розраховують кількість газоповітряної суміші, що пройшла крізь адсорбер за час адсорбції та складають рівняння матеріального балансу за речовиною, яка адсорбується.
В періодичних процесах адсорбції необхідно знайти кількість газоповітряної суміші, кількість адсорбтиву та адсорбату який поглинувся протягом всього часу  до моменту проскоку.
до моменту проскоку.
Кількість газоповітряної суміші, що пройшла крізь адсорбер за час адсорбції, м3;
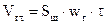 (6.22.)
(6.22.)
Кількість газоповітряної суміші, що пройшла крізь адсорбер за час адсорбції, кг
 (6.22а)
(6.22а)
Кількість адсорбтиву, який поступає в адсорбер, кг:
 (6.23.)
(6.23.)
Кількість адсорбату, який поглинається шаром вугілля (адсорбентом), кг:
 (6.24)
(6.24)
Кількість адсорбтиву, який виходить з апарату з газовою фазою, кг:
|
|
|
|
|
Дата добавления: 2017-02-01; Просмотров: 90; Нарушение авторских прав?; Мы поможем в написании вашей работы!