
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Можна показати, що 3 страница















 Н2О (вода) Hg (ртуть)
Н2О (вода) Hg (ртуть)
 |  | |||||||||||||||||||||||||||
 |  |  | ||||||||||||||||||||||||||
 |  | |||||||||||||||||||||||||||
 |  | |||||||||||||||||||||||||||
 |  |  | ||||||||||||||||||||||||||
 |  |  |  |  | ||||||||||||||||||||||||
 | ||||||||||||||||||||||||||||
 |  | |||||||||||||||||||||||||||
 |
Змiна рiвня рiдини h у капiлярах визначається формулою Жюрена:
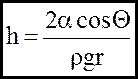 (4)
(4)
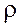 - густина рідини;
- густина рідини;
r - радіус капіляра;
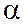 - коефіцієнт поверхневого натягу;
- коефіцієнт поверхневого натягу;
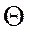 - крайовий кут змочування;
- крайовий кут змочування;
Лекція ХVІ
ТЕМА: ВЛАСТИВОСТІ РЕЧОВИН
В РІЗНИХ АГРЕГАТНИХ СТАНАХ
ПЛАН
1.Види кристалів. Аморфні тіла.
2.Анізотропія та ізотропія кристалів. Типи кристалів.
1.Тверді тіла зберігають об'єм та форму. Більшість твердих тіл мають правильну геометричну форму. Ці тіла називають кристалами.
Кути між гранями кристалів певної речовини однакові. В них молекули знаходяться в певному порядку та створюють кристалічну решітку. Розташування молекул має дальній порядок. Такі кристали називають моно к ристалами. Якщо зростається декілька кристалів, то утворюється полікристал.
Речовини, що за зовнішніми ознаками нагадують тверді тіла, але проявляють властивості рідин називають аморфними. Наприклад: смола, вар.
У них відсутня точка плавлення, при нагріванні.речовина переходить у рідкий стан поступово. Для молекул характерний ближній порядок, тобто відсутня строга періодичність їх розташування.
Анізотропія - це залежність фізичннх(механічиих, електричних, оптичних) властивостей речовини від напрямку.
Ізотропія — незалежність властивостей речовини від напрямку.
Анізотропія характерна для монокристалів, а ізотропія - для полікристалів та аморфних тіл.
В кристалах можуть виникати дефекти порушення порядку:
1.Порушення порядку молекул через тепловий рух;
2.Дислокація порушення будови решітки (див.мап.); 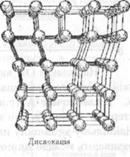
3.Вкраплення інородніх атомів;
4.Відсутність молекул у вузлах решітки.
Дефекти спричиняють зміну властивостей кристалів. Типи к ристалів:
1.Іонні (Наприклад: кухонна сіль).
2.Атомні (ковалентний зв'язок).
3.Молекулярні (наприклад: вода).
Лекція ХVІІ
ТЕМА: ТЕРМОДИНАМІКА
ПЛАН
1. Внутрiшня енергiя.
2. Теплота i робота.
3. Перший початок термодинамiки.
4. Теплоємнiсть багатоатомних газiв.
5. Адiабатичний процес. Рiвняння Пуассона.
1. Термодинамiка - це роздiл фiзики, який вивчає найбільш загальнi властивостi макросистем, якi знаходяться в рiвновазi, та процеси переходу мiж ними.
У статистичнiй фiзицi використовується молекулярно-кiнетичний метод дослiджень. Вiн установлює закони протiкання рiзних процессiв у макротiлах на основi вивчення їх молекулярної структури і механiзму взаємодiї окремих молекул.
Термодинамiка (термодинамiчний метод) - використовується для вивчення властивостей тiл без урахування їх внутрiшньої будови. Його основна мета - визначення стану термодинамiчної системи.
Термодинамiчна система - це сукупнiсть макротiл, якi взаємодiють та обмiнюються енергiєю мiж собою і зовнiшнiм середовищем.
Стан кожної термодинамiчної системи задається термодинамiчними параметрами.
Молекули газу можна розглядати як систему матеріальних точок, які здійснюють як поступальний, так і обертальний рух.
Кількість незалежних координат, які визначають положення молекул у просторі, називають кількістю ступенів вільності молекул.
Одноатомний газ (аргон,...): i = 3
Двоатомний газ (NО,CО,H2): i = 5
Триатомний газ та багатоатомний: і = 6 (3 поступальних та 3 обертальних степенів вільності).
Для поступального руху молекул ми знайшли, що
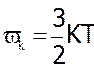 , а оскільки поступальному рухові завжди відповідає 3 степені вільності, то на кожний ступінь вільності припадає
, а оскільки поступальному рухові завжди відповідає 3 степені вільності, то на кожний ступінь вільності припадає  .
.
У цьому і є зміст закону рівномірного розподілу енергії за степенями вільності:
Статистично, в середньому, на кожний ступінь вільності молекули припадає енергія 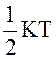
В однорідному багатоатомному газі кожна молекула має
і-ступенів вільності, тому кожна молекула володіє енергією:
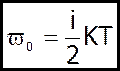 (5)
(5)
Кожна термодинамічна система характеризується повною енергiєю, в яку входять:
1) кінетична енергія механічного руху системи як цiлого у просторi або її макрочастинок;
2) потенціальна енергія, яка залежить вiд положення системи в зовнiшньому силовому полi;
3) внутрiшня енергiя U, яка залежить вiд внутрiшнього стану системи.
Внутрішня енергія мiстить у собi:
1) кінетичну енергію поступального та обертального руху молекул;
2) потенціальну енергію їх взаємодiї;
3) енергiю коливального руху молекул, електронних оболонок і ядер.
Слiд сказати, що внутрішня енергія є функцiєю параметрiвстану системи (перехiд системи з одного стану в iнший не залежить вiд способу переходу цiєї системи з одного стану в iнший).
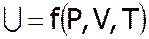 для даної маси.
для даної маси.
В iдеальному газi потенціальна енергія взаємодiї молекул дорiвнює 0. У термодинаміцi не враховується внутрiшньомолекулярна та внутрiшньоядерна енергiя, тому внутрішня енергія iдеального газу однозначно повинна дорiвнювати кінетичній енергії молекул.
Нам відомо, що для однієї молекули 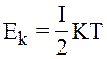 ;
;
а для одного моля 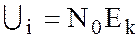 ;
;
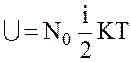 ;
; 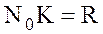 ;
;
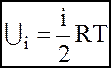 - внутрiшня енергiя одного моля iдеального газу.
- внутрiшня енергiя одного моля iдеального газу.
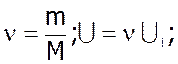
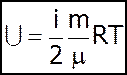 - внутрiшня енергiя iдеального газу.
- внутрiшня енергiя iдеального газу.
2. Змiна стану системи зумовлена передачею енергiї вiд одного тiла системи до iншого, а передача енергiї вiдбувається або у формi виконаної механічної роботи А, або у формi передачi теплоти Q.
Kiлькiсть теплоти Q - це фiзична величина, яка чисельно дорiвнює кiлькостi енергiї, що передається вiд одної системи до iншої внаслiдок теплообмiну.
Вiдомо, що теплота Q i робота А як двi форми передачi енергiї тiсно пов`язанi одна з одною.
Якщо А>0, то газ звершує роботу при розширеннi.
Якщо А<0, то робота звершується над газом, унаслiдок чого вiн стискується.
Розглянемо вираз для роботи для рiзних iзопроцеciв:
1). i зохоричний: V = const; ΔV = 0;
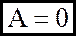
2). iзобаричний:
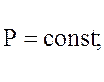 Q=ΔU+A - перший початок термодинаміки
Q=ΔU+A - перший початок термодинаміки
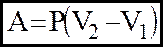
3). iзотермiчний: T=const
Q=AΔU=0
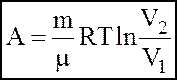
3. Перший початок термодинаміки зумовлює закон збереження та перетворення енергiї стосовно теплових процесiв i формулюється так:
Теплота Q, яка надається системi, при змiнi її стану витрачається на змiну її внутрішньої енергiї 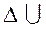 та на виконання цiєю системою роботи А проти зовнiшних сил.
та на виконання цiєю системою роботи А проти зовнiшних сил.
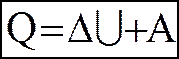 (3)
(3)
- перший початок термодинамiки.
Iснує iнше формулювання:
Неможливий вiчний двигун першого роду
Вiчним двiгуном першого роду називають перiодично дiючий двигун, який звершує роботу в кiлькостях бiльших, нiж енергiя, яка пiдводиться зовнi.
4. Для характеристики теплових властивостей тiл у термодинаміцi широко застосовують поняття теплоємностi:
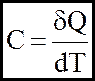 (4)
(4)
Теплоємнiсть - це величина, яка дорiвнює кiлькостi теплоти, що необхiдна для нагрiву тiла на 10.
Питома теплоємність - це величина, яка дорiвнює кiлькостi теплоти, яка необхiдна для нагрiвання одиницi маси тiла на 10.
А якщо нагрiвати 1 моль речовини 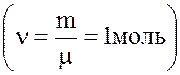 , то треба ввести поняття молярної теплоємностi "
, то треба ввести поняття молярної теплоємностi "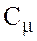 ":
":
 (5) де μ – молярна маса газа (кг/ моль).
(5) де μ – молярна маса газа (кг/ моль).
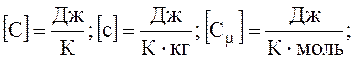
Залежно вiд умов нагрiву розрiзняють теплоємностi при сталому тиску та об'ємі.
Напишемо рiвняння Майера, яке показує, що молярна теплоємнiсть при сталому тискові більша, ніж молярна теплоємність при сталому об'ємі на величину унiверсальної газової сталої:
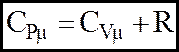 (6)
(6)
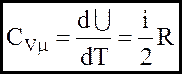 (7a)
(7a)
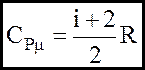 (7б)
(7б)
Формули (7) показують, що згiдно з основним положенням молекулярно-кінетичної теорiї молярнi теплоємностi незалежать вiд природи газу, а визначаються тiлькi числом ступенів вiльностi молекули.
А питомi теплоємностi з урахуванням (7) будуть мати вигляд:
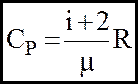 (8a)
(8a)
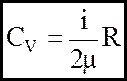 (8б)
(8б)
5. Процес, який проходить у газовi без теплообмiну iз зовнiшнiм середовищем, має назву адiабатичного (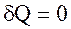 ).
).
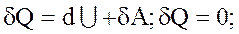 тоді:
тоді: 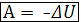 - із першого початку термодинамiки.
- із першого початку термодинамiки.
Фiзичний змiст:
Робота звершується за рахунок зменшення внутрiшньої енергiї системи.
Вiн описується рiвнянням Пуассона:
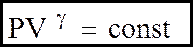 (9)
(9)
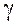 - показник адiабати;
- показник адiабати; 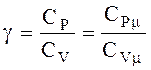 .
.
Лекція XVІІІ
ТЕМА: ОСНОВИ ТЕРМОДИНАМІКИ
ПЛАН
1. Оборотнi та необоротнi процеси.
2. Цикл Карно і його коефiцiєнт корисної дiї.
3. Другий початок термодинамiки.
1. Ранiше ми дали визначення термодинамiчного процесу взагалi.
Круговий процес (цикл) - це такий процес, при якому термодинамічна система, виходячи з початкового стану, проходить ряд промiжних i повертається знову в початковий стан.
Коловi процеси лежать в основi роботи всiх теплових двигунiв, тому вивчення властивостей рiзних колових процесiв - одне з наважливiших завдань термодинаміки.
Коловий процес оборотний, якщо пiсля його завершення система повертається у початковий стан разом з оточуючими її тiлами.
Необхiдною та достатньою умовою проходження цього процесу є його рiвноважнiсть, тому для оборотного процесу 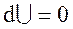 .
.
Процес, при якому система не повертається в початковий стан, називається необоротним.

 P
P
I
 |

 Q1
Q1
 |
 Q2
Q2
 II
II
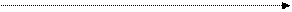 V
V
Нехай газ знаходиться у цилiндрi пiд поршнем у станi I (Р1,V1,T1). Надамо газу теплоту Q1. Вiн розшириться i перейде у стан II (P2,V2,T2). Якщо вiдвести (забрати) у системи теплоту Q2, то це буде означати, що зовнiшнi сили виконали роботу А=Q1-Q2 над системою, внаслiдок чого газ стиснеться i перейде у стан I. Тобто система буде виконувати роботу за рахунок придбаної та вiдданої кiлькостi теплоти.
Перiодично дiючий двигун, який виконує роботу за рахунок рiзницi придбаної та вiдданоє кiлькостi теплоти, називається тепловим двигуном.
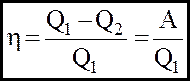 (12)
(12)
- коефiцiєнт корисної дiї теплового двигуна.
Якщо маємо проходження процесу по оборотному циклу, то слiд говорити про холодильну машину, для якої маємо:
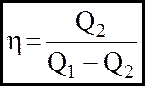 (13)
(13) 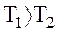
Характерною особливiстю її є те, що розширення газу вiдбувається при нижчiй температурі, нiж нагрiвання.
нагрівач Т1 нагрівач Т1
 |  | ||
Q1 Q1
 |
 A робоче A робоче
A робоче A робоче

 тіло тіло
тіло тіло
 | |||
 | |||
Q2 Q2
 | |||
 | |||
холодильник Т2 холодильник Т2
Робота виконується Робота виконується
газом над газом
2. Французький фiзик-iнженер Карно встановив, що максимальним ККД буде володiти iдеальна теплова машина, яка працює по замкненому циклу, котрий складається з двох адiабат та двох iзотерм.
Умова iдеальної теплової машини:
1) стiнки поршня теплоiзольованi (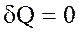 );
);
2) дно поршня - iдеальний провiдник теплоти (Т = const);
3) нехтуємо силами тертя 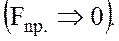 .
.
 P
P


 1
1
 2
2



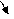 3
3
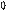
 4
4
 V
V
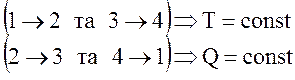
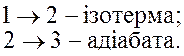
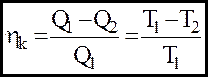 (14)
(14)
- формула Карно.
Т1,Т2 - абсолютнi температури нагрiвача та холодильника.
Iз (14) видно, що 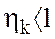 ; але взагалi
; але взагалi 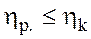 .
.
Iз (14) випливає незалежнiсть ККД Карно вiд природи робочого тiла.
3. Коли застосувати найзагальнiший закон збереження та перетворення енергiї стосовно теплових процесiв, то перший початок термодинамiки не дозволяє встановити напрямок їх протiкання. Це визначається другим початком термодинаміки.
Його формулювання:
І. Клаузiуса:
Неможливi такi процеси, єдиним i кiнцевим результатом яких був би перехiд теплоти вiд менш нагрiтого тiла до бiльш нагрiтого.
ІІ. Кельвiна:
Неможливий круговий процес, єдиним результатом якого є перетворення всiєї теплоти, одержаної вiд нагрiвача, в еквiвалентну їй роботу.
ІІІ.
Вiчний двiгун другого роду неможливий.
Тепловий двигун, який працює тiльки за рахунок охолодження теплового резервуара, називається вiчним двигуном другого роду.
Другий початок термодинаміки вказує на нерiвнозначнiсть двох форм передачi енергiї - теплоти та роботи.
Лекція XІХ
ТЕМА: ЕЛЕКТРОСТАТИКА
1. Електричний заряд, закон Кулона.
2. Напруженість електричного поля. Принцип суперпозиції.
1. Як відомо, в природі існують два види електричних зарядів:
а) позитивні “ +”,
б) негативні “ - ”.
Звичайно, однойменні заряди відштовхуються, а різнойменні притягуються. Найменшою за масою спокою частинкою, яка має негативний елементарний заряд, є електрон
е = 1,6 × 10-19 Кл;
me=9.1 ×10-31 кг
Електричний заряд тіл квантується, тобто приймає ряд дискретних значень (переривчастих).
q = ± ne (n = 1, 2, 3 …) (1)
Тіло приймає або віддає тільки величини зарядів, які кратні елементарному.
Експериментально було встановлено, що в ізольованій системі алгебраїчна сума зарядів зберігається
q 1+q2+q3+···+qп = соnst (2)
Алгебраїчна сума електричних зарядів тіл або частинок, які створюють електрично ізольовану систему, не змінюється при будь-яких процесах, які відбуваються в цій системі (фундаментальний закон природи).
Заряди взаємодіють. Закон цієї взаємодії був установлений у 1785 р. Кулоном: сила взаємодії двох точкових зарядів для однорідного, ізотропного та нескінченного середовища прямо пропорційна добутку величин цих зарядів і обернено пропорційна квадрату відстані між ними.
F= k× (q1 q2 / r2), (3)
k- коефіцієнт пропорційності, який залежить від вибору системи одиниць та від властивостей середовища.
Електричні властивості середовища характеризуються діелектричною проникністю e, яка показує, у скільки разів сила взаємодії зарядів у вакуумі F0 більша, ніж така ж сила F у середовищі на тій же відстані.
e = F0 / F (4)
Тому для однорідного, ізотропного та нескінченного середовища закон Кулона має вигляд:
F= k× (q1 q2 /ε r2);
(5)
Для вакууму e = 1; k = 9 ×109 Н×м2 / Кл2
| k = 1/ 4pe0; | e0 - електрична стала e0 = 8,85 × 10-12 Ф / м |
F = q1q2 /4pεe0r2
2. Оскільки заряджені тіла взаємодіють, то повинно існувати таке середовище, яке передає цю взаємодію.
Матеріальне середовище, оточуюче будь-яке нерухоме заряджене тіло, називається електростатичним полем.
Механізм взаємодії
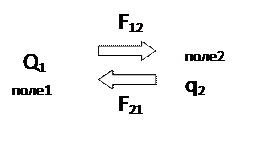
Поля не взаємодіють, а заряджене тіло створює навколо себе поле, яке діє на інше заряджене тіло із силою F.
Для будь-якої точки поля можна ввести його силову характеристику - напруженість, яка чисельно дорівнює силі F, діючій з боку електричного поля на одиничний позитивний точковий заряд, унесений до цієї точки поля:

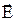 =
= 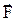 / q (6)
/ q (6)
З урахуванням (5) і (6) маємо:
EA = q /4pεe0r2; (7)
|
Дата добавления: 2014-01-04; Просмотров: 331; Нарушение авторских прав?; Мы поможем в написании вашей работы!