
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Абсолютная температура. Температурные шкалы
|
|
|
|
Согласно нулевому закону термодинамики, существует интенсивная функция состояния равновесной системы – температура (от латинского temperatura – надлежащее смешение, правильное соотношение частей, нормальное состояние).
Температура наряду с внешними параметрами определяет состояние термодинамического равновесия, поэтому все внутренние параметры равновесной системы являются функциями внешних параметров и температуры. В равновесных условиях температура пропорциональна средней кинетической энергии тела.
Температуру нельзя измерить непосредственно. Ее определяют по численным значениям других параметров, зависящих от температуры, что и положено в основу построения эмпирических (опытных) температурных шкал. Свойства, пригодные для определения температуры, называют термометрическими (объем, давление, электрическое сопротивление, скорость звука, ЭДС, интенсивность излучения и др.). В качестве реперных точек (эталон постоянной температуры) при построении температурных шкал используют температуры тройных точек и фазовых превращений чистых веществ.
Эмпирическая температурная шкала – это принятие определенных правил приписания численных значений температуры вещества в определенном состоянии. При этом пользуются тремя допущениями:
1). Размер градуса задается выбором численного значения величины ∆ t между двумя реперными точками t 1 – t 2.
2). Положение температурного нуля в эмпирических шкалах является произвольным.
3). Принимается, что термометрическая функция линейна в данном интервале температур.
Однако большинство термометрических функций нелинейны, поэтому термометры, показывающие одинаковую температуру в реперных точках (например, при 0 оС и 100 оС), могут показывать различные температуры внутри этого интервала.
|
|
|
Возможно неограниченное число эмпирических температурных шкал, различающихся по темометрическому свойству, принятой зависимости температуры t от термометрического свойства х и температурам фиксированных точек. Чаще всего эмпирические температурные шкалы различаются значениями t 1 и t 2, принятыми для одинаковых физических состояний. Так, в шкалах Цельсия (t, оС) (1701-1744), Реомюра (t, oR) (1683-1757), Фаренгейта (t, oF) (1686-1736) точке плавления льда и кипения воды при нормальном давлении приписываются разные температуры: t плавления льда – 0 оС, 0 oR, 32 oF соответственно; t кипения воды – 100 oC, 80 oR, 212 oF.
Соотношения для пересчета температуры из одной шкалы в другую имеют следующий вид:
t (oC) = 1,25 t (oR) = 5/9 [ t (oF) – 32)].
Объективную физическую температурную шкалу можно построить при использовании любой теоретически определенной термометрической функции, т.е. из термического уравнения состояния. С этой целью в термодинамике используют уравнение состояния идеального газа
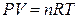 . (3.20)
. (3.20)
По известным значениям P, V, n легко вычислить Т для тех же условий. Однако реальные газы строго не описываются этим уравнением. Оно выполняется только при Р → 0, т.е. как предельное соотношение
 . (3.21)
. (3.21)
Экстраполяция к малым давлениям является сложной экспериментальной задачей. Поэтому определение температур по шкале газового термометра проводят для установления абсолютных температур только некоторых реперных точек, принимая их за эталонные. Промежуточные температуры определяют обычно эмпирическими методами.
Принципиальный недостаток эмпирических температурных шкал – их зависимость от термометрического свойства. Этот недостаток отсутствует у термодинамической температурной шкалы, основанной на втором законе термодинамики. Томсон (Кельвин) показал, что с точностью до масштабного множителя абсолютную температуру можно определить, не прибегая к свойствам идеального газа. Коэффициент полезного действия обратимого цикла Карно равен
|
|
|
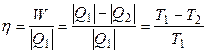 . (3.22)
. (3.22)
Уравнение (3.22) можно записать следующим образом:
 ,
,
 , (3.23)
, (3.23)
где ∆ Т = Т 1 – Т 2, | Q 1| и W – величины, определяемые на опыте и не зависящие от свойств рабочего тела.
Если ∆ Т цикла,проведенного при стандартном давлении между температурами кипящей воды и тающего льда, принять за 100, то абсолютная температура нагревателя окажется равной 373,15 К, и термодинамическая шкала температур (абсолютная шкала температур) совпадет со шкалой газового термометра. Таким образом, шкала газового термометра играет роль абсолютной шкалы температур.
Температура по термодинамической шкале температур измеряется в кельвинах (К). Единица температуры этой шкалы (К) совпадает с единицей температуры для стоградусной шкалы Цельсия, т.е. размер кельвина и градуса Цельсия одинаков: изменение температуры на 1 К эквивалентно изменению температуры на 1 оС, ∆ Т (К) = ∆ t (oC). Соотношение между температурами по шкалам Кельвина и Цельсия следующее:
T (K) = t (oC) + 273,15.
Дополнительное преимущество термодинамической (абсолютной) температурной шкалы состоит в том, что определенные по ней температуры входят в уравнения термодинамики, служащие основой всех теплофизических расчетов. Так, для обратимого процесса простой системы
 , а
, а 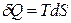 ,
,
поэтому
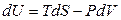 . (3.24)
. (3.24)
Последнее уравнение выражает объединенный первый и второй законы термодинамики и называется фундаментальным уравнением термодинамики. При постоянном объеме (V = const) из уравнения (3.24) получим
 (3.25)
(3.25)
Соотношение (3.25) является определением термодинамической температуры.
Термодинамическая температурная шкала является основной шкалой для измерения температур, однако измерение температур в этой шкале при помощи газового термометра доступно лишь для отдельных лабораторий. Измерение температуры для решения многих практических и научных задач потребовало построения практической шкалы, которая называется «Международной (практической) температурной шкалой» (МПТШ или МТШ).
Первая МТШ была принята в 1927 году, затем она уточнялась — в 1948 году (МПТШ-48), 1968 году (МПТШ-68), 1975 году (улучшенный вариант МПТШ-68) и, наконец, в 1989 году (МТШ-90). МТШ-27 содержала всего 6 реперных точек: нормальные точки кипения воды и затвердевания льда, нормальные точки кипения кислорода и серы, точки затвердевания серебра и золота, а МТШ-90 основывается на 17 реперных точках (причем первые четыре из упомянутых для МТШ-27 реперных точек уже не используются).
|
|
|
С 1954 года международные практические температурные шкалы как наиболее точное приближение к абсолютной температурной шкале строятся только на одной реперной точке с закрепленным постоянным значением температуры. В качестве такой точки используется температура тройной точки воды (равновесие лед – вода – пар при равновесном давлении водяного пара 611 Па). По шкале МПТШ температуре тройной точки воды приписано значение Т тр.т. = 273,1600 К (точно). Численное значение температур для всех других реперных точек непрерывно изменяется по мере повышения точности работы с газовыми термометрами.
В настоящее время действует Международная температурная шкала 1990 года (МТШ-90). Положение о ней было принято Международным комитетом по мерам и весам в 1989 г. в соответствии с решением XVIII Генеральной конференции по мерам и весам (1987 г.).
МТШ-90 устанавливает, что основной температурой является термодинамическая температура (Т), ее единицей служит Кельвин (символ К), определенный как 1/273.16 термодинамической температуры тройной точки воды. Международная температура в МТШ-90 может быть выражена в форме Международной температуры Кельвина (символ Т 90) или Международной температуры Цельсия (символ t 90). Соотношение между Т 90 и t 90 такое же, как и между термодинамическими температурами Т и t:
t 90, оС = Т 90, К – 273.15.
Интервалы температур могут быть выражены в кельвинах или градусах Цельсия.
Из-за перехода в 1954 году к новому определению термодинамической шкалы температура равновесия между жидкой водой и ее паром при давлении 1 атм не является более основной температурой. Если ранее это значение принималось равным 100 оС точно, то теперь эту температуру надо определять экспериментально, пользуясь значением Кельвина, приведенным выше. Результаты последних измерений свидетельствуют, что термодинамическая температура нормальной точки кипения воды равна 99,975 оС.
|
|
|
МТШ-90 построена таким образом, что полученные в ней значения температуры отличаются от термодинамических температур не более, чем погрешность определения последних. Нижняя граница МТШ-90 — температура 0.65 К. Верхнего предела она не имеет: он определяется практической возможностью проведения измерений на основе закона излучения Планка.
МТШ-90 базируется на 17 постоянных (реперных) точках, значения температур которых приведены в таблице 3.1.
Таблица 3.1. Реперные точки МТШ-90.
| № | Т 90, К | Вещество | Тип точки |
| от 3 до 5 | Не3 | V | |
| 13.8033 К | е -Н2 | T | |
| ~17 | е -Н2 (или Не3) | V (или G) | |
| ~20.3 | е -Н2 (или Не3) | V (или G) | |
| 24.5561 К | Ne | T | |
| 54.3584 К | О2 | T | |
| 83.8058 К | Ar | T | |
| 234.3156 К | Hg | T | |
| 273.1600 К | H2O | T | |
| 302.9146 К | Ga | M | |
| 429.7485 К | In | F | |
| 505.078 К | Sn | F | |
| 692.677 К | Zn | F | |
| 933.473 К | Al | F | |
| 1234.93 K | Ag | F | |
| 1337.33 K | Au | F | |
| 1357.77 K | Cu | F |
Примечание: Все вещества, кроме 3Не, естественного изотопного состава; е -Н2 — водород в равновесном составе модификаций орто- и пара-. Символы имеют следующие значения: V – давление насыщенного пара, Т – тройная точка (температура равновесия между твердой, жидкой и газообразной фазами), G – газовый термометр, М, F – температура плавления, температура затвердевания (температура равновесия жидкой и твердой фаз при 101325 Па).
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2274; Нарушение авторских прав?; Мы поможем в написании вашей работы!