
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Свойства бора и его соединений
Химия элементов IIIA группы
Химия р-элементов
В атомах р-элементов электроны заполняют р-подуровень внешнего уровня. В периодической системе есть 30 р-элементов. У атомов р-элементов, расположенных в главных подгруппах III - VIII групп. У р-элементов являются валентными не только р-, но и S-электроны внешнего уровня. Высшая степень окисления атомов р-элементов равна номеру группы.
Элементы IIIА группы имеют электронную формулу ns2np1. Они являются значительно менее активными восстановителями, чем щелочноземельные металлы. Для них характерна степень окисления +3, и валентность 3. При образовании ковалентной связи происходит s®p возбуждение электрона и sp2 гибридизация АО. В группе сверху вниз растут металлические свойства элементов, растут восстановительные свойства их атомов. Увеличиваются основные свойства гидроксидов и уменьшаются их кислотные свойства:
| Элементы | Оксиды | Гидроксиды | |||
| B | - неметалл | B2O3 | - кислотный | H3BO3 | - кислота |
| Al | - металл | Al2O3 | - амфотерный | Al(OH)3 | - амфотерный |
| Ga | - металл | Ga2O3 | - амфотерный | Ga(OH)3 | - амфотерный |
| In | - металл | In2O3 | - амфотерный | In(OH)3 | - амфотерный |
| Tl | - металл | Tl2O3 | - основной | Tl(OH)3 | - основание |
Соединения Tl3+ являются сильными окислителями и восстанавливаются до соединений Tl+.
Бор находится в природе в виде соединений, например, буры - Na2B4O7´10H2O. Бор является неметаллом. При нагревании взаимодействует с кислородом:
4B + 3O2 ® 2B2O3
Оксид бора является кислотным оксидом и растворяется в воде с образованием слабой ортоборной кислоты:
B2O3 + 3H2O ® 2H3BO3 (К1 = 6×10-10)
Ортоборная кислота H3BO3 при нагревании последовательно разлагается до метаборной кислоты HBO2, тетраборной кислоты H2B4O7 и борного ангидрида B2O3.
H3BO3  HBO2
HBO2  H2B4O7
H2B4O7  B2O3
B2O3
Ортоборная кислота H3BO3 взаимодействует с щелочами и образует соли тетраборной кислоты:
4H3BO3 + 2NaOH ® Na2B4O7 + 7H2O
Сильные кислоты при взаимодействии с тетраборатом натрия вытесняют слабую ортоборную кислоту:
Na2B4O7 + H2SO4 + 5H2O ® Na2SO4 + 4H3BO3
Ортоборная кислота взаимодействует с этанолом в присутствии концентрированной серной кислоты с образованием борно-этилового эфира, который горит зеленым пламенем.
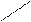
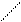 O¾H O¾C2H5
O¾H O¾C2H5



 B O¾H + 3HOC2H5 ® B O¾C2H5 + 3H2O
B O¾H + 3HOC2H5 ® B O¾C2H5 + 3H2O
O¾H O¾C2H5
Бор является микроэлементом. Микроэлементы (или микроудобрения) - это соединения B, Cu, Mn, Co, Mo и др. Они повышают активность ферментов, катализируют биохимические процессы, способствуют синтезу белков и нуклеиновых кислот, витаминов, сахаров и крахмала, влияют на фотосинтез, ускоряют рост растений и созревание семян. Соединения бора влияют на углеводный обмен и необходимы для нормального роста и образования семян.
|
|
Дата добавления: 2014-01-04; Просмотров: 519; Нарушение авторских прав?; Мы поможем в написании вашей работы!