
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Виявлення NO3–-іонів
|
|
|
|
28. Реакція з дифеніламіном. Дифеніламін (C6H5)2NH у сильнокислому середовищі з NO3– -іонами утворює сполуку інтенсивно-синього кольору, яка при подальшому окисненні переходить у сполуку білого кольору:
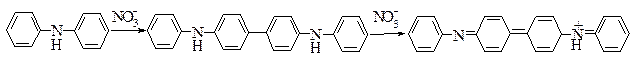
Реакція з дифеніламіном застосовується також для виявлення MnО4– та NO2–-іонів. Чутливість реакції 0,5 мкг.
Виконання реакції. У пробірку вносять кілька крапель розчину натрій нітрату і по стінках пробірки краплями добавляють розчин дифеніламіну. За наявності в розчині аніонів NO3– на стінках пробірки утворюється сполука синього кольору. При збовтуванні розчину синє забарвлення зникає внаслідок подальшого окиснення дифеніламіну.
29. Реакція відновлення. При відновленні NO3–-іонів алюмінієм або цинком утворюється аміак, який виявляється вологим лакмусовим папером:
3NaNO3 + 8Al + 5NaOH + 2H2O ® 3NH3 + 8NaAlO2
FeSO4 відновлює NO3–-іони до NO (при рН < 7):
2NaNO3 + 6FeSO4 + 4H2SO4 ® 3Fe2(SO4)3 + Na2SO4 + 2NO + 4H2O
Нітроген (ІІ) оксид утворює з FeSO4 комплексну сполуку бурого кольору:
FeSO4 + NO ® [Fe(NO)]SO4
Чутливість – 2,5 мкг.
Виконання реакції. До 2-3 крапель свіжоприготованого розчину FeSО4 добавляють 2 краплі розчину натрій нітрату й охолоджують пробірку під водою. Обережно, по стінці, добавляють 2-3 краплі концентрованої H2SО4. На межі дотику рідин утворюється буре кільце.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 848; Нарушение авторских прав?; Мы поможем в написании вашей работы!