
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Визначення швидкості початку псевдозрідження
|
|
|
|
Найбільш надійно швидкість початку псевдозрідження WПС визначається експериментальне на лабораторних або дослідних установках. Розрахунковим шляхом WПС знаходять наступним чином. Для частинок шароподібної або близької до неї форми критичне значення критерія Рейнольдса (Rеопс ), при котрому починається псевдозрідження, можна визначити по наступному рівнянню:
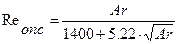 (6.4.1)
(6.4.1)
В критерій Архімеда входять всі відомі величини.
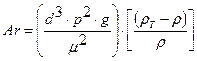
Тоді, визначивши за рівнянням (6.4.1).
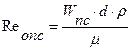
знаходять відому швидкість Wпс .. Знаючи її можна знайти робочу швидкість W0 потоку, а по ній визначають діаметр апарату, використовуючи рівняння:
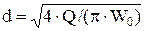 ,
,
де – Wо = kn*Wnc,
kn – число псевдозрідження.
Рівняння для визначення швидкості початку псевдозрідження має вигляд:
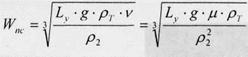 (6.4.2)
(6.4.2)
Для визначення висоти псевдозрідженого шару використовують рівняння:
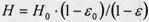 (6.4.3)
(6.4.3)
попередньо визначивши пористість ε за рівнянням:
 (6.4.4)
(6.4.4)
7. Масообмін через напівпроникні перетинки (мембрани)
Процеси розділення рідких систем відіграють важливу роль практично в усіх сферах людської діяльності. Для здійснення цих процесів давно використовують такі способи, як перегонку і ректифікацію, абсорбцію та адсорбцію, екстракцію та ряд інших фізико - хімічних, хімічних, фізичних і механічних методів. Широко застосовуваним методом розділення є розділення з використанням напівпроникних мембран (мембранні методи). Мембранні методи розділення сумішей використовуються в хімічній і нафтохімічній промисловості, в біотехнології і медичній та харчовій промисловостях, Найбільш широко використовують мембранні процеси при обробці води і водних розчинів, очистці стічних вод.
До основних мембранних процесів, що нині успішно використовуються для розділення рідких систем належать: зворотній осмос, нанофільтрування, ультрафільтрування мікрофільтрування, діаліз, електродіаліз, випаровування через мембрану та ін.
|
|
|
7.1. Найважливіші мембранні методи та межі їх застосування.
Зворотній осмос - це процес фільтрування розчинів під тиском крізь напівпроникні мембрани, які пропускають розчинник і повністю або частково затримують молекули чи йони розчинених речовин. В основі цього мембранного процесу лежить явище осмосу - самовільного проникнення розчинника крізь напівпроникну мембрану в розчин (рис.7.1.1.,а)

Рис.7.1.1. Схема виникнення зворотного осмосу; а - осмос; б - рівновага; в - зворотній осмос.
Гідростатичний тиск, за якого встановлюється динамічна рівновага потоку розчинника крізь мембрану, відповідає осмотичному тиску розчину даної концентрації (рис.7.1.1.,б).
Якщо з боку розчину прикласти тиск, який перевищує осмотичний (рис.7.1.1.,в) то розчинник буде переноситись у зворотному напрямку, що відображено в назві процесу - зворотний осмос. Рушійною силою процесу є різниця робочих тисків з обох боків мембрани.
Ультрафільтрування - це процес баромембранного розділення, а також концентрування і фракціонування розчинів високомолекулярних сполук. Він здійснюється за рахунок різниці тисків з обох боків мембрани. Залежно від цілей ультрафільтрувального процесу мембрани пропускають:
- розчинник і переважно (або тільки) низькомолекулярні сполуки (розділення високо-і низькомолекулярних сполук і концентрування високомолекулярних сполук);
- розчини і фракції високомолекулярних сполук з певними молекулярною масою чи розміром макромолекулярних клубків (фракціонування полімерних сполук). Ультрафільтрування, на відміну від зворотного осмосу, застосовують для розділення систем, в яких молекулярна маса розчинених компонентів набагато більша за молекулярну масу розчинника. На практиці ультрафільтрування використовують тоді, коли хоча б один з компонентів розчину має молекулярну масу понад 500 дальтон.
|
|
|
Рушійною силою процесу ультрафільтрування є різниця тисків з обох боків мембрани.
Нанофільтрування - це баромембранний процес розділення речовин (за робочих тисків 1 - 2 МПа) з молекулярними масами до 300 - 500 дальтон. У процесі нанофільтрування частково затримуються низькомолекулярні електроліти і практично повністю органічні сполуки.
Застосовують при водоочищенні природних і стічних вод, в фармацевтичній промисловості і біотехнології.
Мікрофільтрування - це баромембранний процес, який застосовують для відокремлення від розчинника завислих та колоїдних частинок розміром 0,1 - 10 мкм. Рушійною силою процесу є різниця тисків з обох боків мембрани, яка становить 0,01 - 0,05 МПа.
Діаліз - це мембранний процес, рушійною силою якого є градієнт концентрації розчинених речовин з обох боків мембрани. Діаліз відбувається з використанням непористих (дифузійних) мембран і застосовується для розділення речовин, що значно відрізняються за молекулярною масою. Недоліком методу є його низька продуктивність і великі об'єми розчинника. Діаліз раціонально використовувати в технологічних процесах після ультра - або мікрофільтрувального концентрування розчинів високомолекулярних сполук чи колоїдів.
Первапарація - це мембранний процес, який відбувається з використанням непористих мембран для вилучення з води невеликих домішок органічних речовин (спиртів, ацетону, бензолу, толуолу тощо), або для видалення домішок води з цих речовин. Необхідною умовою первапараційного розділення є здатність полімерної мембрани набрякати в речовинах, що є домішками. Рушійною силою процесу первапарації є різниця парціальних тисків пари або градієнт концентрації розчиненої речовини з обох боків мембрани, які створюються за рахунок різниці температур або тисків.
Випаровування через мембрану - це процес пропускання певних компонентів через мембрану, коли розчин, що розділяється контактує з мембраною з однієї сторони, а компонент, що дифундує у вигляді пари відводиться з іншої сторони мембрани за допомогою вакууму або потоку інертного газу.
|
|
|
Дифузійне розділення газів - базується на відмінності коефіцієнтів дифузії в непористих полімерних мембранах і здійснюється під дією градієнта концентрацій у відповідності з законами молекулярної дифузії.
У будь-якому з перелічених мембранних процесів розчин, що підлягає розділенню, обов'язково контактує з напівпроникною мембраною з одного її боку. Внаслідок напівпроникності мембрани розчин, що проходить крізь неї, збагачується на один із компонентів. Часом процес відбувається настільки ефективно, що отриманий фільтрат практично не містить домішок. Водночас, використовуючи той чи інший мембранний процес, можна отримати в розчині над мембраною концентрат без домішок речовин, здатних проникати крізь мембрану.
Рушійною силою мембранних процесів є градієнт хімічного (для незаряджених частинок потоку) або електрохімічного (для заряджених частинок потоку) потенціалу. Для технічних розрахунків таких процесів за рушійну силу приймають градієнт фактора, який визначає швидкість даного процесу. Таким чином основною рушійною силою мембранного процесу може бути градієнт тисків - баромембранні процеси (зворотній осмос, нано-, ультра- і мікрофільтрація); градієнт концентрацій - дифузійно - мембранні процеси (діаліз, випаровування через мембрану, мембранне розділення газів та ін.); градієнт електричного потенціалу - електромембранні процеси (електродіаліз, електроосмос та ін.); градієнт температур - термомембранні процеси (мембранна дистиляція та ін.). В деяких мембранних процесах можливо існування двох і навіть трьох рушійних сил.
7.2 Функціональні характеристики мембран.
Зазначимо, що продукт, який пройшов через мембрану прийнято називати пермеатом, а розділяючу суміш залишилась перед мембраною - ретантом (інколи концентратом).
Найважливішими функціональними характеристиками будь-яких мембран є коефіцієнт затримування (селективності) розчиненої речовини φ (в %)
 (7.2.1)
(7.2.1)
де с1 і с2 - концентрація речовини в вихідній суміші та перміаті відповідно, та питома продуктивність (об'ємний потік) крізь мембрану.
|
|
|
 (7.2.2)
(7.2.2)
G виражається об'ємом (або масою) перміату V, що отримується при даній рушійній силі в одиницю часу τ одиниці робочої поверхні F мембрани.
Обидві ці функціональні характеристики не є константами напівпроникних мембран, оскільки значною мірою залежать ввід зовнішніх умов проведення процесу розділення (тиску, температури, концентрації, гідродинамічних умов, тощо). Тому часто для характеристики функціональних властивостей мембран, що застосовуються в баромембранних процесах, використовують ще два показники:
Коефіцієнт фільтрування який дорівнює об'ємному потоку, нормованому за градієнтом тиску Δ р:
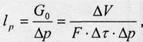 (7.2.3)
(7.2.3)
та коефіцієнтом відбиття мембрани (коефіцієнтом Ставермана)
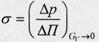 (7.2.4)
(7.2.4)
який дорівнює нулю для повністю проникної для даної розчиненої речовини мембрани та одиниці - для ідеально напівпроникної мембрани. В рівнянні (7.2.4)
ΔП - різниця осмотичних тисків розчину з обох боків мембрани. Коефіцієнт відбиття мембрани характеризує її властивості без урахування умов використання мембрани. Однак на нього справляє значний вплив анізотропність внутрішньої будови мембрани (градієнт діаметра пор у перерізі мембрани), що значно ускладнює визначення "істинного" значення цього показника.
7.3 Кінетика процесів мембранного розділення сумішей.
Механізм переносу атомів, молекул або іонів різних речовин через напівпроникні мембрани може бути пояснений однією з розглянених нижче теорій.
Теорія просіювання припускає, що в напівпроникній мембрані існують пори, розміри котрих достатні для того, щоб пропускати розчини, але досить малі для того, аби пропускати молекули або іони розчинених речовин.
Теорія молекулярної дифузії базується на неоднаковій розчинності і на різниці коефіцієнтів дифузії розділяючих компонентів в полімерних мембранах.
Теорія капілярно - фільтраційної проникності базується на різниці фізико - хімічних властивостей граничного шару рідини на поверхні мембрани і розчину в об'ємі. Так граничний шар рідини має упорядковану структуру, відрізняється складом і, отже, в'язкістю, розчинною здатністю та ін.
 На поверхні і всередині пор (капілярів) мембрани, що занурена в розчин електроліту виникає граничний шар зв'язаної води, як показано на (Рис. 7.3.1.) Цей шар води утворює плівку товщиною δ. Зв'язана в граничному шарі вода втрачає розчинну здатність по відношенню до розчинених в об'ємі солей.
На поверхні і всередині пор (капілярів) мембрани, що занурена в розчин електроліту виникає граничний шар зв'язаної води, як показано на (Рис. 7.3.1.) Цей шар води утворює плівку товщиною δ. Зв'язана в граничному шарі вода втрачає розчинну здатність по відношенню до розчинених в об'ємі солей.
Рис. 7.3.1. До пояснення механізму напівпроникності мембран з високою (а) і низькою (б) селективністю.
Тому під дією перепаду тиску ця вода з з граничного шару перетікає по капілярам через мембрану, якщо розмір капілярів в мембрані менше розмірів гідратованих іонів солі (менше 20/Α), як це схематично показано на (Рис. 7.3.1.,а) Але реальні мембрани мають пори різного розміру, в тому числі і крупні (більше 20 Α), тому частина гідратованих іонів солі може проникнути через ці крупні капіляри, як показано на (Рис. 7.3.1..б). Отже, селективність мембрани тим вище,чим більше розміри гідратованих іонів солі.
На базі розглянутої теорії можна зробити висновок, що знесилювання водних розчинів електролітів зворотнім осмосом є дегідратація іонів, тобто відбір води, найменш міцно зв'язаної з з поверхнею мембрани і з іонами солей під дією прикладеного зовні тиску.
8. Основи масопереносу
8.1 Загальні відомості про масообмінні процеси
Технологічні процеси, швидкість проходження котрих визначається швидкістю переносу речовини (маси) з однієї фази в іншу, називають масообмінними процесами, а апарати, які призначені для проведення цих процесів, - масообмінними апаратами.
В розділяючому агрегаті можуть проводитись різні процеси. Основними і найважливішими з них є абсорбція, ректифікація, екстракція, кристалізація, адсорбція, сушка, іонообмінні процеси і мембранне розділення. Крім перерахованих основних процесів розділення слід зазначити і такі, як термодифузія, зонна плавка та ін.
Для всіх перелічених процесів загальним є перехід речовини з однієї фази в іншу, або масопередача.
Масопередачею називають перехід речовини з однієї фази в іншу в напрямку досягання рівноваги.
В масообміні в більшості випадків приймають участь три речовини: розподіляюча речовина (або речовини), що складає першу фазу; розподіляюча речовина (або речовини), яка складає другу фазу; розподіляюча речовина (або речовини), котрі переходять з однієї фази в другу.
При переносі речовини з однієї фази в іншу змінюється концентрація. Так як концентрація пропорційна числу частинок, то, отже, швидкість переходу розподіляючої речовини з однієї фази в іншу пропорційна різниці між фактичною концентрацією розподіляючої речовини в даній фазі і рівноважній концентрацією.
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1035; Нарушение авторских прав?; Мы поможем в написании вашей работы!