
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гальваническим наращиванием
|
|
|
|
ВОССТАНОВЛЕНИЕ ПОВЕРХНОСТЕЙ
Гальваническое наращивание металла на поверхность детали основано на процессе электролиза. Под действием постоянного электрического тока, поступающего в электролит через проводники-электроды, положительно заряженные ионы (катионы) движутся к катоду, а отрицательно заряженные ионы (анионы) - к аноду (рис. 10.14).
При достижении катода положительными ионами и анода отрицательными образуются нейтральные атомы. В результате на катоде, в качестве которого используется ремонтируемая деталь, выделяются металл и водород, а на аноде - кислотные и водные остатки. Электролиз металлов может осуществляться с растворимыми и нерастворимыми анодами. Растворимые аноды изготовляют из железа Армко, меди или никеля в зависимости от вида электролитического процесса; нерастворимые - из свинца, платины и других металлов. При электролизе с нерастворимыми анодами пополнение электролита ионами металла осуществляется за счет добавления в электролит вещества, содержащего ионы осаждаемого металла.
Теоретическое количество вещества, выделяющегося при электролизе на катоде, согласно закону Фарадея определяется по формуле
GT = CIТ,
где GT - количество вещества, осаждаемого на катоде, г; С - электрохимический эквивалент, г/(А·ч); I - сила тока, А; Т - время протекания электрического тока через электролит, ч.
Фактическая масса осажденного металла G ф всегда меньше теоретической, так как в электролите одновременно протекают другие процессы, на что расходуется часть энергии.
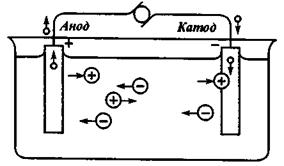
Рис. 10.14. Схема процесса электролиза
При электроосаждении металлов, стоящих в ряду напряжений выше водорода, одновременно с ними происходит выделение водорода, который в большинстве случаев ухудшает качество покрытий, придавая им хрупкость, и увеличивает продолжительность электролиза, так как часть электрической энергии расходуется на его выделение.
|
|
|
Отношение фактической массы осажденного металла к теоретической называется выходом по току и характеризует коэффициент полезного действия ванны:
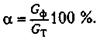
При хромировании выход по току составляет 12 - 18 %, для других процессов гальванического наращивания – 60 - 90 %.
Среднюю толщину слоя металла, осажденного на катоде, определяют по формуле
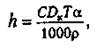
где h - средняя толщина слоя, мм; DK = I/F - плотность тока, А/дм2; F - площадь покрываемой поверхности детали, дм2; α -выход по току, %; ρ - плотность осаждаемого металла, г/см3.
Электрохимические эквиваленты для некоторых металлов приведены в табл. 10.2.
Таблица 10.2
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 724; Нарушение авторских прав?; Мы поможем в написании вашей работы!