
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Коллигативные свойства растворов
|
|
|
|
Разделение жидких летучих смесей.
Различие составов жидкости и равновесного с нею пара имеет большое практическое значение, так как позволяет разделять летучую смесь на практически чистые компоненты. Основными методами разделения жидких летучих смесей является перегонка и ректификация. Эти методы основаны на испарении летучей смеси и конденсации образовавшегося пара.
Различают простую и фракционную перегонку или ректификацию. При простой перегонке нагревание жидкости сопровождается непрерывным отбором пара и его конденсацией. В результате простой перегонки можно выделить практически в чистом виде только один из компонентов (менее летучий компонент). Более летучий компонент при простой перегонке в чистом виде не выделяется.
Фракционная перегонка заключается в многократном повторении процессов испарения и конденсации и позволяет разделить раствор на чистые компоненты. На производстве фракционная перегонка осуществляется непрерывно и называется ректификацией.
Основными законами перегонки и ректификации являются законы Коновалова.
Первый закон Коновалова: пар по сравнению с жидкостью обогащен тем компонентом, добавление которого к бинарной смеси увеличивает общее давление пара при данной температуре или понижает температуру кипения при данном давлении.
Из первого закона Коновалова следует, что пар по сравнению с жидкостью обогащается более летучим компонентом. Таким образом, путем многократного испарения жидкости и конденсации пара можно добиться практически полного разделения компонентов.
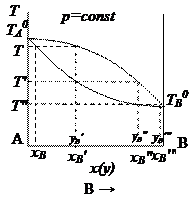
|
|
|
|
Компонент В является более летучим по сравнению с компонентом А, так как его температура кипения ниже. Согласно диаграмме данный раствор закипит при температуре Т и появится пар, состав которого равен уВ′. Сконденсировав образовавшийся пар, получим жидкую смесь, мольная доля компонента В в которой составит хВ′, причем хВ′ > xB. Если снова нагреть полученную смесь, то получим пар состава уВ″, при конденсации которого образуется жидкая смесь такого же состава хВ″ > хВ′. Повторяя указанные действия, получим практически чистые компоненты А и В (хВ′″ ≈ 100 %).
Для реальных растворов, характеризующихся значительными положительными или отрицательными отклонениями, компоненты которых имеют очень близкие температуры кипения или давления насыщенных паров, на кривых жидкости и пара наблюдаются точки экстремума.
Второй закон Коновалова: точкам экстремума на кривой зависимости общего давления пара от состава раствора (температуры кипения раствора от состава раствора) соответствуют азеотропные нераздельно кипящие смеси, в которых состав жидкости и состав равновесного с нею пара одинаковы.
Диаграммы состояния таких растворов представлены на рис. 2.5.
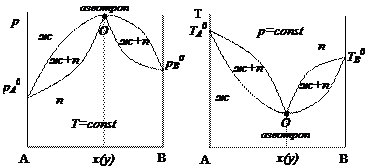
Рис. 2.5. Диаграммы р – х2(у2) и t – х2(у2) с азеотропом
в минимуме давления (максимуме температуры кипения)
Примером смеси, образующей азеотроп, является бражка, основными компонентами которой являются этиловый спирт и вода. При концентрации этилового спирта, равной 96 % об. образуется азеотропная смесь. Поэтому путем обычной ректификации получить 100 %-го этиловый спирт нельзя.
На практике для устранения азеотропа предпринимают различные меры, например, повышают внешнее давление, в результате увеличивается температура кипения смеси и азеотроп исчезает или изменяется его состав.
Коллигативными называются физико-химические свойства разбавленных растворов, не зависящие от природы растворенного вещества и определяющиеся только его концентрацией и природой растворителя. К таким свойствам относятся: понижение давления пара над раствором по сравнению с чистым растворителем, понижение температуры замерзания и повышение температуры кипения раствора по сравнению с чистым растворителем, осмотическое давление.
|
|
|
|
|
|
|
|
Дата добавления: 2013-12-11; Просмотров: 425; Нарушение авторских прав?; Мы поможем в написании вашей работы!