
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Образование дисперсной фазы при кристаллизации металла
|
|
|
|
При охлаждении расплавленного металла ниже температуры кристаллизации Ткр в нем образуются мельчайшие частички твердой фазы (центры кристаллизации). С термодинамической точки зрения при Ткр свободные энергии жидкой и твердой фаз равны. При Т < Ткр наиболее стабильной является твердая фаза, как обладающая меньшей энергией. Образование поверхности раздела при образовании твердой фазы ведет к затрате энергии, что вызывает некоторое увеличение свободной энергии системы, чем объясняется необходимость наличия некоторого переохлаждения жидкости.
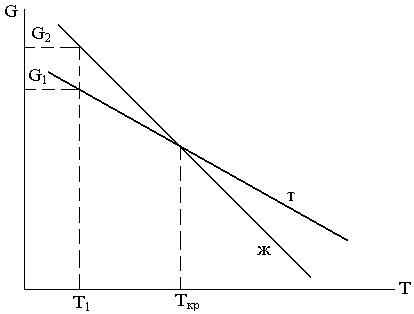
Рис. 3. Зависимость свободной энергии чистого металла от температуры
При переохлаждении до температуры Т 1 (рис. 3) образование сферического зародыша приводит к изменению свободной энергии на
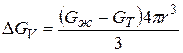 . (1.40)
. (1.40)
Поскольку величина свободной энергии G связана с энтальпией i и энтропией S соотношением G= i-Т S, разность свободных энергий жидкой и твердой фаз
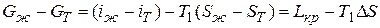 , (1.41)
, (1.41)
где Lкр – скрытая теплота кристаллизации (Lкр = iж- iТ).
Величину D S можно найти из выражения (41), учитывая, что при 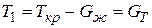 и
и 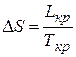 . С учетом полученного соотношения, из (1.40), принимая во внимание (41)
. С учетом полученного соотношения, из (1.40), принимая во внимание (41)
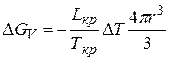 ,
,
где D Т=Т1–Ткр – величина переохлаждения.
Следует считать, что образование границы раздела фаз ведет к затрате энергии 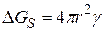 , где g – удельная поверхностная энергия.
, где g – удельная поверхностная энергия.
Общее изменение свободной энергии при образовании зародыша твердой фазы 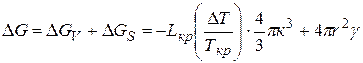 графически представлено на рис. 4.
графически представлено на рис. 4.
Образование зародыша твердой фазы радиусом rmin имеет место при максимальном значении величины D G. Значение rmin можно найти дифференциальное выражение (40) по dr и приравнивая производную к нулю
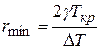 . (1.42)
. (1.42)
Любой зародыш с r < rmin является центром кристаллизации, способным к росту, поскольку это ведет к уменьшению свободной энергии системы. При r < rmin зародыш имеет тенденцию к исчезновению. В сплавах переохлаждение может быть вызвано как изменением температуры (термическое переохлаждение), так и изменение его состава (концентрационное переохлаждение).
|
|
|
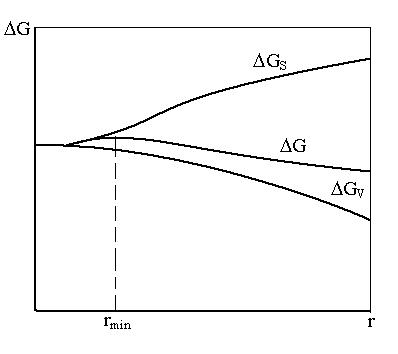
Рис. 4. Зависимость объемной (D GV), поверхностной (D G S) и общей (D G) свободных энергий от радиуса зародыша
При неравновесных условиях затвердевания состав образующейся твердой фазы отличается от состава жидкой фазы. Если, например, концентрация примеси в твердой фазе меньше, чем в жидкой, то примесь будет скапливаться в жидкости перед фронтом кристаллизации. Образующийся градиент концентрации сохраняется в процессе кристаллизации и является причиной концентрационного переохлаждения, в значительной степени определяя структуру кристаллизующегося сплава.
Рассмотрим пути возникновения концентрационного переохлаждения на примере кристаллизации бинарного сплава для случая kо <1 (kо – коэффициент распределения, равный отношению концентраций примеси в твердой и жидкой фазах). Для упрощения сделали следующие допущения: kо = const (линии ликвидус и солидус являются прямыми линиями (рис. 4)), диффузия примеси в твердой фазе отсутствует; перемешивание жидкости происходит вследствие диффузии; на фронте кристаллизации имеет место равновесие концентраций примесей. Последнее допущение означает, что если на фронте кристаллизации концентрация примеси равна Со, то в образующемся твердым слое она будет kоСо. Тогда перед фронтом кристаллизации должен возникнуть слой жидкости с концентрацией более высокой, чем Со. Концентрация примеси в жидкой и твердой фазах будет увеличиваться до тех пор, пока не установится стационарный режим, при котором количество примеси, скапливающейся перед фронтом кристаллизации в единицу времени, не станет равной количеству примеси, диффундирующей в жидкую фазу за тот же отрезок времени. Распределение концентраций примеси перед движущимся фронтом кристаллизации бинарного сплава в стационарном режиме описывается формулой:
|
|
|
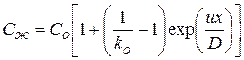 , (1.43)
, (1.43)
где u – скорость передвижения фронта кристаллизации; D – коэффициент диффузии в жидкой фазе; x – расстояние от фронта кристаллизации.
Возникновение переохлаждения обусловлено тем, что каждому составу смеси соответствует равновесная температура ликвидус
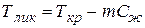 , (1.44)
, (1.44)
где m=const – наклон линии ликвидус.
Подставляя формулу (42) в (43), получим
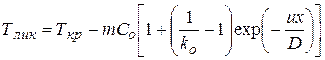 . (1.45)
. (1.45)
На фронте кристаллизации (х =0) температура жидкой фазы
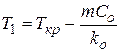 . (1.46)
. (1.46)
Фактическое распределение температуры по толщине слоя жидкого металла
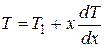
или, учитывая уравнение (44)
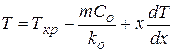 . (1.47)
. (1.47)
Полученные формулы справедливы и для случая ko >1, т.е. концентрационное переохлаждение не зависит от вида ko.
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 415; Нарушение авторских прав?; Мы поможем в написании вашей работы!