
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Аноксигенный 6 CO2 + 12 H2S → 6 (CH2O) +6 H2O + 12 S
|
|
|
|
Оксигенный 6 CO2 + 6 H2O → 6 (CH2O) + 6 O2
ФОТОСИНТЕЗ
Значительная часть минерализуется и образует залежи ископаемого углерода: каменные угли, нефть, известняки и др.
Помимо основной функции - источника углерода - CO2, растворённая в природных водах и в биологических жидкостях, участвует в поддержании оптимальной для жизненных процессов кислотности среды.
В составе CaCO3 - наружный скелет многих беспозвоночных, также содержится в кораллах, яичной скорлупе птиц.
Соединения углерода - HCN, CO, CCl4, преобладавшие в первичной атмосфере Земли в добиологический период, - в дальнейшем, превратились в сильные антиметаболиты обмена веществ.
Ò Миграция углекислого газа в биосфере Земли протекает двумя путями.
Первый путь - поглощение СО2 в процессе фотосинтеза с образованием органических веществ и в последующем захоронении их в литосфере в виде торфа, угля, горных сланцев, рассеянной органики, осадочных горных пород.
По второму пути - создание карбонатной системы в различных водоемах, где CO2 переходит
в H2CO3, HCO31-, CO32-, с последующим осаждением карбонатов CaCO3 биогенным и абиогенным путями. Возникают
мощные толщи известняков

На суше: В воде:
Ассимиляция продуцентами – 500 Растворение - 90
Дыхание авто- и гетеротрофов- 120 Выделение – 90
Гумификация - 1500 Осаждение - 38000
Осадочные породы -24*109
Сжигание топлива
10 Гигатонн

Ò Содержание АЗОТА в атмосфере в газообразном виде
составляет 79%. N │││ N
Существует два пути фиксации азота (перевода его в форму, доступную для растений)
1. Абиогенная фиксация - в результате
электрических разрядов (молний) и других
физических процессов
2. Биогенная фиксация азота - в результате деятельности микроорганизмов, бактерий или водорослей
|
|
|
Ò При фиксации азота (перевод N2 в NO3–) он включается в биомассу продуцентов, консументов и попадает в детрит.
Ò Микроорганизмы извлекают азот из разлагающихся материалов,
азот освобождается в виде аммиака (NH3) или ионов аммония (NH4+).
АММОНИФИКАЦИЯ – перевод азота из органической формы в
аммоний (NH4+) или аммиак NH3 Реакцию осуществляют бактерии
аммонификаторы (анаэробы и аэробы).
Затем другие микроорганизмы связывают аммонифицированный азот, переводя его обычно в форму нитратов (NO3–). Этот процесс носит название НИТРИФИКАЦИЯ – окисление аммония до нитрита (NO2–) затем до нитрата (NO3–).
1 фазу (NH3+ в NO2–) проводят бактерии рода Nitrosomonas,
2 фазу (NO2– в NO3–) бактерии рода Nitrobacter.

При гниении органических веществ часть азота превращается в аммиак, который под влиянием живущих в почве нитрифицирующих бактерий окисляется затем в азотную кислоту. Кислота, вступая в реакцию с находящимися в почве карбонатами, образует нитраты Са(NОз)2. Для уравновешения процесса стока азота существует компенсация этих потерь за счет извержения вулканов идругих видов геологической активности
Ò Процесс восстановления нитратов до молекулярного
азота ДЕНИТРИФИКАЦИЯ, азот из формы
растворенной переходит в атмосферную (из NO3- в N2.)
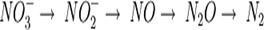
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 562; Нарушение авторских прав?; Мы поможем в написании вашей работы!