
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Отношение к действию окислителей и высоких температур
|
|
|
|
Химические свойства насыщенных углеводородов
Насыщенные (предельные) углеводороды – это вещества, трудно вступающие реакции при обычных температурах. Для всех углеводородов гомологического ряда метана характерна несклонность к реакциям присоединения. При определенных условиях они вступают в реакции замещения, в результате которых атомы водорода их молекул замещаются другими атомами или группами и образуются производные углеводородов. При энергичном воздействии температур или химических реагентов молекулы углеводородов разлагаются с разрушением углеродного скелета.
При низких температурах предельные углеводороды устойчивы даже к действию сильных окислителей. Так, например, раствор KMnO4 или хромовая смесь (K2Cr2O7+H2SO4) при комнатной температуре не окисляют предельные углеводороды и при действии на них не изменяют своей окраски.
Действие кислорода воздуха. При высоких температурах под действием кислорода воздуха предельные воспламеняются и сгорают с образованием СО2 и Н2О, выделяя большое количество тепла; на этом основано применение их в качестве топлива.
В настоящее время разработаны способы окисления углеводородов кислородом воздуха при низких температурах при помощи катализаторов. Так, например, из смеси высших углеводородов нефти путем окисления удается получить смеси высших жирных кислот, что может представить схемой:
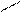
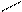
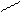
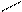 О2 О О
О2 О О
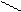
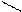 СН3—(СН2)m—CH3 ¾® CH3—(CH2)n—C + CH3—(CH2)p—C и т.д.
СН3—(СН2)m—CH3 ¾® CH3—(CH2)n—C + CH3—(CH2)p—C и т.д.
кат-р ОН n, p < m ОН
Так как окисление сопровождается разрывом углеродных цепей, образующиеся кислоты содержат меньшее число углеродных атомов, чем исходные углеводороды (т.е. в приведенной схеме n и p меньше, чем m).
|
|
|
Этот процесс имеет большое значение, так как высшие жирные кислоты идут для приготовления мыла, свечей и т.п., а получали их до недавнего времени только из жиров. В последнее время их предельных углеводородов путем каталитического окисления стали получать и другие ценные кислородсодержащие вещества (спирты, альдегиды).
Крекинг углеводородов. При нагревании углеводородов до высоких температур (450—550оС) без доступа воздуха они распадаются с разрывом углеродных цепей и образованием более простых и непредельных углеводородов. Такой процесс называют крекингом (расщеплением). Разложение углеводородов при еще более высоких температурах (550—650оС и выше) приводит к образованию простейших (главным образом газообразных) углеводородов; кроме того, при этом происходит замыкание углеродных цепей в циклы и получаются значительные количества ароматических углеводородов. Этот процесс называют пиролизом. Применением в процессах крекинга и пиролиза специальных катализаторов и давления удается регулировать эти процессы и получать необходимые продукты.
Реакция дегидрирования. Эта реакция заключается в отщеплении от молекул предельных углеводородов атомов водорода и приводит к образованию непредельных и циклических углеводородов. Она имеет большое промышленное значение.
Например, образование пропилена:
400-600 оС
СН3—СН2—СН3 ¾¾¾® СН3—СН=СН2 + Н2
кат. (Cr2O3)
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 480; Нарушение авторских прав?; Мы поможем в написании вашей работы!