
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. Сероорганические соединения
|
|
|
|
Физические свойства
Номенклатура
Сероорганические соединения
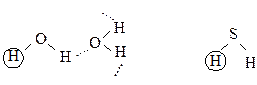 Сера является аналогом кислорода и образует часто аналогичные соединения:
Сера является аналогом кислорода и образует часто аналогичные соединения:
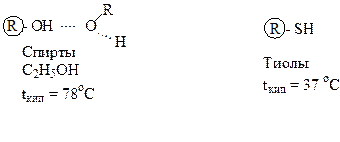 Электроотрицательность О – 3,5; S – 2,5
Электроотрицательность О – 3,5; S – 2,5
SH – тиольная или меркапто группа
Тиолы (тиоспирты)
Систематическая – название углеводорода + суффикс тиол.
Часто используют старые названия, в которых к названию радикала углеводорода добавляют - меркаптан
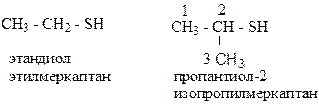 |
CH3 – SH - метантиол – газ, далее этантиол – жидкость, высшие тиолы – твёрдые вещества.
Атом серы вследствие своей меньшей электроотрицательности не склонен (либо в очень малой степени) образовывать водородные связи. В соответствии с этим тиолы – соединения неассоциированные, tкип спирта > tкип тиоспирта, тиоспирты менее растворимы в воде, чем спирты.
Тиоспирты ядовиты и обладают омерзительным запахом, который можно уловить, если на 400 млн частей воздуха – 1 часть меркаптана
Если спирты являются нейтральными соединениями, но проявляют в какой-то степени кислую природу, образуя алкоголяты при взаимодействии со щелочными металлами, то тиоспирты более сильные кислоты, чем соответствующие спирты и образуя соли взаимодействуя не только с металлами, но и с гидроокисями
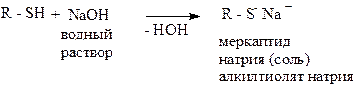
Образуют соли и с тяжёлыми металлами:
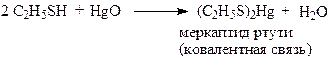 |
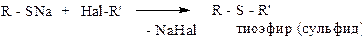 2. Образование простых тиоэфиров
2. Образование простых тиоэфиров
3. Образование сложных тиоэфиров
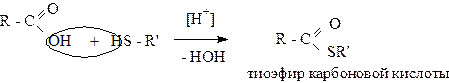
4. Окисление
Окисление спиртов направлено на атом углерода, а тиоспирты окисляются по атому серы.
Протекание реакции зависит от условий:
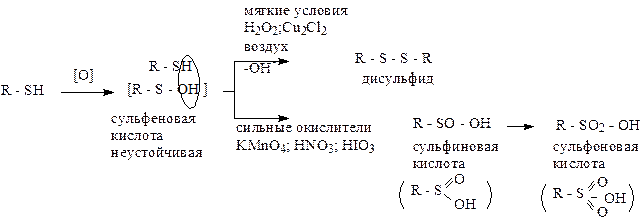 |
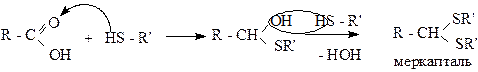 Образование меркапталей (ацеталей)
Образование меркапталей (ацеталей)
6. Алкилирование олефинов (присоединение по правилу Марковникова)
|
|
|
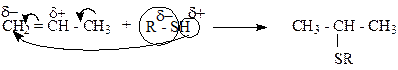 |
7. Десульфурирование
При каталитическом гидрировании в присутствии гетерогенных катализаторов отщепляется H2S
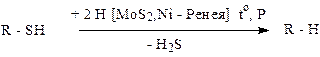 |
Реакция имеет большое промышленное значение в процессе переработки нефти для разложения и удаления серы из углеводородных фракций (гидрорафинирование). 300-400оС, 20-40 ати
Применение: этил- и изоамилмеркаптаны – одоранты бытового газа; додецилмеркаптаны – регулятор эмульсионной полимеризации в производстве синтетического каучука.
Тиоэфиры (сульфиды)
R –S – R; Ar – S – R; Ar – S - Ar
Номенклатура: перечисление названий радикалов + сульфид.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 1278; Нарушение авторских прав?; Мы поможем в написании вашей работы!