
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Natrii hydrocarbonas
Aqua purificata
Вода очищенная, H2O
Описание Бесцветная прозрачная жидкость без вкуса и запаха. pH от 5 до 7.
Недопустимые примеси:
Восстанавливающие в-ва: 100 мл доводят до кипения, прибавляют 1 мл KMnO4 и 2 мл H2SO4 разведённой, кипятят 10 минут. Розовая окраска должна сохраняться.
MnO4- + 6e + 8H+ à Mn2+ + 4H2O
Диоксид углерода: При взбалтывании с раствором известковой воды в течении 1ч. не должно быть помутнения. Известковая вода – это кальция гидроокиси раствор, который готовят из жженой извести, настаивая её в воде.
Ca2+ + CO32- à CaCO3¯
Нитраты и нитриты: к 5 мл. воды прибавляют 1 мл. раствора дифениламина: не должно появиться голубого окрашивания.
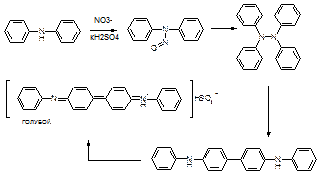
Хлориды, кальций, тяжёлые металлы, сульфаты. Допустимые примеси: Аммиак.
Натрия гидрокарбонат, NaHCO3, M. в. 84,0
Описание. Белый кристаллический порошок без запаха, соленощелочного вкуса, устойчив в сухом воздухе, медленно разлагается во влажном. Водные растворы имеют щелочную реакцию.
Растворимость. Растворим в воде, практически нерастворим в 95% спирте.
Подлинность. Препарат дает характерные реакции на натрий и гидрокарбонаты.
Na+ - смотри выше.
Для отличия от карбонат-иона проводят реакцию взаимодействия с насыщенным раствором сульфата магния. Испытание основано на образовании магния карбоната основного:
4MgSO4 + 4Na2CO3 à MgCO3•Mg(OH)2•3H2O¯ + 4Na2SO4 +CO2
Гидрокарбонат-ион образует осадок только при кипячении смеси, а карбонат-ион при обычной температуре.
Недопустимые примеси: тяжелые металлы, соли аммония.
Допустимые примеси: хлориды, сульфаты, железо, кальций, мышьяк.
Количественное определение. Около 1 г препарата (точная навеска) растворяют в 20 мл свежепрокипяченной и охлажденной воды и титруют 0,5 н раствором соляной кислоты (индикатор — метиловый оранжевый).
NaHCO3 + HCl à H2CO3 + NaCl
f=1; 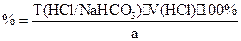
1 мл 0,5 н. раствора соляной кислоты соответствует 0,04200 г NaHCO3, которого в препарате должно быть не менее 99,0%.
Натрия гидрокарбонат для инъекций, кроме перечисленных выше требований, должен выдерживать следующее испытание: 5% раствор препарата должен быть прозрачным и бесцветным.
Хранение. В хорошо укупоренной таре.
Применение: ацидоз, язвенная болезнь желудка и двенадцатиперстной кишки, интоксикации, диабет, воздушная болезнь, морская болезнь.
|
|
Дата добавления: 2013-12-12; Просмотров: 867; Нарушение авторских прав?; Мы поможем в написании вашей работы!