
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электрохимические способы защиты от коррозии
Рациональное конструирование
Рациональное конструирование предусматривает комплекс мероприятий по предотвращению коррозии на основе современных научных данных и практических наработок в области защиты металлов от коррозии. Это исключение: контактной коррозии, внутренних напряжений в деталях, зон конденсации влаги, повреждения защитных покрытий и др. факторы. В случае необходимости применение: коррозионностойких металлов и сплавов, ингибиторов и др.
К электрохимическим способам защиты металлов от коррозии относятся протекторная и катодная защиты:
1) Протекторная защита.
По механизму защитного действия этот вариант аналогичен анодному покрытию. К защищаемой конструкции, находящейся в среде электролита, присоединяется более активный металл. В образующейся гальванопаре, за счет коррозии более активного металла, происходит поляризация электронами защищаемой конструкции. В качестве металла-протектора применяются Мg, Zn, Аl и другие активные металлы или их сплавы. Необходимым условием протекторной защиты является электропроводящий контакт конструкции с металлом-протектором.
Химизм протекторной защиты железа цинком в нейтральной среде:
Анодный процесс: Zn = Zn2+ + 2e.
Катодный процесс: O2 + 4H+ + 4e = 2H2O.
Суммарное уравнение: 2Zn + O2 + 4H+ = 2Zn2+ + 2H2O.
2) Катодная защита.
Сущность данного способа защиты от коррозии заключается в том, что защищаемый металл, находящийся в среде электролита, подключается к катоду(–) внешнего источника тока. В качестве анода можно использовать любой металлический лом. В результате окислители окружающей среды восстанавливаются на защищаемом металле электронами от внешнего источника тока, а окисляется металлический лом. Такой способ защиты чаще всего применяют для крупных конструкций, находящихся в среде электролита.
ТЕМА 5
ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ПРОТЕКАНИЯ ХИМИЧЕСКИХ ПРОЦЕССВ
ЛЕКЦИЯ № 12
«ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА»
Науку о взаимных превращениях различных видов энергии называют термодинамикой. Термодинамика устанавливает законы этих превращений, а также направление самопроизвольного протекания различных процессов.
1 Энергетика химических процессов.
Внутренняя энергия и энтальпия
Химические реакции сопровождаются выделением или поглощением тепла. Тепловой эффект реакции в основном определяется разницей между энергиями разрыва химических связей исходных веществ и образования связей в продуктах реакции.
В любом процессе соблюдается закон сохранения энергии. Теплота (Q), поглощенная системой, идет на изменение её внутренней энергии(DU) и на совершение работы (А):
Q = ΔU + A.
Внутренняя энергия системы U – это общий запас энергии системы. Абсолютные значения внутренней энергии веществ неизвестны, так как нельзя привести систему в состояние, лишенное энергии, поэтому на практике пользуются её изменением ΔU. Внутренняя энергия является функцией состояния, то есть её изменение однозначно определяется начальным и конечным состоянием системы и не зависит от пути перехода, по которому протекает процесс. Изменение внутренней энергии системы измеряют при постоянном давлении, то есть в изохорно-изотермическом процессе (v – const, T – const).
ΔU = U2 - U1,
где ΔU - изменение внутренней энергии системы,
U2 – энергия продуктов реакции, U1 – энергия исходных веществ.
Теплота и работа функциями состояния не являются, т.к. они служат формами передачи энергии и связаны с процессом, а не с состоянием системы.
Энтальпия (Н) применяется случае проведения процесса при постоянном давлении, то есть в изобарно-изотермических (p – const, T – const) и является функцией состояния. На практике пользуются также изменением энтальпии
ΔH = H2 - H1.
Стандартные условия: Т – 298 К, р– 1атм, n – 1моль, агрегатное состояние и кристаллическая модификация – наиболее устойчивые при стандартных условиях. Стандартные условия для изменения энтальпии обозначаются 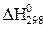 . Для простых веществ в стандартных условиях
. Для простых веществ в стандартных условиях 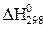 условно приняли равным 0.
условно приняли равным 0.
Примеры:
1) 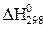 (Н2ОЖ) = -285,8 кДж/моль, т.е. при стандартных условия образование жидкой воды из простых веществ (Н2 и О2) сопровождается выделением 285,8 кДж энергии.
(Н2ОЖ) = -285,8 кДж/моль, т.е. при стандартных условия образование жидкой воды из простых веществ (Н2 и О2) сопровождается выделением 285,8 кДж энергии.
2) 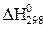 (Н2Г) = 0 кДж/моль.
(Н2Г) = 0 кДж/моль.
В термодинамике в уравнениях химических реакций наряду с указанием теплового эффекта реакции, указываются агрегатные состояния веществ и допускаются дробные коэффициенты. В такой форме записи уравнения называются термохимическими.
Пример:
Н2(г) + ½ О2(г) = Н2О(ж), 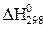 = -285,8 кДж/моль.
= -285,8 кДж/моль.
|
|
Дата добавления: 2013-12-12; Просмотров: 360; Нарушение авторских прав?; Мы поможем в написании вашей работы!