
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энтальпия топлива и продуктов сгорания
|
|
|
|
Величиной, характеризующей уровень энергосодержания рабочего тела является его полная энтальпия, имеющая химическую и теплофизическую составляющие:
I= Iхим+ IQ
Из условия сохранения энергии следует, что если в замкнутой изолированной системе при ее переходе из состояния 1 в состояние 2 происходят внутренние преобразования энергии, без совершения работы, то полное энергосодержание такой системы остается постоянной, перераспределяясь между ее исходными составляющими т.е.:
I1 = I2 и I1хим+ I1Q= I2хим+ I2Q.
где I1 – полная энтальпия рабочей смеси (топлива и воздуха) перед началом горения.
I1= ∑(iхим+ iQ)=I1хим+ I1Q
Тепловая составляющая энтальпии I1Q определяется выражением:
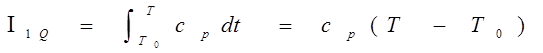
Ср – теплоемкость при постоянном давлении.
Т – текущая температура
Т0 - стандартная температура к которой приводятся теплота образования данного вещества из определенных «стандартных» веществ. Международным стандартом определено значение Т0= 298,15 К0.
I2 - полная энтальпия, образовавшихся в результате химической реакции продуктов сгорания, определяемая суммой их химических энергий и теплового эквивалента эффекта реакции:
I2= ∑(iхим+ iQ)=I2хим+ I2Q.
Таким образом, из условия I1 = I2 теплота, выделившаяся в результате химической реакции горения: Qр= I2Q - I1Q = I1хим - I2хим идет на нагрев продуктов сгорания, которым и надлежит совершить работу и передать часть своей энергии посредством механического преобразователя движителю транспортного средства.
Для совершения полезной работы должно происходить расширение газа. В тепловых двигателях расширение происходит в их рабочих органах: в соплах, сопловых аппаратах, рабочих цилиндрах, на лопатках турбин и т.д. При расчете двигателей обычно принимается, что зона химических реакций ограничена камерой сгорания, а при расширении изменяются только теплофизические параметры газовой смеси, т.е. за пределами камеры сгорания Iхим = const. Причем само расширение газа происходит при постоянной энтропии - (изоэнтропно). Совершаемая при этом единицей массы рабочего тела работа, определится разностью энергосодержаний газовых смесей после и до процесса расширения. Это положение следует из первого закона термодинамики:
|
|
|
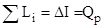 ,
,
где ∑Li – суммарная работа, совершаемая при расширении рабочего тела.
Полное энергосодержание потоков газа характеризуется энтальпией торможения, учитывающей кинетическую энергию его движения. Для газа в конце камеры сгорания (индекс 2) и на срезе сопла (индекс 3)можно записать:
 ;
; 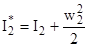 ;
; 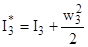
Скорость газа в самой камере сгорания w2 по отношению к скорости w3 - истечения из сопла можно принять равной нулю (w2 ≈0). Тогда:
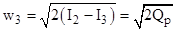
Скорость истечения газа при адиабатном процессе можно определить по известной из термодинамики зависимости:
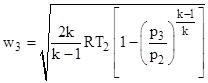
Из данного выражения следует, что скорость истечения определяется теплотой сгорания топлива, которая зависит от свойств самого топлива и режимных условий: (параметры Т, R,k) и от конструктивных возможностей двигателя: степени расширения газов (р3/р2). Для современных воздушно-реактивных двигателей степень расширения газов не превышает значения 0.025…0.033.
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 2975; Нарушение авторских прав?; Мы поможем в написании вашей работы!