
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Контроллинг как информационная система управления затратами
|
|
|
|
Химическая связь это силы, которые удерживают атомы в молекуле. При образовании химической связи энергия молекулы меньше энергии атомов, из которых состоит молекула. Избыточная энергия выделяется в виде теплоты. Природа химической связи едина - это взаимодействие между заряженными частицами (ядрами и электронами). В зависимости от способа реализации различают следующие типы связи: ковалентная, ионная, металлическая, водородная.
Теория химического строения. Химическая связь образуется за счет обобществления пары электронов с разным спином (современная теория ковалентной связи).
При взаимодействии двух атомов, один атом отдаёт, другой принимает электрон – основа современной теории ионной связи.
Правило октета: в результате образования химической связи, атомы могут приобретать такую же электронную конфигурацию, как у благородных газов, которые имеют на внешнем слое 8 электронов.
Количественные характеристики химической связи. Ч ем больше энергия связи, тем устойчивее молекула. Энергия связи (Есвязи) мера прочности связи.
Длина связи – расстояние между ядрами в соединении, зависит от размеров электронных оболочек и степени их перекрытия.
Химическая связь характеризуется углом - угол между линиями соединяющие ядра атомов.
Ионная связь. Электростатическое взаимодействие отрицательно и положительно заряженных ионов в химическом соединении возникает в случае большой разницы в электроотрицательности (ЭО) атомов. Так как действие электрического поля вокруг заряженной частицы имеет сферический характер, то для ионной связи не характерно направленность и насыщенность.
Вещества с ионной связью в обычных условиях являются твёрдыми, с большой температурой плавления и кипения. Их растворы и расплавы проводят электрический ток.
|
|
|
Так как энергия ионизации больше энергии сродства к электрону, то не происходит полного перехода электрона от одного атома к другому, следовательно, нет чисто ионной связи. Можно говорить только о большей или меньшей степени ионности. Предполагается, что ионная связь образуется при ΔЭО>1,7.
Ковалентная связь. Химическая связь, образованная путем обобществления пары электронов двумя атомами, называется ковалентной. При оптимальном расстоянии между ядрами, система имеет минимальную энергию - Есвязи.
Особенности ковалентной связи: направленность и насыщаемость. Направленность обусловлена пространственной ориентацией атомных орбиталей. Ковалентная связь направлена в сторону максимального перекрывания АО. Количественно направленность характеризуется валентным углом между линиями соединяющие ядра атомов. Насыщаемость: вызвана ограниченным количеством электронов на внешней оболочке, которые могут участвовать в образовании связи. Полярность: если обобществленные атомы распределены равномерно между атомами – неполярная связь (Н-Н, О=О). Полярная: один из атомов сильнее притягивает электроны и электронная плотность смещается в его сторону: критерием способности притягивать электрон является ЭО. Таким образом, разность ЭО характеризует полярность связи (ковалентно-полярная ∆ЭО>0,7).
Существует два приближенных метод расчета распределения электронной плотности в молекуле: метод валентных связей (ВС) и метод молекулярных орбиталей (МО).
Метод валентных связей (1927год Тейтлер и Лондон) предполагает, что:
1. Атомы в молекуле сохраняют свою индивидуальность.
2. Электронная пара «заселяет» орбиталь то одного, то другого атома.
3. Химическая связь между атомами возникает как результат перекрывания А.О.
|
|
|
4. Атомы, вступающие в связь, обмениваются электронами, которые образуют связывающие пары.
5. В соответствии с принципом Паули, химическая связь образуется при взаимодействии электронов с антипараллельными спинами.
6. Характер химической связи определяется типом перекрывания АО.
Обменный механизм образования химической связи метода ВС. Валентность – способность атома присоединять или замещать определённое число других атомов с образованием химической связи. Количественная мера в обменном механизме ВС – число неспаренных электронов в основном или возбужденном состоянии. Каждый атом предоставляет по одному электрону в общее пользование.
Донорно – акцепторный механизм. Обменный механизм не может объяснить образование некоторых химических соединений. Общая пара образовалась за счет пары электронов одного атома (донора) и свободной орбитали другого (акцептора).
Таким образом суммарная валентность равна сумме числу неспаренных электронов и числу связей способных образовываться по донорно – акцепторному механизму.
Метод МО. Электроны в молекуле распределены на МО, которые имеют определенную энергию и форму. МО охватывает всю молекулу в целом. Атомы не сохраняют индивидуальность. Молекулы – единая система.
В методе МО используется линейная комбинация атомных орбиталей (ЛКАО), при этом соблюдается ряд правил:
1. Число МО равно числу АО, из которых они комбинируются;
2. Энергия одних МО выше, других – ниже исходных АО;
3. Электроны заполняют МО в порядке возрастания энергии, при этом соблюдаются правило Паули и правило Гунда;
4. Наиболее эффективно комбинируются АО с сопоставимой энергией и симметрией;
5. Прочность связи пропорциональна степени перекрывания АО
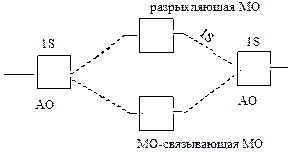
Метод МО объясняет возможность образования химической связи не только парой, но и одним электроном.
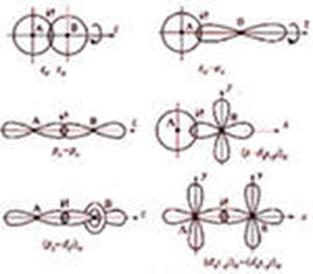
При образовании химической связи возможно несколько случаев перекрытие электронных орбиталей.σ-связь – связь, образованная перекрыванием АО по лини соединяющей ядра взаимодействующих атомов:

π – связь: образована перекрыванием АО по обе стороны линии соединяющей ядра атомов:
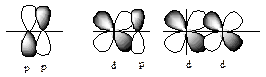
δ – связь – образована перекрыванием орбиталей в четырех точках.
|
|
|
Соотношение энергий и длинны связей следующее: Еπ связи<Еσ связи; Едвойной связи>Е одинарной связи; l двойной< l одинарной. Кратные связи образуются при наложении на σ связь, π и δ связей.
Гибридизация АО – выравнивание различных АО по энергии и по внешнему виду. Углерод, при получении энергии из вне, образует четыре не спаренных электрона, путем перехода одного электрона с 2s подуровня на 2р:
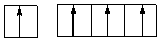 S1+P3
S1+P3
При образовании метана происходит смешивание этих четырех АО с образованием равноценных орбиталей по энергии и внешнему виду:
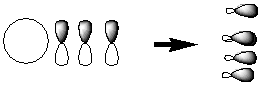
В данном случае имеет место sp3 – гибридизация. Возможны sp2, sp и другие более сложные виды гибридизации АО.
Пространственная структура молекул. АО располагаются в пространстве таким образом, что бы энергия отталкивания между электронами, находящиеся на АО, была наименьшая.
Пространственная структура молекул - определяется числом электронов участвующих в образовании химической связи и ее направленностью:
1. Двуцентровые системы линейны.
2. Если на внешней оболочке атома имеется 2 не спаренных электронов (р элементы VI группы – O, S, Te), то при их перекрывании с АО другого атома образуется угловая система в которой угол между линями соединяющие ядра трех атомов равен 90о. Из-за отталкивания электронов угол несколько больше 90о и для воды он равен 105˚.
3. Гибридизация АО определяет пространственную конфигурацию: sp - линейная, sp2 – угол примерно равен 120˚ (треугольная - молекула плоская), sp3 –гибридизация (молекула имеет объемное строение).
Полярность молекул характеризуется значением дипольного момента, равного произведению заряда на расстояние между зарядами.
Металлическая связь. Элементы-металлы образуют простые вещества-металлы за счет связи, называемой металлической. В атомах металлов малое число валентных электронов, слабо связанных с ядром, сочетается с наличием вакантных, близких по энергии орбиталей во внешнем слое. Эта особенность определяет возможность свободного перемещения электронов с одной орбитали на другую, за счет которого осуществляется связь между всеми атомами кристалла металла. Металлическую связь можно рассматривать как предельно делокализованную ковалентную, когда электроны, осуществляющие связь, обобществлены множеством ядер (“электронный газ”). Связь положительных ионов, расположенных в узлах кристаллической решетки, и обобществленных электронов называется металлической.
|
|
|
Этой связью объясняются физические свойства металлов: блестящий вид, пластичность, теплопроводность, электропроводность.
1. Сущность, задачи и функции контроллинга.
2. Эволюция методов учета и управления затратами.
3. Аналитические процедуры в системе контроллинга.
4. Схема принятия управленческих решений в системе контроллинга.
=1=
Рассматривая понятия управленческого учета, производственного учета или контроллинга следует их соотносить с национальными учетными системами, так как одним и тем же термином в разных странах могут обозначаться разные явления. Кроме того, и в самих западных странах, в Соединенных Штатах, в Германии или во Франции, специалисты в области методов управления не всегда имеют общую точку зрения на трактовку тех или иных понятий.
Так, в теории и практике управления немецкими предприятиями отсутствует понятие управленческого учета. Бухгалтерия четко подразделяется на финансовую и производственную, поэтому немцы заимствовали из английского языка термин «control1ing» и обозначили им качественно новое явление в теории и практике управления предприятием.
Напротив, в США не распространено слово контроллинг, несмотря на название профессии - контроллер (controller), а весь комплекс задач контроллинга решается в рамках управленческого учета.
Контроллинг – это система управления экономикой предприятия, ориентированная на выполнение оперативных и стратегических целей и достижение заданных результатов, объединяющая информационное обеспечение, планирование, контроль и анализ.
Информационное обеспечение контроллинга предполагает использование данных учета (финансового и управленческого) и любой внешней информации, полезной для принятия решений руководителями предприятия(анализ рынка, экономические тенденции, политическая ситуация и т. п.).
Планирование в системе контроллинга осуществляется посредством подготовки бюджетовдетальных планов в денежном выражении для каждого подразделения предприятия, интегрированных в прогнозный баланс, отчет о прибылях и убытках и прогноз движения наличности. Основой построения бюджетов могут являться обоснованные нормативы.
Контроль предполагает сопоставление планов с фактическим уровнем показателей, а также выявление отклонений. При этом концепция контроллинга исходит из того, что наибольший эффект при контроле за отклонениями достигается непосредственно во время возникновения отклонений.
Анализ возникающих отклонений позволяет своевременно выявлять их причины и соответствующим образом реагировать, принимая адекватные управленческие решения.
Одним из основных положений контроллинга является концепция так называемой неполной (усеченной) себестоимости, базирующаяся на методе директ-костинг, предполагающем группировку затрат в зависимости от их связи с объемами производства и реализации. Этот метод определяет себестоимость продукции только по сумме прямых (переменных) затрат, остальные затраты сопоставляются с суммой покрытия (маржинальным доходом, валовой маржой)
Основная задача контроллинга - обеспечивать достижение оперативных и стратегических целей предприятия. Поскольку главной стратегической целью коммерческого предприятия является максимизация прибыли и минимизация затрат, основной функциональной задачей контроллинга является управление затратами и финансовыми результатами деятельности предприятия. Контроллинг, в частности, должен дать ответы на следующие вопросы:
. Прибыльно ли предприятие сегодня?
. Будет ли предприятие прибыльно в будущем?
. Какие действия следует предпринять для изменения (оптимизации)ситуации?
Для реагирования на происходящие изменения в контроллинге реализуется так называемый «принцип термостата», который заключается в следующем. В комнате-термостате задается желаемый «температурный» режим (бюджет, бизнес-план предприятия). Система измеряет начальные показатели (достигнутый уровень предприятия), сравнивает с заданными, производит необходимые действия (управленческое решение). Происходящие внешние и внутренние изменения опять приводят к смене «температуры» (отклонения от бизнесплана). После корректировки принимаются адекватные управленческие решения.
Являясь системой управления экономикой предприятия, контроллинг выполняет следующие функции.
Управленческая (координация управленческой деятельности)
Планирования (постановка целей, разработка планов и бюджетов)
Контрольная (включает функции учета, анализа и регулирования)
Информационная (подготовка и обработка информации для принятия управленческих решений)
=2=
Долгое время учет затрат осуществлялся так называемым «котловым» методом, при котором в течение отчетного периода в едином бухгалтерском регистре учитывалась вся совокупность затрат. Основным недостатком этого метода является то, что представляемая в результате информация о себестоимости обезличена и не дает возможности контролировать и управлять издержками
В конце XIX - начале ХХ века потребности развивающейся экономики индустриальных стран заставили более пристально взглянуть на проблемы затрат и себестоимости.
В это время возникает направление, формирующее управленческий учет. Создателем этого направления принято считать экономиста Александра Гамильтона Черча (1866-1936). I
В учетной практике укрепляется принцип «различной себестоимости для различных целей», что приводит к возникновению и развитию трех основных методов учета затрат и калькулирования себестоимости продукции стандарт-кост, директ-костинга и учета по центрам ответственности.
Метод нормативного определения затрат возник в начале ХХ века в США. Это был один из принципов научного менеджмента, предложенных Ф. Тейлором, Г. Эмерсоном и другими инженерами, которые дали импульс для развития системы нормативного учета затрат. Они применяли стандарты, чтобы выявить «единственный наилучший путь» использования труда и материалов. Стандарты обеспечивали информацией для планирования хода работ так, что потребление материалов и труда сводилось к минимуму.
Бухгалтерское воплощение мыслей Эмерсона осуществил Чартер Гаррисон. В 1911 году он разработал и внедрил первую полную действующую систему нормативного определения затрат в компании-изготовителе рабочих перчаток.
Идея «Стандарт-кост» у Ч. Гаррисона трансформировалась в два положения:
- все произведенные затраты в учете должны быть соотнесены со стандартами;
- отклонения, выявленные при сравнении фактических затрат со стандартами, должны быть расчленены по причинам.
Новое направление, явившееся определенным этапом в становлении управленческого учета, часто связывают с работой выдающегося экономиста Джона Мориса Кларка (1884–1963). Он подчеркивал, что для администраторов каждая статья затрат имеет различную целевую установку и это является главным, а распределение затрат для принятия управленческих решений значения не имеет. В 1936 г., развивая эту идею, Джонатан Харрис создал учение директ-костинг, согласно которому в составе себестоимости необходимо учитывать только прямые расходы. Вначале эта концепция не получила широкого признания, ее критиковали сторонники полной себестоимости, утверждая, что полная себестоимость необходима для акционеров, вкладчиков капитала и даже для управляющих. И только с 60-х годов директ-костинг стал преобладающим методом учета затрат. Его сущность заключается в том, что издержки делятся на две группы: переменные (прямые) и постоянные (косвенные). Основу учета себестоимости составляют только переменные издержки. Косвенные расходы исключаются из себестоимости, так как, по мнению сторонников этого метода, они вызваны не столько процессом производства, сколько течением времени. Кроме того, авторы считали, что для ценовой политики решающее значение имеют именно прямые расходы. Таким образом, для директ-костинга основным принципом является отделение в учете прямых издержек от косвенных. Они совершенно различны и в схемах корреспонденции счетов никогда не должны смешиваться. Это объясняется тем, что только переменные издержки связаны с объемом реализуемой продукции. Иначе в экономической литературе эти издержки называют «затраты на продукт» и «затраты на период»
Развитие систем управления затратами привело также к возникновению. концепции центров ответственности. Данная концепция была сформулирована Джоном А. Хиггинсом.
В соответствии с основным правилом Хиггинса каждую структурную. единицу предприятия обременяют те и только те расходы или доходы, за которые она может отвечать и которые контролирует.
Дальнейшее развитие принципов ответственности связано с созданием Спенсером А. Тукером (1962) метода ТЧМ (тариф-чае-машина), сущность. которого сводится к закреплению за каждым центром ответственности соответствующих машин и определению расходов, связанных с работой одного машино-часа.
Органическим развитием метода стандарт-кост и учета по центрам ответственности явился метод JI Т (джи ай ти)- just-in-time (джаст ин тайм)- точно вовремя. Здесь в основу положены проценты отклонений от графиков работ и стандартов.
Дальнейшее развитие теории и практики управления затратами привело к формированию в 1970-х гг. контроллинга как целостной системы управления предприятием.
=3=
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 496; Нарушение авторских прав?; Мы поможем в написании вашей работы!