
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Структура и функция протонной АТФ-азы. Механизм разобщения
|
|
|
|
Механизм генерации DmН+, его компоненты, стехиометрия Н+/е.
Движение электронов через электронтраспортную систему дыхательных ферентов сопровождается одновременно «перекачиваем» протонов из матрикса в межмебранное пространство. Эта передислокация протонов осуществляется I, III и IV комплексами дыхательной цепи. Английский биохимик Питер Митчелл предложил рассматривать внутреннюю мембрану митохондрий как конденсатор, который со стороны матрикса заряжается отрицательно (благодаря направленному току электронов), а со стороны межмембранного пространства – положительно. Следовательно, при тканевом дыхании совершается осмотическая работа по концентрации протонов в межмембранном пространстве и возникает разность электрических потенциалов, т.е. генерируется электро-химический (или протонный) потенциал:
Δ μН+ = Δ Ψ – (-)ΔрН+
Электрохимический Мембранный Градиент рН
градиент рН потенциал
Градиент ΔрН+ имеет отрицательное значение, поскольку измерение проводится от внутренней поверхности мембраны, имеющей более отрицательную величину, к наружной. В целом Δ μН+ имеет положительное значение, равное +0,224v.
Внутренняя мембрана не может заряжаться сколь угодно долго. Если продолжить аналогию с конденсатором, то перезарядка приводит к «пробою», т.е. разрядке.Роль разряжающего устройства выполняет АТФ-синтаза – V комплекс дыхательной цепи.
Каким же образом генерирование протонного потенциала связано (сопряжено) с образованием АТФ?
Свободная энергия электрохимического протонного градиента митохондриальной мембраны используется для синтеза АТФ с помощью протон-переносящей АТФ-синтазы (она также называется протонным насосом, АТФ-азой, F1Fo-АТФ-азой, V комплексом дыхательной цепи).
|
|
|
АТФ-синтаза является самым крупным, по форме напоминающим гриб, структурным компонентом внутренней митохондриальной мембраны. АТФ-синтаза представлена 2 большими полиферметными белками - F1 (шляпка гриба) и Fo (ножка), каждый из которых, в свою очередь, состоит из нескольких неоднородных полипептидов.
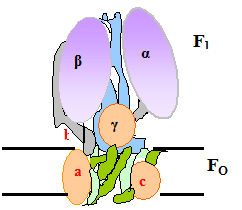
Рис. 5.6. Модель грибовидного комплекса АТФ-синтазы. V комплекс.
Fо – не растворимый в воде трансмембранный белок, главной частью которого является канал для транслокации протонов. Fo означает «ф актор О» (от слова олигомицин - антибиотик, продуцируемый Streptomyces). Олигомицин ингибирует транспорт протонов через «ножку» Fо, реагируя с единственным остатком глутаминовй кислоты на одной из субъединиц. Блокада транспорта протонов приводит к потере способности АТФ-азы синтезировать АТФ.
F1- водорастворимый периферический мембранный белок, состоящий из 5 субъединиц. Если отделить (например, мочевиной) F1 от Fо, то первый сможет только гидролизовать АТФ, но потеряет способность эту молекулу синтезировать.
Синтез АТФ катализирует β-субъединица белка F1. Этот синтез осуществляется спонтанно, т.е. без затраты энергии. Происходит это следующим образом (рис.5.7): F1 имеет 3 химически идентичных, но конформационно различно взаимодействующих αβ-протомеров: О (open) – с открытой конформацией, характеризующейся очень низкое сродство к лигандам и каталитически неактивной; L (loose) - легко связывающей лиганды и каталитически неактивной; T (tight) – жёстко связывающей лиганды и каталитически активной.

Рис. 5. 7. Работа «молекулярной турбины» – фактора F1.
В состав F1 входит γ-субъединица, способная вращаться подобно тому, как вращается турбина в воде («молекулярная турбина»). Вращение γ-субъдиницы обуславливает конформационные изменения в αβ-протомерах.
|
|
|
Связывание АДФ с неорганическим фосфатом происходит на участке L. После этого происходит вращение γ-субъединицы на 120˚ (на рис. против часовой стрелки). Это вращение требует затраты энергии, которая аккумулируется при генерации электро-химического потенциала и подпитывается протонным переносом через канал Fo. При вращении γ-субъединицы происходят конформационные изменения αβ-протомеров, в результате чего L -участок преобразуется в T, а T - в O. В Т-участке осуществляется синтез АТФ, а из О -участка (вследствие вращения «турбины») высвобождается АТФ.
Таким образом, энергия электро-химического потенциала требуется не для синтеза АТФ, а для удаления её из активного центра V комплекса. Эта энергия расходуется также на транспорт АТФ из матрикса через митохондриальные мембраны в цитоплазму клетки, а АДФ – в обратном направлении (на работу фермента АТФ-транслоказы). Львиная доля энергии протонного потенциала расходуется на транспорт ионов кальция. Доставка субстратов тканевого дыхания также осуществляется за счёт этой энергии.
Измерение «силы протонного потенциала» показало, что 1 молекула АТФ может образоваться за счёт окисления НАДН∙Н+ первым комплексом дыхательной цепи, 1 молекула АТФ – за счёт окисления убихинола третьим комплексом и 1 молекула – при окислении цитохрома с четвёртым комплексом. Именно в этих местах падение редокс-потенциала превышает 0,2 v, при таком перепаде освобождается энергия, вполне достаточная для синтеза молекулы АТФ (для синтеза АТФ необходимо затратить 42 кДж/моль). Таким образом, при окислении НАД-зависимых субстратов может образоваться 3 молекулы АТФ, а при окислении ФАД-зависимых – 2 молекулы АТФ (транспорт электронов начинается со второго комплекса дыхательной цепи).
Следует заметить, что ещё в 30-х годах академик В.А. Энгельгардт обнаружил, что при тканевом дыхании на 1 молекулу кислорода расходуется 3 молекулы фосфата, т.е. отношение Р/О=3 (при использовании НАД-зависиымых субстратов тканевого дыхания). Если в среду инкубации митохондрий добавлялся сукцинат, коэффициент Р/О=2. Эти показатели были названы В.А. Белицером и Е.Т. Цыбаковой коэффициентами фосфорилирования, а I, III и IV комплексы дыхательной цепи – пунктами сопряжения ( связи между процессами окисления и фосфорилирования).
|
|
|
Согласно подсчётам известного российского биохимика В.П. Скулачёва, в сутки у человека может синтезироваться более 30 кг (!) АТФ: поскольку в сутки у человека образуется 400 мл воды (22 моля), а коэффициент Р/О=3 (66 молей АТФ), то умножая на молекулярную массу АТФ (507), получаем
707 х 66 = 33 462 (т.е.>33 кг)
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 713; Нарушение авторских прав?; Мы поможем в написании вашей работы!