
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внутренняя энергия и энтальпия системы. Первый закон термодинамики. Тепловой эффект химической реакции
|
|
|
|
Основные понятия термодинамики.
Основные понятия химической термодинамики.
1. Основные понятия термодинамики.
2. Внутренняя энергия и энтальпия системы. Первый закон термодинамики. Тепловой эффект химической реакции.
3. Факторы, определяющие глубину и направленность химических реакций. Понятия об энтропии и энергии Гиббса. Второй и третий законы термодинамики.
4. Термодинамические представления о равновесном состоянии.
Химическая термодинамика изучает энергетические эффекты, сопровождающие химические процессы, зависимость их от условий протекания, вероятность самопроизвольного течения процесса, их направление и пределы.
Термодинамический подход к изучению систем состоит в том, чтобы мысленно изолировать объект исследования от окружающей среды, называемой термодинамической системой.
Система, лишенная возможности обмена веществом или энергией с окружающей средой и имеющая постоянный объём, называется изолированной или замкнутой.
Фаза – это часть системы с одинаковыми физическими и химическими свойствами.
Различают гомогенные и гетерогенные системы.
Гомогенная система – это однородная система, имеющая одну фазу (воздух, любая газовая смесь и т.д.).
Гетерогенная система – это система, имеющая две или более фазы (насыщенный раствор с осадком, уголь в атмосфере воздуха).
Различают фазовые и химические превращения. При химических превращениях изменяется состав и свойства химических соединений. При фазовых превращениях не затрачивается состав и свойства химического вещества (плавление льда, превращение воды в пар и т.д.)
|
|
|
Совокупность термодинамических свойств системы называется её состоянием.
Величины, позволяющие определить состав системы, называются параметрами (состав, концентрация, давление, объём, температура).
Состав системы может быть равновесным и неравновесным.
Равновесное состояние – это такое состояние системы, которое с течением времени самопроизвольно не изменяется (т.е. без каких-либо внешних воздействий на систему её параметры остаются неизменными). Напротив, состав системы будет неравновесным, если параметры её изменяются во времени при отсутствии внешнего воздействия.
Равновесное состояние может быть устойчивым и ограниченным (метостабильное состояние), причём в ограниченном состоянии система стремится занять устойчивое состояние.
Переход термодинамической системы из одного состояния в другое, сопровождающееся изменением параметров системы, называется процессом.
Процесс, при котором термодинамическая система, пройдя через ряд промежуточных состояний, возвращается в исходное состояние, называется круговым процессом или циклом.
В зависимости от того, какие параметры системы при переходе её из одного состояния в другое, остаются постоянными, процессы делятся на:
- изотермические (Т = const),
- изохорические (V = const),
- изобарические (P=const),
- адиабатические (отсутствует теплообмен с окружающей средой).
Параметры системы дают возможность ввести переменные, позволяющие характеризовать состояние системы, следовательно, происходящие в ней изменения. Это термодинамические функции:
внутренняя энергия u,
энтальпия H,
энтропия S,
энергия Гиббса G.
Данные функции являются функциями состояния, т.е. их значения определяются только начальными и конечными параметрами системы и не зависят от пути перехода, по которому протекает процесс.
Внутренняя энергия системы (u) складывается из поступательного и вращательного движения молекул, атомов; энергии движения ядер и электронов, энергии межъядерного и внутриядерного взаимодействия. Изменение внутренней энергии при переходе из одного состояния в другое:
|
|
|
Δu=u2–u1,
где u2 и u1 – внутренняя энергия системы в конечном и начальном состояниях.
Количественное соотношение между изменением внутренней энергии, теплотой и работой устанавливает первый закон термодинамики: теплота, подведённая к системе Q, расходуется на изменение внутренней энергии системы Δu и на совершение системой работы A против внешних сил:
Q = Δu+A (1)
A = P(V2-V1) = p ΔV
Q = Δu+РΔV, (2)
где p – внешнее давление, V1– объём начального состояния системы, V2 - объём конечного состояния системы.
При изохорическом процессе (V = const, ΔV = 0):
QV = Δu (3)
При изобарическом процессе (Р = const):
Qp = Δu+pΔV (4) или
Qp =u2–u1+ pV2 -pV1 = (u2 +p V2 )-(u1+ pV1) (5)
Термодинамическая функция:
u + рV = H (6),
называется энтальпией системы.
Подставив уравнение (6) в (5), получим первый закон термодинамики для изобарического процесса:
Δ Qp = H2 – H1 = Δ H (7)
Энтальпия также как и внутренняя энергия характеризует энергетическое состояние вещества, но включает ещё работу на расширение.
Энтальпия является функцией состояния системы, т.е. её значение определяется заданными начальным и конечным состояниями и не зависит от пути перехода. Она выражается в кДж/моль.
Тепловым эффектом химической реакции называется количество тепла (энергии), выделяемое или поглощаемое системой в ходе химической реакции, протекающей необратимо при р,Т = const или V,T = const, т.е. в условиях постоянного объёма или постоянного давления, а получаемые продукты реакции имеют при этом ту же температуру, что и исходные вещества.
При экзотермических реакциях теплота выделяется, т.е. уменьшается энтальпия и внутренняя энергия системы, и значения Δu и ΔH для них отрицательны.
При эндотермических реакциях теплота поглощается, энтальпия и внутренняя энергия системы возрастают, а это значит, что ΔH и Δuимеют положительные значения.
Уравнения химических реакций с указанием теплового эффекта называются термохимическими.
В термохимических уравнениях указываются не только тепловые эффекты реакций, но и агрегатные состояния или кристаллическая модификация веществ.
|
|
|
Термохимическое уравнение реакции образования 1 моль СО2 имеет вид:
С(гр.)+ О2 (г) = СО2 (г); ΔH= -393,5 кДж.
В основе термодинамических расчётов лежит закон Г.И. Гесса (1841 г): тепловой эффект химической реакции зависит только от природы и состояния исходных веществ и конечных продуктов, но не зависит от пути процесса, т.е. от числа и характера промежуточных стадий.
В термодинамических расчётах часто применяют следствия из закона Гесса:
1. Тепловой эффект прямой реакции равен тепловому эффекту обратной реакции с противоположным знаком:
Δ H1
А ══ В
Δ H2
ΔH1 = - ΔH2 (8)
2. Тепловой эффект химической реакции Δ Нх.р. равен сумме теплот образования ΔНобр.продуктов реакции за вычетом суммы теплот образования исходных веществ (с учётом коэффициентов перед формулами этих веществ в уравнении реакции):
ΔНх.р. = S (Δ Нобр.)прод. - S (Δ Нобр.)исх. (9)
3. Тепловой эффект химической реакции ΔНх.р.равен сумме теплот сгорания ΔНсгор.исходных веществ за вычетом суммы теплот сгорания продуктов реакции (с учётом коэффициентов перед формулами этих веществ в уравнениях реакции):
Δ Нх.р. = S (Δ Нсгор.)исх. - S (Δ Нсгор.)прод.(10)
Тепловой эффект реакции зависит не только от природы реагирующих веществ, но и от условий, в которых протекает реакция, поэтому все тепловые эффекты приводят к стандартным условиям: 1 моль вещества, температура 250С (298 К), давление 1 атм. (101325 Па).
В термохимических расчётах используют энтальпии (теплоты) образования веществ.
Теплотой образования называется тепловой эффект реакции образования 1 моль вещества из простых веществ, при этом он приведён к стандартным условиям.
Стандартные теплоты образования принято обозначать 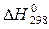 .
.
Стандартные теплоты образования простых веществ, устойчивых в стандартных условиях, равны нулю.
Теплота образования одного и того же химического соединения зависит от агрегатного состояния вещества и от его аллотропного видоизменения:
|
|
|
H2(г)+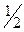 О2 (г) =Н2О(ж);
О2 (г) =Н2О(ж); 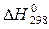 = -285,83 кДж
= -285,83 кДж
H2(г)+ 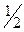 О2 (г) = Н2О(г);
О2 (г) = Н2О(г); 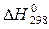 = -241,82 кДж
= -241,82 кДж
Для реакции вида аА+вВ=сС+dD тепловой эффект определяется равенством:
ΔH = с(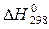 )обр.(С) + d(
)обр.(С) + d(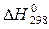 )обр(D) – a(
)обр(D) – a(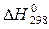 )обр(A) – b(
)обр(A) – b(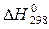 )обр (B)
)обр (B)
|
|
|
|
|
Дата добавления: 2013-12-14; Просмотров: 5964; Нарушение авторских прав?; Мы поможем в написании вашей работы!