
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Понятие об электродном потенциале
|
|
|
|
Сущность возникновения электродного потенциала заключается в следующем: при погружении металла в раствор собственных ионов начинается сложное взаимодействие металла с компонентами раствора. Наиболее важной является реакция поверхностных ион - атомов металла, находящихся в узлах решетки, с полярными молекулами воды, ориентированными у поверхности электрода.
|
 M + mH2O M(H2O)m
M + mH2O M(H2O)m


|


















|
|











 | |||||||
 | |||||||
 |  | ||||||
 | |||||||
 | |||||||
 | |||||||
 | |||||||
 | |||||||
 | |||||||
 | |||||||
 |  | ||||||
 | |||||||
 | |||||||
 |
Рис. 1 Двойной электрический слой на границе раздела металл-раствор.
Между металлом и раствором возникает разность потенциалов, которая называется электродным потенциалом. По мере перехода ионов в раствор растет отрицательный заряд поверхности металла и положительный заряд раствора. Наряду с этой реакцией протекает обратная реакция – восстановление ионов металла до атомов:
 |

|
При некотором значении электродного потенциала скорость прямого процесса будет равна скорости обратного процесса, устанавливается равновесие:
|
|
|
 |
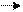
|
 M + mH2O M(H2O)
M + mH2O M(H2O)
Или упрощенно:
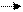
 М Мn+ + ne
М Мn+ + ne
Потенциал, устанавливающийся в условиях равновесия электродной реакции, называется равновесным электродным потенциалом.
|
|
|
|
Дата добавления: 2013-12-14; Просмотров: 305; Нарушение авторских прав?; Мы поможем в написании вашей работы!