
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Присоединение карбенов к двойным связям углерод-гетероатом
|
|
|
|
Присоединение к тройным связям
Алкины реагируют с карбенами (преимущественно первичными [Днепровский, с. 203]), давая циклопропены, однако в случае самого ацетилена первоначально получающиеся циклопропены выделить не удается из-за их быстрой перегруппировки в аллены:

Имеются примеры присоединения карбенов к двойным связям углерод-гетероатом Реакции проходят без участия свободного карбена, т. е. это реакции переноса карбена:
(i)

(ii)

4. Внедрение карбенов по связи С–Н (O–H, N–H, C–Hal, C–Si)
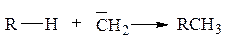
Благодаря высокой реакционной способности синглетного метилена реакция его внедрения (insertion reaction) по связям С–Н протекает неселективно, т. е. константы скоростей внедрения по третичным, вторичным и первичным связям С–Н примерно равны [Беккер, Ельцов, с. 187]. Благодаря этому в приведенной ниже реакции все три возможных продукта образуются примерно в статистическом соотношении 6:4:2=3:2:1:

Из-за неселективности эта реакция непригодна в синтетических целях.
Триплетный карбен реагирует со связями С–Н значительно более селективно: относительные константы скоростей внедрения kvперв.: kvвтор.: kvтрет. = 1: 12: 120.
Предполагаемые механизмы:
Определенных доказательств механизма не имеется, но можно представить по крайней мере два основных пути реакции.
(1) Синхронный одностадийный процесс с трехцентровым переходным состоянием
Такой механизм возможен только для синглетных карбенов (см. ниже). Его можно представить либо гетеролитическим, либо гомолитическим.
При гетеролитическом одностадийном механизме происходит синхронное смещение электронных пар, без предварительного образования каких-либо радикалов:
|
|
|

Для синглетных (но не триплетных – см. ниже) карбенов можно предположить и синхронный одностадийный гомолитический (свободнорадикальный) процесс:
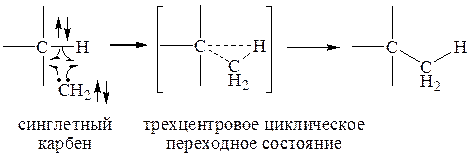
(2) Двухстадийный процесс
Его также можно представить либо гомолитическим, либо гетеролитическим.
Двухстадийный гомолитический (свободнорадикальный) механизм теоретически можно предположить как для синглетных, так и для триплетных карбенов.
Для триплетных карбенов:
а) Отрыв водорода (см. раздел III-7) с последующей инверсией спина:
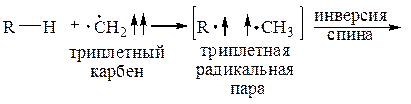
б) Рекомбинация в клетке растворителя:
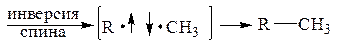
Для синглетных карбенов:
В случае реализации такого механизма для синглетных карбенов на стадии отрыва водорода (а) должна образовываться синглетная радикальная пара, рекомбинирующая в клетке растворителя на стадии (б):
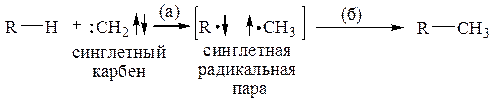
Казалось бы, доказательством двухстадийного гомолитического механизма могут служить наблюдаемые в реакциях внедрения карбенов диспропорционирование и димеризация, например:
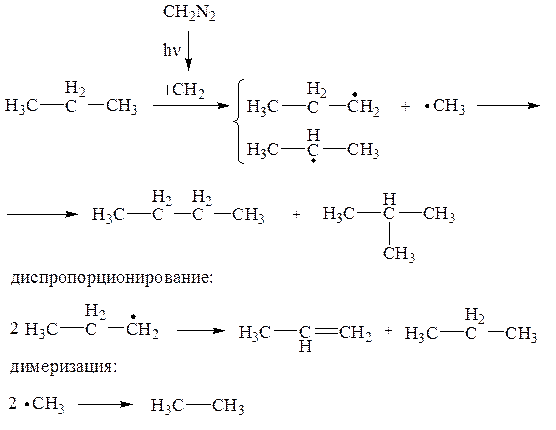
Однако продукты диспропорционирования и димеризации могут образовываться и при реализации одностадийного механизма (1), т. е. процесса прямого («истинного») внедрения карбена, за счет того, что образующееся в результате прямого внедрения соединение находится в возбужденном состоянии и, обладая избыточной энергией, может распадаться на свободные радикалы:
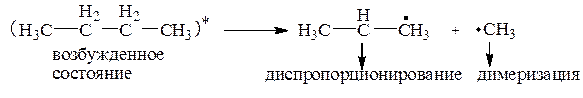
Двухстадийный гетеролитический механизм внедрения возможен только для синглетных карбенов:

Предполагается, что синглетные карбены внедряются по прямому одностадийному гетеролитическому механизму (1), хотя до конца вопрос не выяснен. Одним из доказательств в пользу синхронного одностадийного механизма, а не двухстадийного гомолитического или гетеролитического, также теоретически возможных для синглетных карбенов, может служить наблюдаемое во множестве случаев сохранение конфигурации при атоме углерода, по которому происходит внедрение карбена. Действительно, в случае промежуточного образования радикала R˙ или аниона Ry происходила бы инверсия конфигурации и, как следствие, потеря оптической активности при этом углероде. Кроме того, тенденция к отрыву водородного радикала у синглетных карбенов, не являющихся свободными радикалами, выражена слабо: они способны отрывать только атомы галогенов, но не водорода [Марч, т. 1, с. 255].
|
|
|
Триплетные карбены, будучи бирадикалами, легче отрывают водород (см. раздел III-7) и внедряются по двухстадийному свободнорадикальному механизму (2). Образование триплетной радикальной пары в случае внедрения триплетных карбенов зафиксировано методом химически индуцированной поляризации ядер [Днепровский, с. 202]. Кроме того, синхронный одностадийный механизм, как гетеролитический, так и гомолитический, для триплетных карбенов запрещен в соответствии с законом сохранения спина. Действительно, при атаке связи С–Н триплетной частицей новая ковалентная связь не может быть образована обоими неспаренными (свободными) электронами карбена, т. е. гетеролитическим способом, так как она (ковалентная связь) может осуществляться только парой электронов с антипараллельными спинами, а согласно правилу Гунда триплетные карбены имеют параллельные спины (см. выше); при этом самопроизвольная инверсия одного из них в ходе элементарного реакционного акта запрещена. Синхронный гомолитический механизм для триплетных карбенов также не реализуется из-за запрета по симметрии (сравни с разделом III-1):
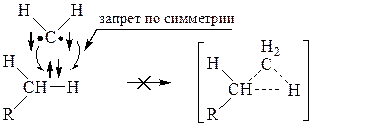
Установлен следующий порядок реакционной способности карбенов в реакциях внедрения и присоединения:
CH2 > HCC(O)OR > PhCH > BrCH» ClCH
Синглетный метилен CH2 является, по-видимому, самой реакционноспособной частицей из всех органических частиц. Триплетный метилен несколько менее реакционноспособен. Дигалогенкарбены, как правило, вообще не вступают в реакции внедрения.
Способность внедрения по связям С–Н уменьшается в ряду:
третичный алкил > вторичный алкил > первичный алкил
Ниже приведены примеры реакций внедрения карбенов по связям С–Н и C–Hal:
|
|
|
(i)
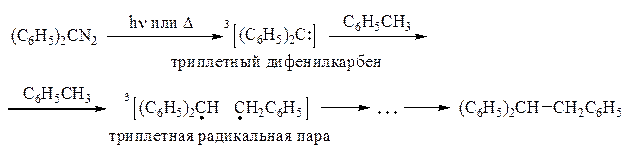
(ii) В зависимости от того, в каком состоянии находится метилен, он внедряется в дейтерохлороформ по разным связям: синглетный – по связи C–Cl, а триплетный – по связи C–D. Использование дейтерированного хлороформа позволяет легко различить продукты внедрения с помощью метода ЯМР на ядрах 1Н.
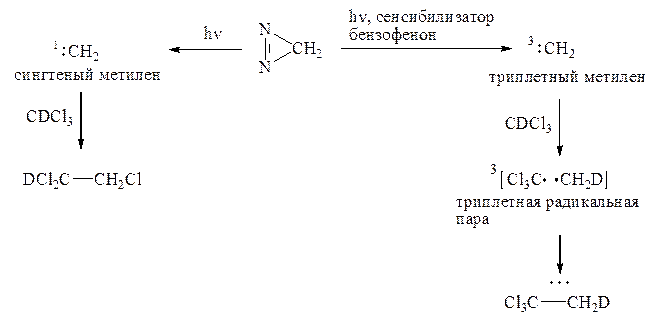
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 779; Нарушение авторских прав?; Мы поможем в написании вашей работы!