
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Випаровування. Пружність насиченого пару
|
|
|
|
Тема 6. Водяна пара в атмосфері
Лекція 10
Водяна пара потрапляє в атмосферу завдяки випаровуванню з поверхонь морів і океанів, річок і озер, вологого ґрунту і рослинного покриву. Випаровування відбувається також з поверхні снігового покриву та льодовиків. За сучасними підрахунками М.І.Львовича, з поверхні океанів випаровується за рік 447 900 км³ води (86%), а з поверхні материків 70 700 км³ (14%).
Найбільшу кількість водяної пари містять шари повітря, що безпосередньо прилягають до поверхні випаровування. У вищележачі шари водяна пара потрапляє за допомогою дифузії та також шляхом вертикального обміну – конвекції та турбулентності.
Повітряні течії переносять водяну пару з океанів углиб континентів. Тому кількість водяної пари зменшується по мірі підняття над поверхнею землі та по мірі віддалення від океанів і берегів углиб континентів. Кількість водяної пари в атмосфері залежить від багатьох причин, і тому водяна пара є наймінливою складовою частиною атмосферного повітря.
Фізична суть процесу випаровування полягає в наступному.
Молекули рідини (твердого тіла) знаходяться в безперервному русі та рухаються з різними швидкостями. Молекули, що розташовані у поверхні та володіють великими швидкостями, переборюють сили молекулярного зчеплення та вилітають із рідини в оточуючий простір. З підвищенням температури кількість молекул, що швидко рухаються, збільшується й, отже, швидше йде випаровування.
У результаті випаровування рідина (тверде тіло) переходить у газоподібний стан, і над поверхнею розподілу утворюється шар пару цієї речовини. Молекули пару рухаються в різних напрямках, і частина їх може знову потрапити назад у рідину.
|
|
|
Якщо більше тих частинок, що вилітають, ніж тих, які повертаються назад, то спостерігається процес випаровування. По мірі збільшення кількості пари в просторі над поверхнею випаровування кількість молекул, що вилітають і повертаються, в одиницю часу може виявитися однаковою, тоді установлюється рухома рівновага (стан насичення), при якому видиме випаровування закінчується.
Якщо кількість пари у просторі над поверхнею випаровування чомусь більше тієї, яка необхідна для насичення, тобто простір перенасичений парою, то кількість молекул, які повертаються, перевищить кількість молекул, вилітаючих із рідини, і розпочнеться процес обернений випаровуванню - конденсація пари на поверхні рідини. Таким чином, випаровування відбувається тим швидше, чим вище температура випаровуючого тіла та чим менше пари знаходиться над випаровуючою поверхнею.
При випаровуванні молекули, що переходять у газоподібний стан, витрачають частину своєї енергії на переборювання сил зчеплення та на роботу розширення, оскільки питомий об’єм рідини збільшується при переході її в пару. Внаслідок цього середня енергія молекул, які залишаються в рідині, зменшується, тобто рідина охолоджується. Щоб рідина, що випаровується, зберігала постійну температуру, до неї необхідно підводити тепло ззовні. Це тепло називається теплотою випаровування.
Для випаровування води та льоду необхідна велика кількість тепла: так, при 0° теплота випаровування води складає Lв=597 кал/г, а льоду Lл=677 кал/г, тобто більше на 80 кал, ніж це необхідно для перетворення 1 г води в пару. Водяна пара, що утворюється над випаровуючою поверхнею, чинить на неї тиск, який називають пружністю пари. Пружність пару е, як і тиск повітря, вимірюється в міліметрах ртутного стовпа або в мілібарах.
Пружність водяної пари зі збільшенням її кількості в одиниці об’єму збільшується до деякого граничного значення Е, яке відповідає стану рівноваги або насичення. Це граничне значення пружності Е називається максимально можливою пружністю водяного пару або пружністю пари, що насичує простір при даній температурі.
|
|
|
Пружність насичуючої водяної пари перш за все залежить від температури. Ця залежність показана на графіку (рис. 10.1).

Рис. 10.1. Залежність пружності насичуючої пари від температури.
Як видно із наведеного графіку, пружність насичуючої пари дуже швидко зростає зі збільшенням температури. Вона залежить також від агрегатного стану води, що випаровується (рідка вода, лід). Сили зчеплення між молекулами льоду більші, ніж між молекулами води, тому кількість частинок, що відриваються від поверхні льоду, менше, ніж кількість частинок, що відриваються від поверхні переохолодженої води при тій же температурі. Стан насичення над льодом настане при меншій пружності водяної пари. Таким чином, пружність насичуючої пари над водою більше, ніж над льодом: Ев>Ел.
У табл. 10.1. наведені значення пружності пари, що насичує простір над водою Ев і льодом Ел, при різних температурах. Із таблиці видно, що різниця пружностей при 0° дорівнює 0; з пониженням температури вона швидко збільшується, досягаючи при температурі 12° максимального значення 0,27 мб, а потім повільно зменшується. Пояснюється це тим, що при більш низьких температурах величина Ев стає дуже малою.
Таблиця 10.1
Пружність насичуючої водяної пари над льодом і над водою
(мілібари)
| t ° | -50 | -40 | -30 | -20 | -15 | -12 | -11 | -10 | -5 | -0 |
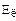
| 0,04 | 0,13 | 0,38 | 1,03 | 1,65 | 2,17 | 2,37 | 2,61 | 4,01 | 6,10 |

| 0,06 | 0,19 | 0,51 | 1,25 | 1,91 | 2,44 | 2,64 | 2,86 | 4,21 | 6,10 |
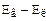
| 0,02 | 0,06 | 0,13 | 0,22 | 0,26 | 0,27 | 0,27 | 0,25 | 0,20 | 0,0 |
Окрім температури й агрегатного стану рідини, пружність насичуючої пари залежить від кривизни випаровуючої поверхні. Якщо випаровуюча поверхня випукла, наприклад поверхня краплини, то частинкам, що прагнуть вилетіти, необхідно подолати поверхневу плівку з увігнутого боку, на що потрібно менше енергії, ніж частинкам, що прагнуть повернутися, тобто долають поверхневу плівку з випуклого боку. Вилітати частинкам легше, ніж повертатися (рис. 10.2а). Якщо ж випаровуюча поверхня увігнута, то спостерігається обернена картина: вилітати частинкам трудніше, ніж повертатися (рис. 10.2в). Для плоскої поверхні умови вилітання та повернення частинок однакові (рис. 10.2б).
|
|
|
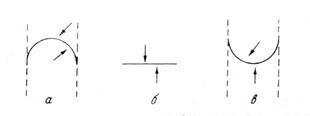
Рис. 10.2. Випаровування з випуклої, плоскої і увігнутої поверхонь рідини.
Тому пружність насичуючої пари над випуклою поверхнею Е͡ більше, а над увігнутою Е͜ менше, ніж над плоскою поверхнею Е ̲.
Е͡ >Е ̲ >Е͜ (10.1)
Це необхідно враховувати, коли питання постає про пружність насичення над краплинами хмар, туманів і дощових краплин.
У табл. 10.2 наведені відносні величини пружності насичуючої пари над краплями різних розмірів при 0°.
Таблиця 10.2
Пружність насичуючої пари над краплями по відношенню до пружності над плоскою поверхнею при різних розмірах крапель
| Радіус крапель r см | 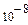
| 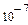
| 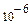
| 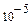
| 
|
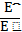
| 10,96 | 3,320 | 1,128 | 1,012 | 1,0012 |
Таким чином, насичення над поверхнею крапель досягається тільки при перенасиченні над плоскою поверхнею води; чим менше розмір краплини, тим більше його перенасичення. Наприклад, для крапель радіусом 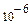 см пружність насиченої пари Е͡ складає 112% від Е ̲; але вже для крапель радіусом
см пружність насиченої пари Е͡ складає 112% від Е ̲; але вже для крапель радіусом  см вона відрізняється тільки на 0,1% від Е ̲.
см вона відрізняється тільки на 0,1% від Е ̲.
При увігнутих поверхнях пружність пари зменшується на ту ж величину. Такі увігнуті поверхні з малим радіусом кривизни зустрічаються в ґрунті, у рослин і у багатьох пористих матеріалів. Всі вищезгадані залежності відносяться до чистої води. Розчинені у воді солі значно зменшують пружність насиченої пари та тим більше, чим більше концентрація розчину.
Сили притягання молекул розчиненої речовини та молекул розчинника (води) перевершують сили притягання між молекулами чистої води. Розчинена речовина як би перешкоджає молекулам води вилітати із розчину. Внаслідок цього швидкість випаровування з поверхні розчину менше, ніж з поверхні чистої води; отже, і пружність насичуючого пару над водними розчинами менше, ніж над чистою водою.
Концентрація розчину виражається відношенням числа грам-молекул розчиненої речовини n до числа грам-молекул розчину n+n1, тобто
 , (10.2)
, (10.2)
де  - число грам-молекул розчинника.
- число грам-молекул розчинника.
|
|
|
Тоді
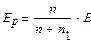 , (10.3)
, (10.3)
де 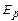 і
і 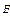 - пружність насичуючої пари над розчином і над чистою водою.
- пружність насичуючої пари над розчином і над чистою водою.
Вплив домішок помітно лише при значних концентраціях. Так, наприклад, над насиченим розчином повареної солі пружність насичуючої пари складає 82% Е, а над морською водою, що вміщує 3,7% солі, - 97,5% Е. Для річкової та дощової води вплив домішок виявляється ще меншим.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1831; Нарушение авторских прав?; Мы поможем в написании вашей работы!