
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рушійна сила масообмінних процесів
|
|
|
|
Згідно з другим законом термодинаміки стан замкненої системи при взаємодії двох фаз прямує до рівноваги, яка характеризується рівністю хімічних потенціалів компонентів фаз. Рушійною силою перенесення маси при цьому є різниця хімічних потенціалів того чи іншого компонента. Хімічні потенціали неідеальних систем визначити досить складно, тому, розраховуючи масообмінні процеси, розглядають зазвичай зміну не хімічних потенціалів, а концентрацій розподілюваного компонента, визначення яких значно простіше.
Найчастіше початкові й кінцеві робочі концентрації задано або визначають за рівнянням матеріального балансу. Зміну робочих концентрацій уздовж поверхні масообміну описують рівнянням робочих ліній. При цьому процес масопередачі відбувається самочинно за наявності різниці між робочими та рівноважними концентраціями розподілюваної речовини у фазі (за даних температури й тиску), які можна виразити через концентрації у і у* фази  , а також х і х* фази
, а також х і х* фази  .
.
Різниця між робочими й рівноважними концентраціями розподілюваної речовини у певній фазі є рушійною силою масообмінних процесів.
Рушійна сила в концентраціях фази  становить:
становить:
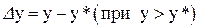
або
 ,
,
а в концентраціях фази  :
:
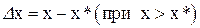
або
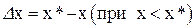 .
.
Отже, рушійна сила характеризує ступінь відхилення системи від рівноваги (при встановленні рівноваги між фазами рушійної сили немає й масопередача припиняється).
Отже, основне рівняння масопередачі можна записати двома способами:
 ,
,
або  , (26)
, (26)
а для всієї поверхні контакту фаз
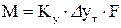 ,
,
або 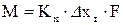 , (27)
, (27)
де 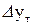 і
і  - середні рушійні сили масообмінного процесу.
- середні рушійні сили масообмінного процесу.
Індекси коефіцієнта К показують, які концентрації взято для вираження рушійної сили. Загалом 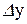

 і
і 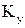

 , але, очевидно, завжди
, але, очевидно, завжди
|
|
|
 =
= . (28)
. (28)

|
Рисунок 2. Варіанти вираження рушійної сили масообмінного процесу: а – при 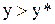 і і 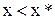 ; б - ; б - 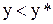 і і 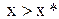 . .
|
Як видно з рисунку 2, рушійна сила зазвичай змінюється зі зміною робочих концентрацій, тому для всього процесу масообміну (або для всієї поверхні масопередачі F) треба визначити середню рушійну силу 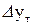 або
або  .
.
При визначенні середньої рушійної сили можливі два випадки:
1) залежність між рівноважними концентраціями (тобто рівноважна залежність) нелінійна, тобто у* = f(x), де f – загальна функціональна залежність;
2) залежність між рівноважними концентраціями є лінійною, тобто у* = 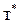 x, де
x, де 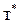 - стала величина, яка називається коефіцієнтом розподілу.
- стала величина, яка називається коефіцієнтом розподілу.
Розглянемо випадок, коли рівноважна залежність нелінійна: у* = f(x).
Вважаємо, що апарат працює за прямотечійною схемою при ідеальному витисканні, переході речовини з фази  у фазу
у фазу  (тобто
(тобто 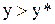 ) і практично постійних значеннях G i L (рисунок 3).
) і практично постійних значеннях G i L (рисунок 3).

|
| Рисунок 3. До визначення середньої рушійної сили масообмінних процесів. |
Для елемента поверхні dF справедливо:
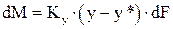 і
і 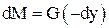 ,
,
тоді
 .
.
Після інтегрування у границях 0 – F і 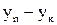 маємо:
маємо:
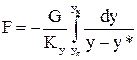 .
.
Враховуючи, що 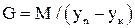 , отримаємо:
, отримаємо:
 . (29)
. (29)
 . (30)
. (30)
Виражаючи рушійну силу через концентрацію х, отримаємо:
 . (31)
. (31)
Порівнюючи рівняння (30) і (31) з (27), можна записати залежності для визначення середньої рушійної сили масообмінного процесу:
 ; (32)
; (32)
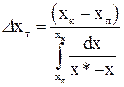 . (33)
. (33)
Інтеграл у рівнянні (32) (або в (33)) обчислюють аналітично, числовим або графічним інтегруванням. Так, при графічному інтегруванні у границях концентрацій  через певні інтервали для ряду значень робочих концентрацій у і х знаходять відповідні їм значення у* і величину 1/(у-у*). Побудувавши далі залежність 1/(у-у*)=φ(у), враховуючи масштаби по осях, знаходять площу під кривою, обмеженою абсцисами
через певні інтервали для ряду значень робочих концентрацій у і х знаходять відповідні їм значення у* і величину 1/(у-у*). Побудувавши далі залежність 1/(у-у*)=φ(у), враховуючи масштаби по осях, знаходять площу під кривою, обмеженою абсцисами 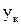 і
і  , яка становить значення шуканого інтегралу.
, яка становить значення шуканого інтегралу.
Тепер розглянемо випадок, коли рівноважна залежність лінійна, тобто у*=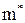 x.
x.
Тоді для умов у = тx і у* = 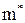 x маємо:
x маємо:
|
|
|
 ,
,
а інтеграл у рівнянні (32) набуває вигляду

Різницю  у рівнянні (32) подамо так:
у рівнянні (32) подамо так:
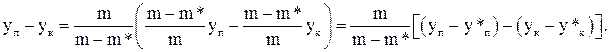
Тоді залежність (44) для визначення середньої сили набуде вигляду:
 або
або 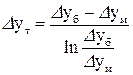 , (34)
, (34)
де 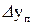 і
і  - рушійна сила на початку та в кінці поверхні контакту фаз.
- рушійна сила на початку та в кінці поверхні контакту фаз.
При 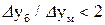 , де
, де 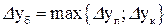 і
і  середню рушійну силу можна обчислити як середнє арифметичне:
середню рушійну силу можна обчислити як середнє арифметичне:
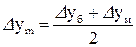 ,
,  (35)
(35)
Аналогічно можна отримати співвідношення і для  :
:
 (36)
(36)
Інтеграли у знаменниках залежностей (32) і (33) називаються числами одиниць переносу (ЧОП):
 ; (37)
; (37)
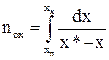 . (38)
. (38)
Число одиниць переносу характеризує зміну робочої концентрації розподілюваної речовини в даній фазі, яка припадає на одиницю рушійної сили.
ЧОП визначають через середню рушійну силу:
 ; (39)
; (39)
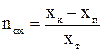 . (40)
. (40)
Якщо лінія рівноваги – пряма, то ЧОП визначають так:
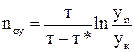 ;
;  . (41)
. (41)
| Коментар: |
Модифікування основного рівняння масопередачі
У багатьох масообмінних процесах визначення поверхні контакту фаз досить складне. Тому при розрахуванні відповідного технологічного обладнання вдаються до різних прийомів, які дозволяють проектувати це обладнання, обминаючи необхідність визначення поверхні контакту фаз. У цьому випадку основною технологічною характеристикою апарата можна вважати об’єм V або висоту Н його контактної частини.
Якщо основною характеристикою апарата беремо об’єм контактної частини, то поверхню контакту фаз F можна визначити так:
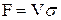 , (42)
де , (42)
де 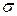 - питома поверхня контакту фаз (тобто поверхня фазового контакту, що розвивається в 1 м3 апарата), м2/м3.
Тоді, враховуючи, що згідно з основним рівнянням масопередачі F=M/(Ky Δym), рівняння (43) набуває вигляду: - питома поверхня контакту фаз (тобто поверхня фазового контакту, що розвивається в 1 м3 апарата), м2/м3.
Тоді, враховуючи, що згідно з основним рівнянням масопередачі F=M/(Ky Δym), рівняння (43) набуває вигляду:
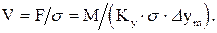 (43)
Добуток (43)
Добуток  називається об’ємним коефіцієнтом масопередачі називається об’ємним коефіцієнтом масопередачі 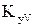 .
Розмірність .
Розмірність 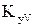 становить: становить:
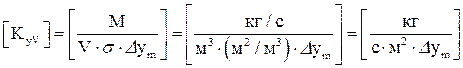 .
Остаточно модифіковане основне рівняння масопередачі для фаз .
Остаточно модифіковане основне рівняння масопередачі для фаз  і і  набуває вигляду: набуває вигляду:
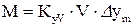 ; ; 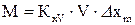 . (44)
Якщо основною характеристикою апарата беремо висоту його контактної частини Н, то поверхню контакту фаз F можна виразити так: . (44)
Якщо основною характеристикою апарата беремо висоту його контактної частини Н, то поверхню контакту фаз F можна виразити так:
 , (45)
де S – площа поперечного перерізу контактної частини апарата.
У цьому разі модифіковане основне рівняння масопередачі набуває вигляду: , (45)
де S – площа поперечного перерізу контактної частини апарата.
У цьому разі модифіковане основне рівняння масопередачі набуває вигляду:
 ; ; 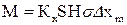 . (46)
або . (46)
або
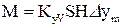 ; ;  . (47)
З рівнянь (45) і (46) або (47) визначають відповідно об’єм V і висоту Н контактної частини апарата (при відомому діаметрі). . (47)
З рівнянь (45) і (46) або (47) визначають відповідно об’єм V і висоту Н контактної частини апарата (при відомому діаметрі).
|
Закон молекулярної дифузії (перший закон Фіка)
Одним із основних законів масообміну є закон молекулярної дифузії.
|
|
|
Дифузією називається перенесення частинок різної природи, обумовлене хаотичним рухом молекул (атомів) в одно- чи багатокомпонентних газових або конденсованих середовищах (рідинах і твердих тілах).
| Коментар: |
| Дифузія (від лат. diffusio – розповсюдження, розтікання, розсіювання). |
Кінетика перенесення в цьому разі підлягає першому закону Фіка: маса речовини, що продифундувала, пропорційна градієнту концентрації, площині, перпендикулярній напрямку дифузійного потоку, і часу:
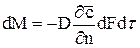 , (48)
, (48)
де 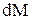 - кількість речовини, що продифундувала;
- кількість речовини, що продифундувала;
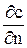 - градієнт концентрації в напрямку дифузії.
- градієнт концентрації в напрямку дифузії.
Для всієї поверхні дифузії F перший закон Фіка набуває вигляду:
 , (49)
, (49)
де п – довжина шляху речовини, що дифундує (знак „мінус” обумовлено зменшенням градієнта концентрації в напрямку дифузії речовини).
Коефіцієнт молекулярної дифузії D залежить від природи речовини, що дифундує, і характеризує здатність останньої проникати в певне середовище. Його розмірність становить:
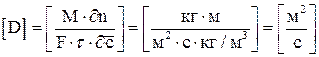 ,
,
тобто коефіцієнт молекулярної дифузії показує, яка маса речовини дифундує за одиницю часу крізь одиницю поверхні при градієнті концентрації, що дорівнює одиниці.
Значення D знаходять у довідниках або розраховують.
Наприклад:
- для газів:
 , (50)
, (50)
- для рідин:
 , (51)
, (51)
де Т – абсолютна температура, К; р – тиск, Па; VA i VB – молярні об’єми речовин, які взаємодіють,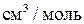 ; МА і МВ – молярні маси речовин, кг/моль;
; МА і МВ – молярні маси речовин, кг/моль;  - в’язкість рідин, у якій відбувається дифузія, Па·с.
- в’язкість рідин, у якій відбувається дифузія, Па·с.
Отже, коефіцієнт дифузії підвищується зі збільшенням температури, а для газів – також і зі зменшенням тиску. При цьому для рідин коефіцієнт дифузії приблизно на чотири порядки менший, ніж для газів.
Диференціальне рівняння молекулярної дифузії (другий закон Фіка)
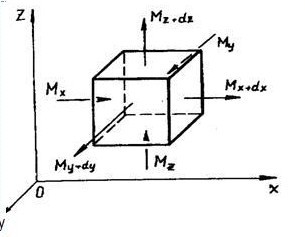
Виділимо в нерухомому або такому, що рухається ламінарно, потоці елементарний паралелепіпед з ребрами дх, ду і дz (рисунок 4).
|
| Рисунок 4. До виведення диференціального рівняння молекулярної дифузії. |
|
 Якщо крізь цей паралелепіпед за рахунок молекулярної дифузії переміщується розподілювана речовина, то крізь ліву, задню й нижню грані за час
Якщо крізь цей паралелепіпед за рахунок молекулярної дифузії переміщується розподілювана речовина, то крізь ліву, задню й нижню грані за час 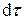 в нього входить речовина у кількості
в нього входить речовина у кількості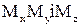 , а крізь протилежні грані — праву, передню й верхню, - речовина виходить у кількості відповідно
, а крізь протилежні грані — праву, передню й верхню, - речовина виходить у кількості відповідно 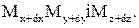 Отже, за час
Отже, за час 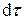 елемент здобуває речовину, що дифундує, у кількості
елемент здобуває речовину, що дифундує, у кількості|
|
|
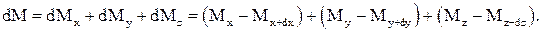
Згідно з першим законом Фіка:
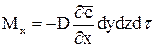 ;
;
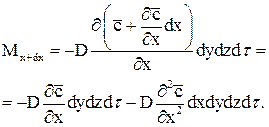
Отже

Аналогічно можна отримати відповідні прирости кількості речовини в напрямках у і z.
Додаючи ліві та праві частини отриманих рівностей, маємо:
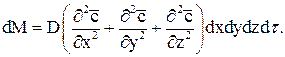 (52)
(52)
З другого боку, той самий приріст кількості речовини в елементі дорівнює добутку об'єму елемента 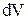 на зміну концентрації речовини за час
на зміну концентрації речовини за час 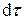 :
:
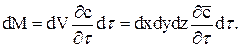 (53)
(53)
Порівнюючи рівності (52) і (53), отримуємо диференціальне рівняння молекулярної дифузії:
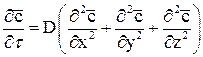 (54)
(54)
або
 . (55)
. (55)
Масовіддача. Рівняння масовіддачі (закон Щукарєва)
Процес перенесення речовини з ядра потоку до межі поділу фаз або навпаки називається масовіддачею. Масовіддача, як і конвекція, буває природна й вимушена. При природній масовіддачі рух рідини виникає внаслідок різниці густин у різних точках газу, пари або рідини, а при вимушеній - унаслідок витрат енергії на рух потоку (насосами, мішалками тощо).
За аналогією з емпіричним рівнянням тепловіддачі рівняння масовіддачі (закон Щукарєва) має такий вигляд:
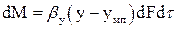 , (56)
, (56)
де 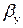 - коефіцієнт масовіддачі;
- коефіцієнт масовіддачі;  - концентрація на межі поділу фаз.
- концентрація на межі поділу фаз.
При сталому процесі для всієї поверхні F і τ =1 рівняння (68) для фаз 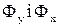 набуває вигляду:
набуває вигляду:
 ;
; 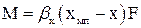 . (57)
. (57)
Отже, кількість речовини, перенесеної від межі поділу фаз у фазу (або навпаки), пропорційна різниці концентрацій біля поверхні поділу фаз і в ядрі потоку фази (або навпаки), поверхні фазового контакту й часу. При цьому концентрацію на межі поділу фаз ( або
або 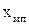 ) розглядають як рівноважну:
) розглядають як рівноважну:
Розмірність коефіцієнта масовіддачі, наприклад, становить:
 ,
,
тобто коефіцієнт масовіддачі показує, яка маса (або кількість) речовини переходить від одиниці поверхні поділу фаз у ядро потоку (або навпаки) за одиницю часу при рушійній силі, що дорівнює одиниці.
Коефіцієнт масовіддачі характеризує кінетику процесу перенесення речовини в окремій фазі й залежить від фізичних властивостей фази та її гідродинамічного стану (коефіцієнт же масопередачі характеризує кінетику процесу перенесення речовини з однієї фази в іншу крізь межу поділу фаз, тобто по всій системі в цілому).
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 4252; Нарушение авторских прав?; Мы поможем в написании вашей работы!