
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Спектр атома водорода
|
|
|
|
Используя теорию Бора и схему энергетических уровней атома, легко объяснить процессы испускания и поглощения излучения атомом.
Чтобы атом получил возможность испускать свет, его нужно возбудить, т.е. перевести электрон на более высокий энергетический уровень (нагреванием, освещением и т.д.). В возбужденном состоянии атом неустойчив и через t~ 10-8 c переходит на более близкую к ядру орбиту, испуская квант электромагнитного излучения (фотон) с энергией  .
.
Согласно второму постулату Бора (для водорода  )
)

 , (1)
, (1)
где  – постоянная Ридберга.
– постоянная Ридберга.
 Исследования спектров излучения разряженных газов (т.е. отдельных атомов) показали, что каждому газу присущ определенный линейчатый спектр (рис. 4). Все обнаруженные серии в спектре атома водорода могут быть описаны одной эмпирической формулой, называемой обобщенной формулой Бальмера:
Исследования спектров излучения разряженных газов (т.е. отдельных атомов) показали, что каждому газу присущ определенный линейчатый спектр (рис. 4). Все обнаруженные серии в спектре атома водорода могут быть описаны одной эмпирической формулой, называемой обобщенной формулой Бальмера:
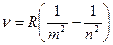 . (2)
. (2)
Для серии Лаймана (ультрафиолетовая область спектра) (рис. 2) m =1, n= 2,3,4,…
Для серии Бальмера (видимая область спектра) m =2, n =3,4,5,…
Для серии Пашена (инфракрасная область спектра) m =3, n =4,5,6,…
Значения R в формулах (1) и (2) совпадают, что свидетельствует о правильности полученной Бором формулы (1).
Теория Бора, на основе которой были рассмотрены спектры атома водорода и водородоподобных систем и вычислены частоты спектральных линий, не смогла объяснить интенсивности спектральных линий, вероятности возможных переходов и не позволила описать спектр атома гелия – одного из простейших атомов. Все эти проблемы были решены в рамках квантовой механики.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2053; Нарушение авторских прав?; Мы поможем в написании вашей работы!