
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гидроксильная (спиртовая, фенольная)
|
|
|
|
Лекция № 14
Тема «Качественные реакции на функциональные группы»
План:
1) Гидроксильная (спиртовая, фенольная)
2) Карбонильная (альдегидная, карбоксильная, сложно-эфирная)
3) Первичная ароматическая аминогруппа, третичная аминогруппа(третичный азот)
4) Имидная, сульфамидная.
Функциональные группы (ФГ)- это связанные с углеродным радикалом отдельные атомы или группы атомов, которые вследствие своих характерных свойств могут быть использованы определения лекарственных веществ.
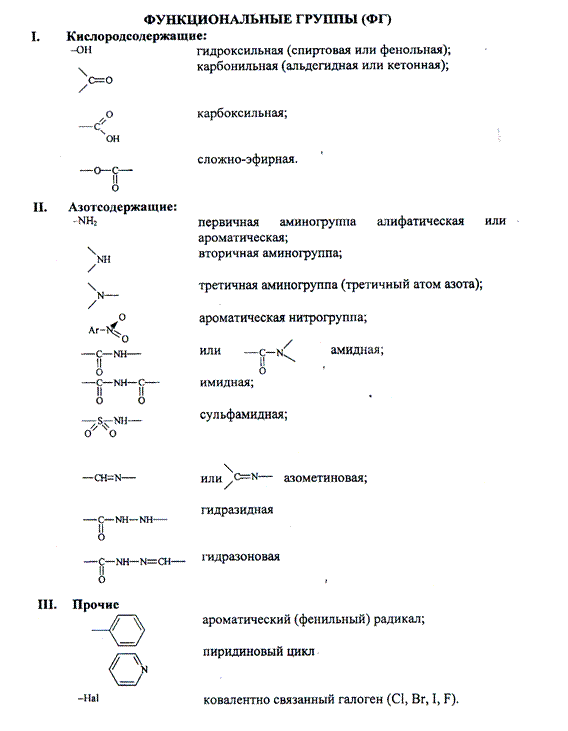
I. Спиртовой гидроксил. Alr-OH - это гидроксил, связанный с алифатическим углеводородным радикалом.
Его содержат ЛВ группы спиртов (спирт этиловый и глицерин); карбоновых кислот и их солей (кальция лактат, глюконат и др.); терпенов (ментол, терпингидрат); производных фенилалкиламинов (эфедрина гидрохлорид, мезатон,адреналин);
На основе спиртового гидроксила в анализе содержащих его ЛВ используются следующие реакции:
-этерификации (образования с кислотами или их ангидридами сложных эфиров);
- окисление до альдегидов, а в некоторых случаях и до кислот;
- комплексообразование с ионами меди (II) в щелочной среде.
1.Реакция этерификации в присутствии водоотнимающих средств с кислотами или их ангидридами. Основана на свойстве спиртов образовывать сложные эфиры. В случае низкомолекулярных соединений эфиры обнаруживают по запаху, при анализе ЛВ с высокой молекулярной массой – по температуре плавления.
Реакция этерификации является фармакопейной для спирта этилового.
CH3CH2OH + CH3COOH H2SO4 → CH3CH2OCOCH3
2. Реакция окисления, основана на свойстве спиртов окисляться до альдегидов, которые обнаруживают по запаху. В качестве реагентов используют различные окислители: калия перманганат, калия бихромат, гексацианоферрат (III) калия и др. Наибольшую аналитическую ценность имеет калия перманганат, который, восстанавливаясь, меняет степень окисления от +7 до + 2 и обесцвечивается, т.е. делает реакцию эффектной.
|
|
|
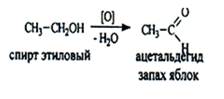
Реакция комплексообразования, основанная на свойстве спиртов образовывать окрашенные комплексные соединения с сульфатом меди (II) в щелочной среде.
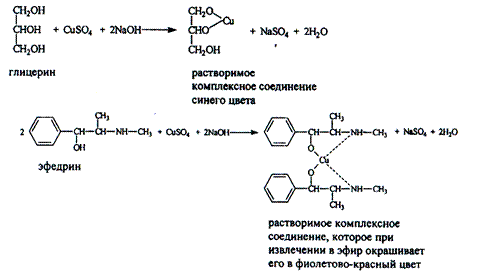
Используется для идентификации многоатомного спирта – глицерина и эфедрина гидрохлорида, в котором кроме спиртового гидроксила участвует в комплексообразовании и вторичная аминная группа.
Фенольный гидроксил - это гидроксил, связанный с ароматическим радикалом. Его содержат ЛВ группы фенолы (фенол, резорцин); фенолокислот и их производных (кислота салициловая, фенилсалицилат, салициламид, оксафенамид); производные фенантренизохинолина (морфин гидрохлорид, апоморфин); синестрол, адреналин, мезатон и др.
Химические свойства соединений, содержащих фенольный гидроксил, обусловлены взаимодействием электронной пары с π – электронами ароматического кольца. Это взаимодействие приводит к смещению электронной плотности с ОН- – группы на кольцо, нарушения в нем равномерности распределения электронов, созданию избыточного отрицательного заряда в орто- и пара- положениях. Атом водорода гидроксигруппы ионизирует и придает фенолам слабые кислотные свойства, которые однако редко используются в анализе. наибольшее значение имеют реакции электрофильного замещения водородов в о- и n- положениях ароматического кольца.
На основе свойств фенольного гидроксила используются следующие реакции:
- комплексообразования;
- бромирования;
- азосочетания;
- окисления;
- образования индофенолового красителя;
- конденсации
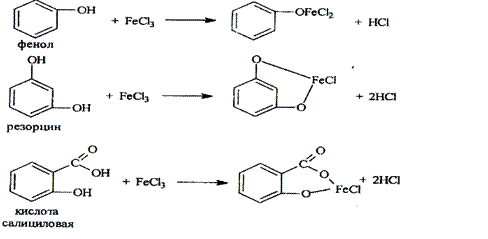
1. Реакции комплексообразования фенольного гидроксила с ионами железа (III). Основана на свойствах фенольного гидроксила образовывать растворимые комплексные соединения, окрашенные чаще в синий (фенол) или фиолетовый цвет (резорцин, кислота салициловая), реже в красный (ПАСК – натрия) и зеленый (хинозол).
|
|
|
Состав комплекса, а, следовательно, и их окраска обусловлены количеством фенольных гидроксилов (фенол – синее, резорцин – фиолетовое), и влиянием других функциональных групп.
Реакция рекомендована фармакопеей для большинства соединений, содержащих фенольный гидроксил.
2. Реакция бромирования ароматического кольца. Основана на электрофильном замещении водорода в о- и n- положении на бром с образованием нерастворимого бромопроизводного.
 Основные правила бромирования
Основные правила бромирования
- бром замещает водород в о- и n- положении по отношению к фенольному гидроксилу (наиболее рационноспособное n – положение):
 - при наличии в о- или n- положениях ароматического кольца заместителей в реакцию вступает меньше атомов брома:
- при наличии в о- или n- положениях ароматического кольца заместителей в реакцию вступает меньше атомов брома:
 - если в о- или n- положениях находиться карбоксильная группа, то при наличии избытка брома происходит декарбоксилирование и образование трибромпроизводного:
- если в о- или n- положениях находиться карбоксильная группа, то при наличии избытка брома происходит декарбоксилирование и образование трибромпроизводного:
- если заместитель находится в м- положении, то он не препятствует образованию трибромпроизводного:
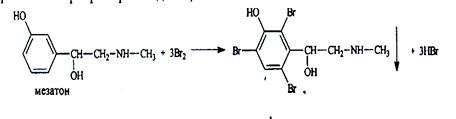
- если в соединении содержится два фенольных гидроксила в м- положении, то в результате их согласной ориентации образуется трибромпроизводное
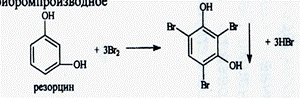
-
если две гидроксильные группы расположены в о- или n- положении друг к другу, то они действуют несогласованно: бромирование не происходит:
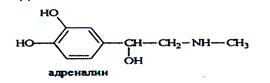
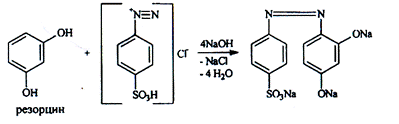
3.Реакция азосочетания фенолов с диазореактивом (диазотированная сульфаниловая кислота) с образованием азокрасителя, окрашенного в оранжево-красный цвет.
4. Реакция окисления. Фенолы могут окисляться до различных соединений, но чаще всего до хинонов окрашенных в розовый или реже в желтый цвет.
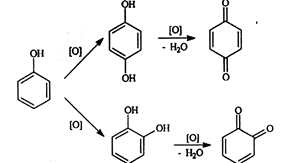
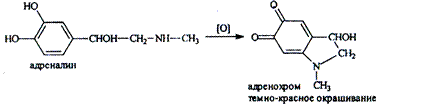
В частности, реакция окисления рекомендована ГФ для адреналина и норадреналина: в качестве окислителя используется йод при определенном pH среды. При этом образуются окрашенные продукты адренохром и норадренохром.
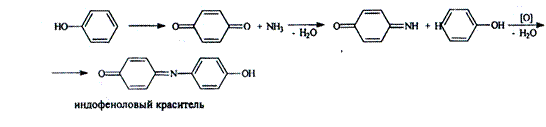
5. Реакция образования индофенолового красителя. Основана на окислении фенолов до хинонов, которые при конденсации с аммиаком или аминопроизводными и избытком фенола образуют индофеноловый краситель, окрашенный в фиолетовый цвет.
|
|
|
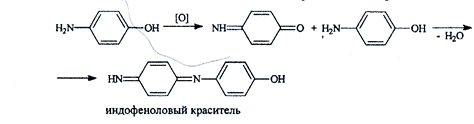
ГФ X рекомендует эту реакцию для идентификации фенацетина и парацетамола, которые, гидролизуясь, выделяют n-аминофеол, обнаруживаемый реакцией образования индофенолового красителя.
6. Реакция конденсации с альдегидами или ангидридами кислот:
С формальдегидом в присутствии концентрированной серной кислоты с образованием ауриноваго (арилметанового) красителя окрашенного в красный цвет.
Реакция является фармакопейной для кислоты салициловой.
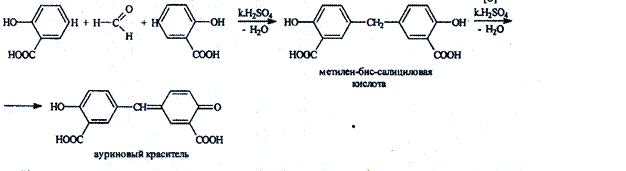
Концентрированная серная кислота на первой стадии реакции играет роль водоотнимающего средства, на второй – является окислителем.
Химизм реакции на резорцин
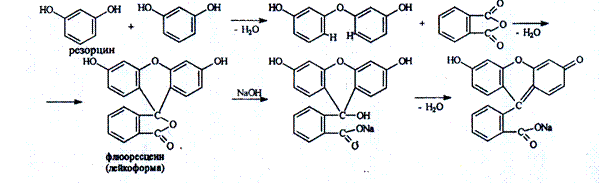
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 27984; Нарушение авторских прав?; Мы поможем в написании вашей работы!