
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Отсюда концентрация вещества в приповерхностном слое равна
|
|
|
|
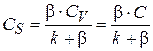 . (11)
. (11)
Подставив выражение (11) в уравнение (10), получим выражение для скорости химической реакции:
 , (12)
, (12)
где k 1 - константа скорости реакции в целом (макроскопическая константа скорости реакции).
В стационарных условиях макроскопическая скорость реакции соответствует уравнению реакции первого порядка по концентрации реагирующего вещества.
Очевидно, что
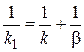 (13)
(13)
Проанализируем уравнение (13).
Если скорость диффузии значительно превосходит скорость собственно химической реакции (b» k), то из уравнения (13) имеем
k 1» k
т. е. в стационарных условиях скорость всей реакции определяется скоростью собственно химической реакции. Процесс протекает в кинетическойобласти. Энергия активации реакций в этом случае обычно составляет значения более 60 кДж/моль (рис. 3). Значения концентраций CV и CS мало отличаются друг от друга.
Если скорость собственно химической реакции значительно превышает скорость диффузии, т. е. (k» b), то из уравнения (13) имеем
k 1» b.
Лимитирующей стадией процесса в этом случае является диффузия реагирующего вещества к поверхности раздела фаз. Энергия активации в этой области составляет менее 10 кДж/моль. Процесс протекает в диффузионной области.
Существует и переходная область, для которой скорости реакции и диффузии соизмеримы между собой (рис. 3).
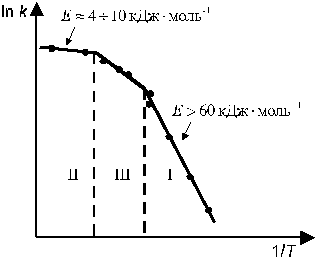 |
Рис. 3. Области протекания гетерогенных химических процессов.
I — кинетическая, II — диффузионная, III — переходная области
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 249; Нарушение авторских прав?; Мы поможем в написании вашей работы!