
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Нормирование качества воды в водоемах
|
|
|
|
Классификация примесей и их влияние на гидробионты.
Свойства, классификация и ресурсы вод.
ЗАЩИТА ВОДНОГО БАССЕЙНА
ЛЕКЦИЯ 16.
План лекции:
1. Свойства, классификация и ресурсы вод.
2. Классификация примесей и их влияние на гидробионты.
3. Нормирование качества воды в водоемах.
4. Методы контроля качества воды.
5. Расчет допустимого состава сточных вод.
6. Количественные оценки водопотребления и водоотведения.
Вода играет решающую роль во многих процессах, протекающих в природе, и в обеспечении жизни человека. В промышленности воду используют как сырье и источник энергии, как хладоагент, растворитель, экстрагент, для транспортирования сырья и материалов и др. целей.
Особенностью внутреннего строения молекулы воды является несимметричное расположение атомов водорода относительно атома кислорода. В результате этого внутримолекулярные силы компенсируются не полностью, и их избыток проявляется вне молекулы. В силу асимметричного распределения положительных и отрицательных зарядов молекула воды обладает ярко выраженной полярностью, значительно превосходящей разделение зарядов у других веществ. Этим объясняется хорошая способность воды растворять многие вещества.
Вода - наилучший растворитель для многих газов, жидкостей и твердых соединений. В то же время вода химически не изменяется под действием большинства соединений, т.к. является инертным растворителем. Этим обеспечивается полноценное питание живых существ и возможность многократного использования в природе и технологических процессах.
Вода обладает наибольшим поверхностным натяжением из всех известных жидкостей, за исключением ртути. Это свойство обусловливает возможность движения воды в стеблях растений, стволах деревьев, движение крови в тончайших сосудах организмов.
|
|
|
Химически чистая вода обладает следующими физическими свойствами: плотность при температуре 0°С - 1 г/см3, температура плавления - 0°С, температура кипения - 100°С, не обладает запахом и вкусом. Наибольшую плотность вода приобретает при температуре около 4°С, при замерзании увеличивает объем примерно на 10%.
Ресурсы воды. Общее количество природной воды на земле составляет 1386 млн. км3. В основном (свыше 97,5 %) - это соленые воды. Количество пресной воды - 35 млн. км3. Подавляющая часть пресной воды является труднодоступной для людей, так как она в основном находится в полярных ледниках и водоносных слоях под землей. В России запас пресных поверхностных вод составляет 40,5 тыс. км. Объем потребления пресной воды в мире достигает приблизительно 3900 км3/год. Около половины этого количества потребляется безвозвратно, а другая половина превращается в сточные воды.
Природная вода - это вода, которая качественно и количественно формируется под влиянием естественных процессов при отсутствии антропогенного воздействия. Ее качественные показатели находятся на естественном среднемноголетнем уровне. Классификация воды в зависимости от степени минерализованности приведена на рисунке 1.

Рисунок 1. Классификация вод
По преобладающему аниону все воды делятся на гидрокарбонатные, сульфатные и хлоридные.
Жесткость природных вод обуславливается присутствием в них солей кальция и магния и выражается концентрацией ионов Са2+ и Мg2+ в ммоль-экв/л. Различают общую, карбонатную и некарбонатную жесткость. Общая жесткость представляет собой сумму двух последних, карбонатная связана с присутствием в воде бикарбонатов кальция и магния, а некарбонатная - сульфатов, хлоридов, нитратов кальция и магния.
|
|
|
Сточные воды. В производстве образуются различные категории сточных вод.
Сточная вода - это вода, бывшая в бытовом, производственном или сельскохозяйственном употреблении, а также прошедшая через какую-либо загрязненную территорию. В зависимости от условий образования сточные воды делятся на бытовые или хозяйственно-фекальные (БСВ), поверхностные и производственные (ПСВ).
Бытовые сточные воды предприятий образуются при эксплуатации на его территории душевых, туалетов, прачечных, столовых. Они содержат примеси, из которых примерно 58% органических веществ и 42% минеральных. Предприятие не отвечает за качество данных сточных вод и направляет их на городские или районные станции очистки.
Поверхностные сточные воды образуются в результате смывания дождевой, талой, поливочной водой примесей, скапливающихся на территории, крышах и стенах производственных зданий. Основными примесями этих вод являются твердые частицы, нефтепродукты, органические и минеральные удобрения. Каждое предприятие отвечает за загрязнение водоемов, поэтому необходимо знать объем сточных вод данного типа.
Расход сточных вод рассчитывают по методу предельной интенсивности в соответствии со СНиП 2.04.03-85. "Нормы проектирования, канализация, наружные сети и сооружения".
Производственные сточные воды. Они образуются в результате использования воды в технологических процессах. Их количество, состав и концентрация примесей определяется типом предприятия, его мощностью, видами используемых технологических процессов. В технологических процессах источниками сточных вод являются:
1. воды, образующиеся при протекании химических реакций (они загрязнены исходными веществами и продуктами реакций);
2. воды, находящиеся в виде свободной и связанной влаги в сырье и исходных продуктах и выделяющиеся в процессе переработки;
3. промывные воды после промывки сырья, продуктов и оборудования;
4. маточные водные растворы;
5. водные экстракты и абсорбенты;
6. воды охлаждения.
Для обеспечения промышленных предприятий нашей страны ежегодно забирается из естественных источников водоснабжения примерно 100 млрд. м3 воды, при этом 90% этого количества возвращается обратно в водоемы с различной степенью загрязненности. Около 10% общего водопотребления приходится на машиностроительные предприятия, где воду используют для следующих целей:
|
|
|
1. охлаждение или подогрев исходных материалов и продукции, деталей и узлов технологического оборудования;
2. приготовление различных технологических растворов;
3. промывку, обогащение и очистку исходных материалов или продукции;
4. хозяйственно-бытовое обслуживание
.
Химически чистой воды в природе нет. Даже дистиллированная вода содержит микросоединения и растворенные углекислоту, азот, кислород.
Природные воды являются сложными дисперсными системами, содержащими большое количество разнообразных минеральных и органических примесей. Дисперсной системой называют систему, которая состоит из очень мелких частичек распределенного вещества. При нахождении частичек в молекулярно-растворенном состоянии или в виде ионов система называется истинным раствором. Это, как правило, гомогенная, т.е. не имеющая внутренних поверхностей раздела, система. При наличии внутренних поверхностей раздела (гетерогенная система) в зависимости от степени раздробленности примеси образуют коллоидные растворы или взвеси.
В природных водах наряду с неорганическими соединениями почти всегда присутствуют сложные органические вещества. Наиболее распространенными органическими примесями являются гумусовые вещества, придающие воде окраску. Гумусовые вещества представляют комплекс органических веществ - продуктов конденсации ароматических соединений фенольного типа с аминокислотами и протеинами. В природных водах гумусовые вещества представлены фульвокислотами и гуминовыми кислотами, а также их солями.
Присутствие в природных водах органических соединений обусловливает цветность, запах и привкус воды, изменение физических показателей по прозрачности, преломлению света, снижению поверхностного натяжения, изменению способности растворять кислород.
Это дало основание акад. Л.А. Кульскому предложить классификацию примесей воды по их фазово-дисперсному состоянию.
|
|
|
Сущность классификации заключается в том, что все примеси воды по их отношению к дисперсионной среде объединены в четыре группы с общей для них физико-химической характеристикой. Примеси первых двух групп образуют термодинамически неустойчивые гетерогенные системы, а примеси двух других групп - термодинамически равновесные и обратимые гомогенные системы. Связь между техникой очистки воды и принадлежностью удаляемых примесей и загрязнений к той или иной группе классификации определяется общими закономерностями, которым подчиняются процессы, происходящие в водной среде в зависимости от физико-химической характеристики этих примесей.
Примеси первой группы, к которым относятся грубодисперсные вещества, образующие с водой суспензии, эмульсии, пены, а также планктон и патогенные бактерии - кинетически неустойчивы, удерживаются во взвешенном состоянии динамическими силами потока. Попадают такие вещества в водоемы в результате размыва пород, смыва почв, со сточными водами. Наиболее часто эти примеси представлены частицами глины, песка, почвы, ила, а также эмульсиями минеральных масел, нефтепродуктами и т.п. На поверхности частиц сорбируются патогенные бактерии, вирусы и т.п. В состоянии покоя для таких систем характерно осаждение (седиментация) частиц или всплытие в зависимости от их плотности. Примеси группы 1 эффективно удаляются под действием сил гравитации, сил прилипания (адгезии).
Таблица 1
Классификация примесей воды
| Фазовая характеристика | Системы | |||
| гетерогенные | гомогенные | |||
| Группа | I | II | III | IV |
| Физико-химическая характеристика | Грубодисперсные примеси: суспензии, эмульсии, планктон, патогенные микроорганизмы | Примеси коллоидной степени дисперсности, органические, неорганические вещества, вирусы | Примеси молекулярной степени дисперсности: газы, органические вещества | Примеси ионной степени дисперсности: соли, кислоты, основания |
| Поперечный размер частицы, см | 10-1-10-5 | 10-6 | 10-7 | 10-8 |
Примеси второй группы представляют собой коллоидные растворы, состоящие из гуминовых и фульвокислот, высокомолекулярных соединений естественного происхождения и попадающих со сточными водами, вирусы и другие микроорганизмы коллоидной степени дисперсности. Примеси второй группы образуют с водой кинетически и агрегативно устойчивые системы. Кинетически устойчивость данных примесей характеризуется соотношением сил гравитационного поля и броуновского движения, примеси практически не оседают, время седиментации измеряется годами. Эти примеси удаляются в результате коагуляции, сорбции, воздействия окислителей.
Примеси третьей группы - растворенные газы, органические соединения биологического происхождения, соединения в производственных и бытовых стоках. Это, как правило, неэлектролиты или слабые электролиты: фенолы, его производные, амины, нитросоединения.
Молекулы примесей третьей группы могут существенно изменять структуру воды и взаимодействовать и с ней, и друг с другом. В первом случае происходит гидратация молекул, во втором - ассоциация. Исключая случай образования химических соединений, эти взаимодействия в основном обусловлены силами Ван-дер-Ваальса.
Молекулярно-растворенные вещества способны за счет водородных связей образовывать с водой непрочные соединения, существующие лишь в растворе. Большое значение имеют эти связи при ассоциации молекул растворенного вещества, необходимым условием возникновения таких связей является достаточная полярность валентных связей водорода в исходных веществах.
Примеси четвертой группы образуются в результате диссоциации в воде солей, кислот, оснований. Примеси этой группы удаляются из воды в результате образования малорастворимых или малодиссоциированных соединений.
Природные воды отличаются от водных растворов минеральных и органических веществ присутствием сложных сообществ живых организмов и концентрацией химически активных частиц и соединений. С участием этих организмов и частиц осуществляется синтез и разрушение органических веществ, преобразование их форм и миграция химических элементов.
Водоем как водный источник связан с окружающей его природной средой. На него оказывают влияние условия формирования поверхностного и подземного стока, разнообразные природные явления, индустрия, промышленное и коммунальное строительство, транспорт, хозяйственна и бытовая деятельность человека. Последствием этих влияний является привнесение в водную среду новых не свойственных ей веществ - загрязнителей, ухудшающих качество воды. При этом возможно химическое, физическое и биологическое загрязнение воды и водоемов.
Химическое загрязнение представляет собой изменение естественных химических свойств воды за счет увеличения содержания в ней вредных примесей как неорганической, так и органической природы.
Физическое загрязнение связано с изменением параметров водной среды и определяется тепловыми, механическими, радиоактивными примесями.
Биологическое загрязнение заключается в изменении свойств воды в результате увеличения количества не свойственных ей видов микроорганизмов, растений и животных, привнесенных извне.
Основными неорганическими загрязнителями пресных и морских вод являются разнообразные химические соединения, токсичные для обитателей водной среды.
Тяжелые металлы поглощаются фитопланктоном, а затем передаются по пищевой цепи более высокоорганизованным организмам. Токсический эффект некоторых наиболее распространенных загрязнителей гидросферы представлен в таблице 2.
Таблица 2
Степень токсичности ряда загрязняющих веществ
| Вещество | Планктон | Ракообразные | Моллюски | Рыбы |
| Соли тяжелых металлов | ||||
| Медь | +++ | +++ | +++ | +++ |
| Ртуть | ++++ | +++ | +++ | +++ |
| Свинец | - | + | + | +++ |
| Цинк | + | ++ | ++ | ++ |
| Кадмий | - | ++ | ++ | ++++ |
| Неорганические вещества | ||||
| Хлор | - | +++ | ++ | +++ |
| Цианид | - | +++ | ++ | ++++ |
| Фтор | - | - | + | +++ |
| Сульфид | - | ++ | + | +++ |
Кроме перечисленных в таблице веществ, к опасным загрязнителям водной среды можно отнести неорганические кислоты и основания. Они обусловливают широкий диапазон рН водной среды промышленных стоков (1,0-11,0) и способны изменять рН водной среды ниже 5,0 и выше 8,0, тогда как рыба в пресной и морской воде может существовать только в интервале рН 5,0-8,5.
Нормирование качества воды рек, озер и водохранилищ проводят в соответствии с "Санитарными правилами и нормами охраны поверхностных вод от загрязнения" (1988 г). Эти правила устанавливают две категории водоемов (или их участков):
1. водоемы питьевого и культурно-бытового назначения;
2. водоемы рыбо-хозяйственного назначения.
Состав и свойства воды водных объектов первого типа должны соответствовать нормам в створах, расположенных в водотоках на расстоянии 1 км выше ближайшего по течению, а в не проточных водоемах - в радиусе одного километра от пункта водопользования. Состав и свойства воды в рыбохозяйственных водоемах должен соответствовать нормам в месте выпуска сточных вод при рассеивающем выпуске (наличие течений), а при отсутствии рассеивающего выпуска - не далее, чем в 500 м от места выпуска.
Нормируемые значения параметров воды водоемов:
1. Содержание плавающих примесей и взвешенных веществ;
2. Запах, привкус, окраска и температура воды;
3. Значение рН, состав и концентрация минеральных примесей и растворенного кислорода;
4. Биохимическая потребность в кислороде;
5. Возбудители заболеваний, концентрация и состав ядовитых и вредных веществ.
Вредные и ядовитые вещества нормируют по принципу лимитирующего показателя вредности (ЛПВ), под которым понимают наиболее вероятное неблагоприятное воздействие каждого вещества.
При нормировании качества воды в водоемах питьевого и культурно-бытового назначения используют три вида ЛПВ:
1. санитарно-токсикологический;
2. общесанитарный;
3. органолептический.
Для водоемов рыбохозяйственного назначения наряду с указанными используют еще два вида ЛПВ:
4. токсикологический;
5. рыбохозяйственный.
Санитарное состояние водоема отвечает требованиям норм при выполнении соотношения:
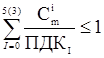 ,
,
где  - концентрация вещества i-ro ЛПВ в расчетном створе водоема, мг/л,
- концентрация вещества i-ro ЛПВ в расчетном створе водоема, мг/л,
ПДКi - предельно допустимая концентрация i-ro вещества, мг/л.
Для водоемов питьевого и культурно-бытового назначения проверяют выполнение трех, а для водоемов рыбохозяйственного назначения пяти неравенств. При этом каждое вещество можно учитывать только в одном неравенстве. "Санитарные правила и нормы охраны поверхностных вод от загрязнения" запрещают:
1. сбрасывать в водоемы сточные воды, если этого можно избежать (используя рациональную технологию, безводные процессы и системы повторного и оборонного водоснабжения);
2. если сточные воды содержат ценные отходы, которые можно утилизировать;
3. если сточные воды содержат сырье, реагенты и продукцию предприятий в количествах, превышающих технологические потери;
4. если сточные воды содержат вещества, для которых не установлены ПДК.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2879; Нарушение авторских прав?; Мы поможем в написании вашей работы!