
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Криві титрування кислот і основ
|
|
|
|
Інтервал переходу індикатора і показник заломлення.
З попереднього розділу видно, що для м. о., а це стосується і інших кислотно-основних індикаторів, при поступовій зміні рН розчину забарвлення індикатора змінюються досить різко. Цей інтервал носить назву інтервалу переходу індикатора. На основі наведеного прикладу можна сказати, що він складає
рН = рКінд ± 1;
тобто для м. о. складає 3-5.
У табл. 2 наведенні інтервали переходу та відповідні кольори для деяких найбільш вживаних в аналізі індикаторів
Таблиця 2
| індикатор | Інтервал переходу | рТ | Кольори |
| Тимолсиній | 1-3 | червоний-жовтий | |
| Метилоранжевий | 3-5 | червоний-жовтий | |
| Метилчервоний | 4-6 | червоний-жовтий | |
| Лакмус | 6-8 | червоний- синій | |
| Фенолфталеїн | 8-10 | безбарвний-червоний | |
| Тимолфталеїн | 9-11 | безбарвний-синій |
Проте, в об’ємному аналізі частіше користуються не інтервалом переходу, а показником титрування рТ. рТ є те значення рН розчину, при якому відбувається найбільш різка зміна його забарвлення. За допомогою величини рТ, яка у звичайних умовах спостереження вимірюється з точністю до ±0,3, визначають рН кінця титрування. З даних, наведених у табл. 2, видно, що рТ мають величини, близькі до рКінд, і вони знаходяться в середині інтервалу переходу.
Криві титрування є графічним зображенням зміни рН розчину при поступовому додаванні робочого розчину до певного об’єму розчину, що аналізується. Вони дають уявлення про те, наскільки різко змінюється р Н розчину поблизу точки еквівалентності.
Розглянемо побудову кривої титрування у випадку титрування сильної кислоти сильною основою. рН розчину обчислюється за відомими формулами: рН = - lgCHCl; рOН = - lgCNaOH; рН =14 – рOН. Зведемо необхідні для побудови дані у табл. 3. на титрування взято 0,1н розчину HCl. Зміною рН за рахунок розведення розчину, що титрується, нехтуємо.
|
|
|
 0.1н HCl 0.01н HCl
0.1н HCl 0.01н HCl
Рисунок 1 Криві титрування сильної кислоти сильною основою.
| Додано 0,1н розчину NaOH, мл | Електроліт, що визначає рН розчину | рН |
| 0,1н HCl | ||
| 90,0 | 0,01н HCl | |
| 99,0 | 0,001н HCl | |
| 99,9 | 0,0001н HCl | |
| 100,0 | NaCl | |
| 100,1 | 0,0001н NaCl | |
| 101,0 | 0,001н NaCl | |
| 110,0 | 0,01н NaCl | |
| 0,1н NaCl |
Зрозуміло, що при титруванні більш розведених розчинів титрантом меншої концентрації відповідна крива буде коротшою (синя лінія рис. 1).
Подібним чином можна розрахувати рН розчинів і побудувати криві титрування для інших випадків. Так, крива титрування слабкої кислоти сильною основою буде мати вигляд, зображений на рис. 2. нижня частина кривої має саме такий вигляд тому, що в результаті реакції утворюється буферна суміш CH3COOH- CH3COONa, яка втрачає свою дію лише при надлишку лугу.
При титруванні лугів (слабких основ) сильними кислотами відповідні криві мають перевернутий вигляд.
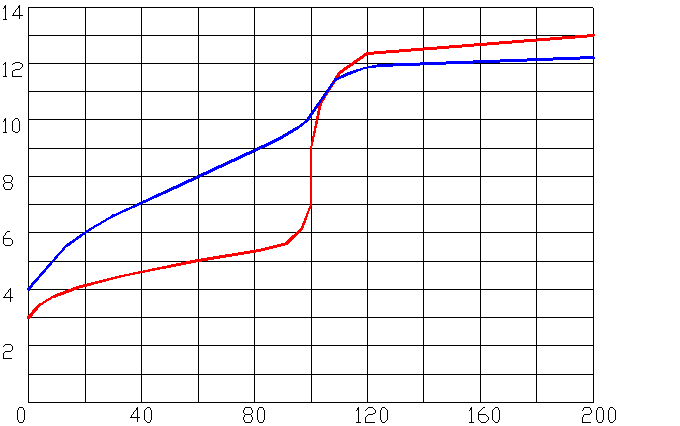 H3BO4 0.01н CH3COOH
H3BO4 0.01н CH3COOH
Рисунок 2 Криві титрування слабких кислот (CH3COOH i H3BO3) сильною основою (NaOH).
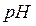 Вибір індикаторів кислотно-основного титрування.
Вибір індикаторів кислотно-основного титрування.
Головне правило при виборі найбільш придатного для титрування індикатора таке: рТ індикатора повинно бути як найближче до точки еквівалентності (а це точка перегину на кривій титрування), або, принаймні, інтервал переходу індикатора повинен входити на круту ділянку кривої.
Так, в першому випадку (рис 1) найкращим індикатором буде нейтральний червоний або лакмус (рТ =7). З невеличкою похибкою, проте, можна використовувати і метиловий оранжевий (рТ =4) і фенолфталеїн (рТ =9), однак ні в якому разі не можна брати тимол синій (рТ =2), чи тимолфталеїн (рТ =10), бо їх інтервал переходу не захоплює круту ділянку кривої.
Для другого випадку вимоги до індикатора значно посилюються. З рис. 2 видно, що застосування метилового оранжевого призводить до грубих помилок: індикатор змінить забарвлення задовго до точки еквівалентності, коли буде відтитровано менше половини оцтової кислоти. Точка еквівалентності зміщена від нейтральної реакції розчину (рН =7) до лужної (рН =8,9). Тому не бажано застосовувати індикатор типу лакмусу (рТ =7). Ідеальним індикатором, зрозуміло, тут буде фенолфталеїн.
|
|
|
Можна вибрати індикатор і без кривої титрування, розрахувавши за допомогою відомих формул рН розчину у точці еквівалентності. Але цей спосіб менш наглядний і зі зрозумілих причин таїть більше можливостей для помилок, ніж щойно розглянутий.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1509; Нарушение авторских прав?; Мы поможем в написании вашей работы!