
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Раскисление стали
|
|
|
|
Окислительные условия ведения плавки в сталеплавильных агрегатах, наличие окислительных шлаков, а также взаимодействие металла с атмосферой при выпуске и разливке - все это, вместе взятое, приводит к тому, что кислород, растворенный в стали, к моменту его выпуска имеет определенную, часто повышенную активность.
Влияние кислорода на свойства стали:
1. Кислород - основная причина старения стали, то есть кислород, избыточный по отношению к ферриту (a-Fe) в виде FeО выделяется в процессе кристаллизации. Выделение избыточной фазы из переохлажденного раствора сопровождается появлением большого количества зародышей зерен, фаза становится мелкодисперсной, выделяется по границам ферритных зерен, изменяя свойства сплава: пластичность, предел текучести, стойкость к коррозии снижаются; предел прочности возрастает. Изменение всего комплекса свойств стали называется старением металла.
2. Кислород, избыточный по отношению к аустениту (g-Fe), выделяется из металла в процессе кристаллизации, обогащая жидкую фазу, и взаимодействует с примесями Si, Al, Mn, образуя SiO2, Al2O3, MnO, то есть является причиной загрязнения стали неметаллическими включениями, которые ухудшают механические свойства стали.
3. В условиях кристаллизации, избыточный кислород взаимодействует с углеродом. Это взаимодействие приводит к газовыделению. С понижением температуры динамическая вязкость возрастает. Образующиеся пузыри газа {СО} не могут полностью удалиться из стали, и остаются в металле, определяя макроструктуру слитка, что делает невозможным получение плотной макроструктуры.
4. На завершающих стадиях охлаждения избыточный к a-Fe кислород выделяется в виде FeО по границам аустенитных зерен. При этом образуется эвтектика FeS-FeO с температурой плавления 910оС (температура плавления эвтектики FeS-Fe - 988оС), которая является причиной красноломкости стали, следовательно, избыточный кислород усиливает явление красноломкости стали.
|
|
|
Заключительным этапом любого сталеплавильного процесса является снижение концентрации кислорода до пределов, исключающих вредное влияние кислорода на свойства стали. Эта операция получила название раскисление. Существует три способа раскисления:
1. Осаждающее.
2. Диффузионное (экстракционное).
3. Раскисление в вакууме.
Осаждающее раскисление получило наибольшее распространение.Его суть заключается в снижении концентрации растворенного в металле кислорода путем перевода его в прочные конденсированные оксиды по схеме [О] + [Эл] = (ЭлО) и последующее их удаление из металла. Элементами чаще всего являются металлы активные к кислороду (Al, Si, Mn)
[О] + [Ме] = (МеО), (7.4‑1)
где [Ме] – элемент-раскислитель; (МеО) – продукт раскисления. Константа равновесия реакции (7.4-1) определяется
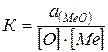 . (7.4‑2)
. (7.4‑2)
Следовательно, 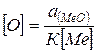 . (7.4‑3)
. (7.4‑3)
Эта равновесная концентрация кислорода в металле с продуктами раскисления и элементом-раскислителем получила название раскислительная способность. Чем ниже содержание кислорода в металле (¯ [О]), тем выше раскислительная способность. Из выражения (7.4-3) видно, что раскислительная способность определяется активностью продукта раскисления, константой равновесия реакции и концентрацией элемента раскислителя.
Константа равновесия зависит от температуры и сродства элемента-раскислителя к кислороду. Оценка раскислительной способности элементов лежит в основе решения первой задачи раскисляющего осаждения. Вторая задача – наиболее полное удаление из металла продуктов раскисления (неметаллические включения). Способы удаления неметаллических включений смотри в разделе 7.5. (способы обеспечения чистоты стали).
|
|
|
Комплексное раскисление стали. Металл раскисляют сильными и слабыми раскислителями в таком соотношении, чтобы они образовывали легкоплавкие соединения. Например, температура плавления оксида (MnO) составляет примерно 1600 оС, температура плавления соединения (MnO×SiO2) – 1270 оС, при выполнении условия легкоплавкости: [Mn]/[Si] ≥ 3-3,5.
При комплексном раскислении повышается раскислительная способность каждого из раскислителей. Это обусловлено снижением активности каждого оксида в продуктах раскисления. Так, при одновременном раскислении кремнием и марганцем область жидких сплавов FeO-MnO-SiO2 расширяется. Раскислительная способность алюминия увеличивается также в присутствии марганца. На этом принципе основано применение ряда комплексных раскислителей и лигатур. Применение комплексных лигатур объясняется также быстрым удалением комплексных продуктов раскисления из металла, благоприятной формой оставшихся в металле оксидных включений, меньшим их отрицательным влиянием на служебные свойства стали и т.п.
Диффузионное (экстракционное) раскисление основано на изменении условий равновесного распределения кислорода между металлом и шлаком. Поскольку кислород в виде FeO достаточно хорошо растворяется и в шлаке, и в металле, то согласно закону распределения Нернста-Шилова при Т = const
[FeO]/ (FeO) = const = LFeO. (7.4‑4)
В условиях постоянства этой величины добиться снижения содержания кислорода в металле можно за счет снижения концентрации [FeO] в металле следующими способами:
1. За счет увеличения количества шлака, что экономически не выгодно.
2. Перевод [FeO] в другие соединения нерастворимые в металле, например 2(FeO) + [Si] = (SiO2) + 2[Fe] (7.4‑5)
или (FeO) + [C] = [Fe] + {CO}. (7.4‑6)
Здесь оксид (SiO2) не растворяется в металле, а оксид {CO} не растворяется ни в металле, ни в шлаке. Раскисляя шлак, добиваются раскисления металла. В качестве раскислителей, вводимых в шлак, используют кокс, электродный бой, ферросилиций, алюминий и др.
Переход [FeO] ® (FeO) происходит до установления постоянства коэффициента распределения. Этот переход при нарушении равновесия осуществляется диффузией. Поэтому раскисление называется диффузионным.
|
|
|
Основное достоинство – процесс не связан с загрязнением металла продуктами раскисления, следовательно, обеспечивается более высокое качество стали.
Недостаток – процессы диффузионного распределения между металлом и шлаком носят затяжной характер. Поэтому на раскисление требуются большие затраты времени. В результате, низкая производительность процесса и высокая стоимость стали. По этому способу раскисляются стали высокого качества
Раскисление в вакууме основано на возрастающей раскисляющей способности углерода при снижении внешнего давления
[С] + [О] = {СО}, (7.4‑7)
 . (7.4‑8)
. (7.4‑8)
Условие протекания реакции: Рсо ³ Рв . Соотношение (7.4-8) характеризует раскисляющую способность углерода в зависимости от внешнего давления. При снижении Рв содержание кислорода [О] также понизится.
Достоинство данного способа раскисления заключается в том, что раскисление металла не сопровождается загрязнением металла неметаллическими включениями, следовательно, обеспечивается высокое качество металла.
Недостаток – необходимо дорогостоящее оборудование.
Диффузионное раскисление в вакууме применяется для получения специальных высококачественных сталей (трансформаторная сталь)
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1721; Нарушение авторских прав?; Мы поможем в написании вашей работы!