
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Модели каталитического процесса
|
|
|
|
1) Модель с равнодоступной поверхностью;
2) Модель с неравнодоступной поверхностью.
Квазигомогенная модель берется за основу, т. е. процесс идет по всему объему частицы одновременно.
Модель с равнодоступной поверхностью.
(теория Ленгмюра).
Допущения:
1) Между адсорбированными молекулами не действуют силы притяжения и отталкивания;
2) Процесс адсорбции заканчивается, когда все центры заняты;
3) Все центры являются равнозначными.
Доля занятой поверхности катализатора θ.
1. 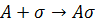
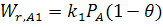 – скорость адсорбции,
– скорость адсорбции,
где 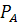 – давление.
– давление.
2. Десорбция

активный центр освобождается.
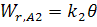 – скорость десорбции.
– скорость десорбции.
При равновесии 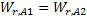 ;
;
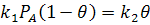
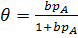
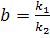
Скорость всего каталитического процесса
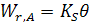 ,
,
 − эффективная константа скорости всего процесса.
− эффективная константа скорости всего процесса.
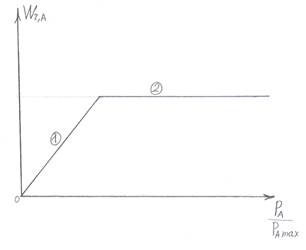
Случаи:
1) низкое давление PA; 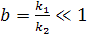
Слабая адсорбция.
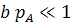 ;
; 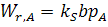 ,
,  − линейная адсорбция.
− линейная адсорбция.
2) высокое давление PA;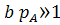
Сильная адсорбция.
θ=1, вся поверхность занята.
Модель с неравнодоступной поверхностью.
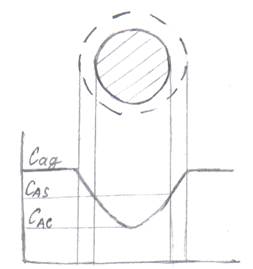
Эффективность процесса ε – коэффициент использования внутренней поверхности катализатора.
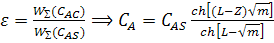
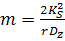 , где Dz – коэффициент диффузии.
, где Dz – коэффициент диффузии.
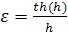 , где h – модуль Тиле.
, где h – модуль Тиле.
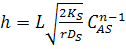

|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 487; Нарушение авторских прав?; Мы поможем в написании вашей работы!