
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Находим
|
|
|
|
Сравнивая это выражение с уравнением Ван-дер-Ваальса
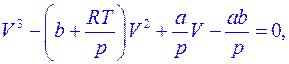
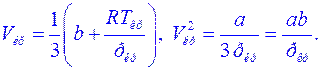
Откуда 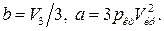 Переходя к приведенным переменным, получаем искомое уравнение.
Переходя к приведенным переменным, получаем искомое уравнение.
Отметим здесь следующее важное свойство. Из последних двух равенств получаем, что TкрR/(pкрVкр) = 8/3 ≈ 2,67. Для идеального газа это соотношение, как известно, тождественно равно 1 согласно уравнению Клапейрона-Менделеева. Однако для реальных газов эта величина в среднем равна примерно 3,7 при разбросе, в основном, от 3 до 6. Таким образом, уравнение Ван-дер-Ваальса более точно описывает реальные свойства, поскольку величина 2,67 ближе к 3,7, чем единица.
Критическое давление – давление, при котором газообразный углеводород переходит в жидкое состояние.
Критическая температура – температура, при которой жидкий углеводород переходит в газообразное состояние.
Приведёнными параметрами индивидуальных компонентов называются безразмерные величины, показывающие, во сколько раз действительные параметры состояния газа отклоняются от критических:
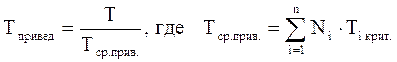 (3.20)
(3.20)
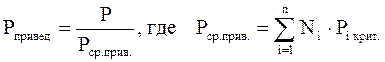 (3.21)
(3.21)
z = f (Тприв, Рприв) (3.22)
|
|
|
Дата добавления: 2014-01-04; Просмотров: 273; Нарушение авторских прав?; Мы поможем в написании вашей работы!